Título
Rol de los Corticoides en el Trauma de Cráneo Severo: Un Interrogante no Resuelto
Autor
Patricia Maggiora
Alberto Gidekel
Fecha
Septiembre 2004
Lugar de Realización
División Neurocirugía, Hospital "Dr. Cosme Argerich", Buenos Aires
Correspondencia
patomaggiora@hotmail.com
Texto
Rev. Argent. Neuroc. 2004, 18: 152
Patología traumática
División Neurocirugía, Hospital "Dr. Cosme Argerich", Buenos Aires
Correspondencia: Tomás Liberti 425 Piso 8° Dto P (1 156) Buenos Aires.
E-mail: patomaggiora@hotmail.com
ABSTRACT
Objective: To evaluate the effectiveness of corticosteroids in the management of traumatic brain injury.
Methods: Trials concerning administration of corticosteroids to patients sustaining acute head injury were identified by means of electronic searches of MEDLINE. Articles related to pharmacology of corticosteroids, with special emphasis on potential neuroprotective activities were reviewed.
Results: Nineteen trials were identified, showing, except for a few, no statistical difference in outcome or mortality between patients receiving corticosteroids or placebo. Nevertheless, a tendency was noticed towards a small number of deaths in the treated group. There was no statistical difference between groups concerning gastrointestinal bleeding or other major complications. The analysis of the available literature on corticosteroids pharmacology provided a wide range of potentially beneficial effects through direct (receptor independent) and indirect actions, including among others, anti-inflammatory, membrane stabilizing, anti-oxidant and energetic metabolism protecting activities.
Conclusion: Corticosteroids given acutely to patients sustaining severe head injury resulted in a small but statistically insignificant reduction in mortality. There was no significant difference between corticosteroid and control groups in mortality, nor in the rates of gastrointestinal bleeding or infection. Because of the relatively small number of patients previously enrolled in corticosteroids versus placebo trials, small reductions in mortality or deleterious effects associated with corticosteroid administration cannot be excluded.
Key words: Corticosteroids, Randomized trials, Traumatic brain injury.
Palabras clave: corticoides, ensayos aleatorizados, trauma de cráneo.
INTRODUCCIÓN
Los corticosteroides han sido utilizados en el tratamiento del traumatismo encéfalo craneano (TEC) en forma empírica durante décadas, desapareciendo y reapareciendo según los dictámenes de la moda, pero nunca en base a evidencia científica concluyente.
La evidencia experimental en animales demostró efectos beneficiosos claros. Sin embargo, los múltiples estudios realizados en humanos aportan resultados disímiles y de dificil interpretación.
El presente trabajo constituye una revisión de la bibliografía acerca del uso de esteroides en el TEC, poniendo énfasis en la fisiopatología del mismo, la farmacología de los corticosteroides y las bases científicas de su utilización.
MATERIAL Y MÉTODO
Se analizaron las publicaciones concernientes a fisiopatología del TEC, farmacología de corticosteroides y fundamentos de su uso en el tratamiento de dicha patología, emitidas desde 1984 en adelante. Asimismo, se realizó una revisión de los estudios clínicos sobre uso de corticosteroides en el TEC. con un número total de diecinueve, el primero de los cuales data de 1979.
RESULTADOS Y DISCUSIÓN
FISIOPATOLOGÍA DEL TEC
El trauma agudo afecta al tejido nervioso desde el punto de vista anatómico y funcional, incluyendo esta última categoría los niveles tisular y celular. Citando a Hall1, "mucho de la fisiopatología del daño postraumático evoluciona rápidamente y es largamente irreversible", lo cual puede explicar el relativamente magro beneficio que parecen aportar la mayoría de las intervenciones terapéuticas actualmente disponibles2.
El trauma encéfalocraneano genera en el paciente dos tipos de daño: uno primario, producido en forma directa por la noxa (contusiones, laceraciones, lesión axonal difusa, etc.), y otro secundario, que perpetúa y agrava la lesión inicial (Fig. 1).
El daño secundario depende de la activación de la cascada inflamatoria, liberación de excitotoxinas y radicales libres de oxígeno, peroxidación lipídica, alteración de la vasomotricidad y la permeabilidad vascular, y disfunción de las membranas astrocitaria y neuronal, llevando finalmente a la muerte celular2,3: es aquí donde los corticoides resultan potencialmente útiles, debido a sus propiedades de estabilizantes de membrana y antiinflamatorias.
TEC Y ESTEROIDES
Resultados de la investigación clínica previa
En los últimos treinta años, a partir de resultados alentadores en el campo de la experimentación en animales y en ausencia de otras intervenciones terapéuticas que demostraran efectos favorables en el TEC más allá de las destinadas a optimizar las funciones vitales básicas, se realizaron múltiples estudios clínicos destinados a evaluar la utilidad de los corticosteroides. Sin embargo, ninguno de ellos aportó información consistente acerca de los resultados terapéuticos o efectos adversos. Según un metaanálisis de dichos estudios realizado por Alderson y Roberts4, las fallas de los mismos en cumplir sus objetivos se deberían a errores de diseño (errores de randomización, ausencia de grupo control, falta de estandarización de los tratamientos...), número escaso de pacientes o deficiencias en el tratamiento estadístico de la información, no pudiéndose, a partir de la información disponible, descartarse ni asegurarse un beneficio moderado a partir del uso de los corticosteroides.
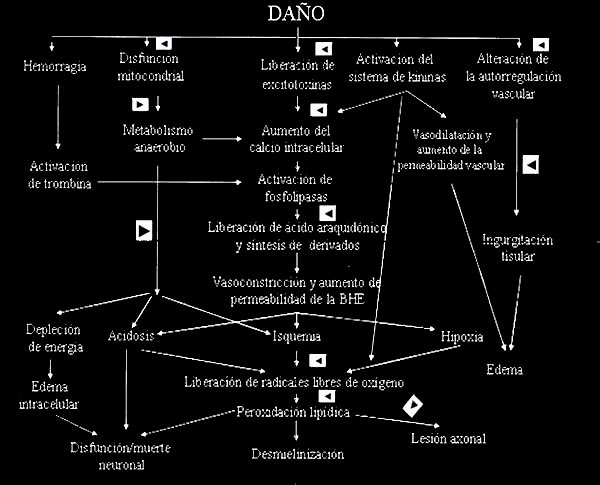
Fig. 1. Mecanismos de daño secundario. Las puntas de flecha señalan los sitios teóricos de acción de los esteroides
BASES FARMACOLÓGICAS DEL USO DE ESTEROIDES EN EL TEC
La elección de los esteroides como posibles modificadores de la evolución en el TEC depende de varios factores, pero fundamentalmente se basa en sus propiedades antiinflamatorias, inmunomoduladoras y estabilizantes de membrana. En los últimos treinta años se han ensayado clínicamente en varias oportunidades en base a muy estimulantes resultados en el plano experimental, utilizando múltiples formas moleculares (hidrocortisona, dexametasona, metilprednisolona y triamcinolona), dosis, duraciones de tratamiento, etc.. Lamentablemente, ha sido virtualmente imposible reproducir los beneficios hallados experimentalmente en el plano clínico, hecho que se repite en el caso de otras drogas potencialmente efectivas como los antagonistas de los receptores NMDA y los bloqueantes cálcicos.
Mecanismos de acción
En 1980, Demopoulos et al propusieron a la peroxidación lipídica inducida por radicales libres como el mecanismo fundamental en la degeneración neuronal postraumática (a la que luego se agregarían la alteración del metabolismo energético y la neurotoxicidad mediada por excitotoxinas). A partir de esta premisa, se centró la atención en los procesos generadores de dichos radicales libres y en la búsqueda de fármacos antioxidantes.
En los años siguientes, la experimentación en animales demostró que la metilprednisolona y en menor grado dexametasona y prednisona, eran capaces de disminuir la peroxidación lipídica en homogenados de médula ósea de gatos sometidos a trauma raquimedular. Por otra parte, la evaluación de las cantidades de metilprednisolona requeridas para obtener dicho efecto demostró como óptimas las dosis de 30 mg/kg (muchísimo mayores de las requeridas para saturar a los receptores de esteroides), teniendo dosis menores o de 60 mg/kg efecto nulo, y dosis de 90 mg/kg o más un efecto francamente facilitador de la peroxidacióni. Estos hallazgos llevaron a la conclusión de que los efectos favorables de la metilprednisolona estaban mediados, al menos en parte, por una actividad antioxidante intrínseca de la molécula y separada del efecto mediado a través de sus receptores nucleares (Fig. 2). En estas premisas, se basó el estudio clínico NASCISS II, cuyos resultados introdujeron como recomendación el uso de metilprednisolona en el trauma medular agudo y sugirieron la posible utilidad en el TEC.
Por otra parte, Casanova sugirió que la metilprednisolona era capaz de disminuir la permeabilidad del endotelio vascular, y consecuentemente la formación de edema, a través de la formación de uniones hidrófobas en las membranas celulares y el impedimento de los mecanismos de endocitosis. Ildan et al, demostraron en ratas que la metilprednisolona producía en tejido cerebral sometido a trauma la activación de la ATPasa de Na+ K+ Mg2+, que mejoraría el ambiente iónico intracelular y contribuiría a mantener la homeostasis de las células involucradas.
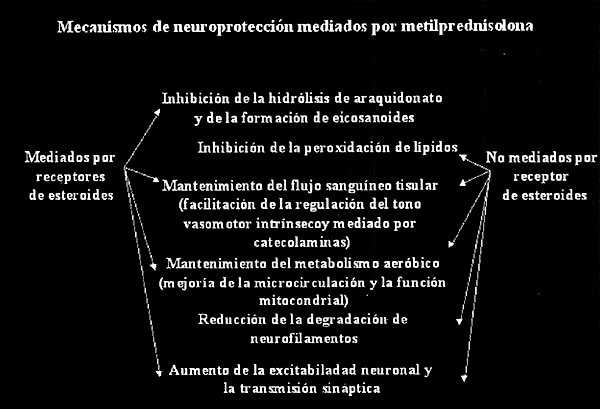
Fig. 2. Mecanismos de neuroprotección mediados por melilprednisoiona
Además de la actividad antioxidante de la metilprednisolona, la investigación de los años siguientes demostró otros mecanismos de neuroprotección mediados por dicha droga a través de los receptores de esteroides. Un ejemplo de esto estaría dado por el hecho de que en el 15% de los pacientes críticos con TEC que muestran insuficiencia suprarrenal y dependencia de vasopresores, presenta mejoría de la inestabilidad hemodinámica y de la respuesta a inotrópicos luego de dosis de reposición de corticosteroides. Sin embargo, esta acción no seria tan relevante como la antioxidante.
Falkenstein et al5, mostraron la existencia de un segundo grupo de receptores de hormonas esteroideas, ubicados en la membrana citoplasmática de las células blanco. Estos receptores estarían asociados a sistemas de segundos mensajeros y serian activados por la unión simultánea de dos ligandos, siendo uno un esteroide (Fig. 3). De esta manera, las concentraciones de ambas moléculas serian moduladoras de la activación del sistema. Esto ha sido corroborado a raíz del descubrimiento de los "neuroesteroides endógenos", grupo de moléculas producidas intra y extra cerebralmente, que serian responsables de facili tar la activación o inactivación de ciertos receptores, como los GABAérgicos. Los neuroesteroides derivados de pregnanos serian entonces capaces de aumentar en un 100% la conductancia al Cl- en presencia de otro agonista GABAérgico, generando disminución de la excitabilidad en ciertos grupos neuronales, lo cual les conferiría actividad anticonvulsivante, por ejemplo. Resta investigar si los esteroides exógenos probados en el TEC tienen a estos sistemas como posibles sitios de acción.
Sin embargo, y a pesar de la extensa evidencia experimental concerniente a acciones neuroprotectoras de los esteroides, la comprobación clínica no se ha presentado aún en forma concreta. Algunos investigadores sugieren que, además del carácter multifactorial, complejo y evolutivo de las lesiones en situaciones no controladas, esto podría deberse a que la inhibición de ciertos procesos lesivos secundarios a partir de una intervención farmacológica podría activar o incluso incrementar el daño a través de mecanismos alternativos: así, por ejemplo, la metilprednisolona seria por un lado capaz de inhibir la lesión oxidativa de las membranas celulares a corto plazo, pero seria responsable a mediano plazo de la activación de sistemas intracelulares mediadores de apoptosis en neuronas, lo cual no seria detectado al evaluar la respuesta a corto plazo en preparados histológicos. Esto llevaría a afirmar que no se dispone actualmente de modelos experimentales representativos de TEC.

Fig. 3. Clasificación de Mannheim de las respuestas no genómicas mediadas por hormonas esteroides. Las lineas interrumpidas implican mecanismos hipotéticos de los cuales no se dispone de ejemplo experimental
CONCLUSIÓN
El TEC es una de las mayores causas de muerte e incapacidad en el mundo desarrollado y una de las patologías en las que no se dispone de un tratamiento farmacológico efectivo. Mucho de su fisiopatología persiste sin ser develada, lo cual dificulta el desarrollo de maniobras terapéuticas.
Los corticosteroides han sido utilizados en el tratamiento del TEC en forma empírica durante décadas. Si bien gozan de una amplia base experimental a favor de sus actividades neuroprotectoras, estos notables resultados no han podido ser repetidos en la práctica clínica, posiblemente debido al carácter raramente aislado, complejo, eminentemente multifactorial y rápidamente evolutivo del TEC. Sin embargo, los datos obtenidos de la investigación clínica no permiten descartar ni asegurar un beneficio ni un efecto deletéreo moderado a partir del uso de esteroides en esta patología, por lo cual se requerirá un gran número de pacientes en búsqueda de resultados más representativos.
En los años por venir, quizá el estudio multicéntrico randomizado CRASH (Corticosteroid Randomization After Significant Head Injury)6 aporte información suficiente para la formulación de nuevas recomendaciones sobre el uso de esteroides en el TEC, como en su momento ocurriera con el Chinese Acute Stroke Trial- CAST (aspirina versus placebo) en el accidente cerebrovascular isquémico.
Bibliografía
1. Hall E. The neuroprotective pharmacology of methilprednisolone. J Neurosurg 1992; 76: 13-20.
2. Teasdale GM. Current status of neuroprotection trials for traumatic brain injury: lessons from animal models and clinical studies. Neurosurgery 1999; 45: 207-20,
3. Marmarou A. Pathophysiology of traumatic brain edema: current concepts. Acta Neurochir (Wien) (Suppl.) 2003; 86: 7-10
4. Alderson P, Roberts I. Corticosteroids in acute traumatic brain injury: a systematic review of randomised trials. BMJ 1997; 314: 1855-9.
5. Falkenstein E, Tillmann H, Feuring M, Wehling M. Multiple Actions of Steroid Hormones: A Focus on Rapid, Nongenomic Effects. Pharmacol Rev 2000; 52: 513-56.
6. MRC CRASH Trial National Coordinators. Update on progress in the international multicenter, randomized, controlled trial of corticosteroids after significant head injury (Medical Research Councill CASH Trial) Curr Open Crit Care 2003; 9: 92-7.
Patología traumática
Rol de los Corticoides en el Trauma de Cráneo Severo: Un Interrogante no Resuelto
Patricia Maggiora, Alberto GidekelDivisión Neurocirugía, Hospital "Dr. Cosme Argerich", Buenos Aires
Correspondencia: Tomás Liberti 425 Piso 8° Dto P (1 156) Buenos Aires.
E-mail: patomaggiora@hotmail.com
ABSTRACT
Objective: To evaluate the effectiveness of corticosteroids in the management of traumatic brain injury.
Methods: Trials concerning administration of corticosteroids to patients sustaining acute head injury were identified by means of electronic searches of MEDLINE. Articles related to pharmacology of corticosteroids, with special emphasis on potential neuroprotective activities were reviewed.
Results: Nineteen trials were identified, showing, except for a few, no statistical difference in outcome or mortality between patients receiving corticosteroids or placebo. Nevertheless, a tendency was noticed towards a small number of deaths in the treated group. There was no statistical difference between groups concerning gastrointestinal bleeding or other major complications. The analysis of the available literature on corticosteroids pharmacology provided a wide range of potentially beneficial effects through direct (receptor independent) and indirect actions, including among others, anti-inflammatory, membrane stabilizing, anti-oxidant and energetic metabolism protecting activities.
Conclusion: Corticosteroids given acutely to patients sustaining severe head injury resulted in a small but statistically insignificant reduction in mortality. There was no significant difference between corticosteroid and control groups in mortality, nor in the rates of gastrointestinal bleeding or infection. Because of the relatively small number of patients previously enrolled in corticosteroids versus placebo trials, small reductions in mortality or deleterious effects associated with corticosteroid administration cannot be excluded.
Key words: Corticosteroids, Randomized trials, Traumatic brain injury.
Palabras clave: corticoides, ensayos aleatorizados, trauma de cráneo.
INTRODUCCIÓN
Los corticosteroides han sido utilizados en el tratamiento del traumatismo encéfalo craneano (TEC) en forma empírica durante décadas, desapareciendo y reapareciendo según los dictámenes de la moda, pero nunca en base a evidencia científica concluyente.
La evidencia experimental en animales demostró efectos beneficiosos claros. Sin embargo, los múltiples estudios realizados en humanos aportan resultados disímiles y de dificil interpretación.
El presente trabajo constituye una revisión de la bibliografía acerca del uso de esteroides en el TEC, poniendo énfasis en la fisiopatología del mismo, la farmacología de los corticosteroides y las bases científicas de su utilización.
MATERIAL Y MÉTODO
Se analizaron las publicaciones concernientes a fisiopatología del TEC, farmacología de corticosteroides y fundamentos de su uso en el tratamiento de dicha patología, emitidas desde 1984 en adelante. Asimismo, se realizó una revisión de los estudios clínicos sobre uso de corticosteroides en el TEC. con un número total de diecinueve, el primero de los cuales data de 1979.
RESULTADOS Y DISCUSIÓN
FISIOPATOLOGÍA DEL TEC
El trauma agudo afecta al tejido nervioso desde el punto de vista anatómico y funcional, incluyendo esta última categoría los niveles tisular y celular. Citando a Hall1, "mucho de la fisiopatología del daño postraumático evoluciona rápidamente y es largamente irreversible", lo cual puede explicar el relativamente magro beneficio que parecen aportar la mayoría de las intervenciones terapéuticas actualmente disponibles2.
El trauma encéfalocraneano genera en el paciente dos tipos de daño: uno primario, producido en forma directa por la noxa (contusiones, laceraciones, lesión axonal difusa, etc.), y otro secundario, que perpetúa y agrava la lesión inicial (Fig. 1).
El daño secundario depende de la activación de la cascada inflamatoria, liberación de excitotoxinas y radicales libres de oxígeno, peroxidación lipídica, alteración de la vasomotricidad y la permeabilidad vascular, y disfunción de las membranas astrocitaria y neuronal, llevando finalmente a la muerte celular2,3: es aquí donde los corticoides resultan potencialmente útiles, debido a sus propiedades de estabilizantes de membrana y antiinflamatorias.
TEC Y ESTEROIDES
Resultados de la investigación clínica previa
En los últimos treinta años, a partir de resultados alentadores en el campo de la experimentación en animales y en ausencia de otras intervenciones terapéuticas que demostraran efectos favorables en el TEC más allá de las destinadas a optimizar las funciones vitales básicas, se realizaron múltiples estudios clínicos destinados a evaluar la utilidad de los corticosteroides. Sin embargo, ninguno de ellos aportó información consistente acerca de los resultados terapéuticos o efectos adversos. Según un metaanálisis de dichos estudios realizado por Alderson y Roberts4, las fallas de los mismos en cumplir sus objetivos se deberían a errores de diseño (errores de randomización, ausencia de grupo control, falta de estandarización de los tratamientos...), número escaso de pacientes o deficiencias en el tratamiento estadístico de la información, no pudiéndose, a partir de la información disponible, descartarse ni asegurarse un beneficio moderado a partir del uso de los corticosteroides.

Fig. 1. Mecanismos de daño secundario. Las puntas de flecha señalan los sitios teóricos de acción de los esteroides
BASES FARMACOLÓGICAS DEL USO DE ESTEROIDES EN EL TEC
La elección de los esteroides como posibles modificadores de la evolución en el TEC depende de varios factores, pero fundamentalmente se basa en sus propiedades antiinflamatorias, inmunomoduladoras y estabilizantes de membrana. En los últimos treinta años se han ensayado clínicamente en varias oportunidades en base a muy estimulantes resultados en el plano experimental, utilizando múltiples formas moleculares (hidrocortisona, dexametasona, metilprednisolona y triamcinolona), dosis, duraciones de tratamiento, etc.. Lamentablemente, ha sido virtualmente imposible reproducir los beneficios hallados experimentalmente en el plano clínico, hecho que se repite en el caso de otras drogas potencialmente efectivas como los antagonistas de los receptores NMDA y los bloqueantes cálcicos.
Mecanismos de acción
En 1980, Demopoulos et al propusieron a la peroxidación lipídica inducida por radicales libres como el mecanismo fundamental en la degeneración neuronal postraumática (a la que luego se agregarían la alteración del metabolismo energético y la neurotoxicidad mediada por excitotoxinas). A partir de esta premisa, se centró la atención en los procesos generadores de dichos radicales libres y en la búsqueda de fármacos antioxidantes.
En los años siguientes, la experimentación en animales demostró que la metilprednisolona y en menor grado dexametasona y prednisona, eran capaces de disminuir la peroxidación lipídica en homogenados de médula ósea de gatos sometidos a trauma raquimedular. Por otra parte, la evaluación de las cantidades de metilprednisolona requeridas para obtener dicho efecto demostró como óptimas las dosis de 30 mg/kg (muchísimo mayores de las requeridas para saturar a los receptores de esteroides), teniendo dosis menores o de 60 mg/kg efecto nulo, y dosis de 90 mg/kg o más un efecto francamente facilitador de la peroxidacióni. Estos hallazgos llevaron a la conclusión de que los efectos favorables de la metilprednisolona estaban mediados, al menos en parte, por una actividad antioxidante intrínseca de la molécula y separada del efecto mediado a través de sus receptores nucleares (Fig. 2). En estas premisas, se basó el estudio clínico NASCISS II, cuyos resultados introdujeron como recomendación el uso de metilprednisolona en el trauma medular agudo y sugirieron la posible utilidad en el TEC.
Por otra parte, Casanova sugirió que la metilprednisolona era capaz de disminuir la permeabilidad del endotelio vascular, y consecuentemente la formación de edema, a través de la formación de uniones hidrófobas en las membranas celulares y el impedimento de los mecanismos de endocitosis. Ildan et al, demostraron en ratas que la metilprednisolona producía en tejido cerebral sometido a trauma la activación de la ATPasa de Na+ K+ Mg2+, que mejoraría el ambiente iónico intracelular y contribuiría a mantener la homeostasis de las células involucradas.

Fig. 2. Mecanismos de neuroprotección mediados por melilprednisoiona
Además de la actividad antioxidante de la metilprednisolona, la investigación de los años siguientes demostró otros mecanismos de neuroprotección mediados por dicha droga a través de los receptores de esteroides. Un ejemplo de esto estaría dado por el hecho de que en el 15% de los pacientes críticos con TEC que muestran insuficiencia suprarrenal y dependencia de vasopresores, presenta mejoría de la inestabilidad hemodinámica y de la respuesta a inotrópicos luego de dosis de reposición de corticosteroides. Sin embargo, esta acción no seria tan relevante como la antioxidante.
Falkenstein et al5, mostraron la existencia de un segundo grupo de receptores de hormonas esteroideas, ubicados en la membrana citoplasmática de las células blanco. Estos receptores estarían asociados a sistemas de segundos mensajeros y serian activados por la unión simultánea de dos ligandos, siendo uno un esteroide (Fig. 3). De esta manera, las concentraciones de ambas moléculas serian moduladoras de la activación del sistema. Esto ha sido corroborado a raíz del descubrimiento de los "neuroesteroides endógenos", grupo de moléculas producidas intra y extra cerebralmente, que serian responsables de facili tar la activación o inactivación de ciertos receptores, como los GABAérgicos. Los neuroesteroides derivados de pregnanos serian entonces capaces de aumentar en un 100% la conductancia al Cl- en presencia de otro agonista GABAérgico, generando disminución de la excitabilidad en ciertos grupos neuronales, lo cual les conferiría actividad anticonvulsivante, por ejemplo. Resta investigar si los esteroides exógenos probados en el TEC tienen a estos sistemas como posibles sitios de acción.
Sin embargo, y a pesar de la extensa evidencia experimental concerniente a acciones neuroprotectoras de los esteroides, la comprobación clínica no se ha presentado aún en forma concreta. Algunos investigadores sugieren que, además del carácter multifactorial, complejo y evolutivo de las lesiones en situaciones no controladas, esto podría deberse a que la inhibición de ciertos procesos lesivos secundarios a partir de una intervención farmacológica podría activar o incluso incrementar el daño a través de mecanismos alternativos: así, por ejemplo, la metilprednisolona seria por un lado capaz de inhibir la lesión oxidativa de las membranas celulares a corto plazo, pero seria responsable a mediano plazo de la activación de sistemas intracelulares mediadores de apoptosis en neuronas, lo cual no seria detectado al evaluar la respuesta a corto plazo en preparados histológicos. Esto llevaría a afirmar que no se dispone actualmente de modelos experimentales representativos de TEC.

Fig. 3. Clasificación de Mannheim de las respuestas no genómicas mediadas por hormonas esteroides. Las lineas interrumpidas implican mecanismos hipotéticos de los cuales no se dispone de ejemplo experimental
CONCLUSIÓN
El TEC es una de las mayores causas de muerte e incapacidad en el mundo desarrollado y una de las patologías en las que no se dispone de un tratamiento farmacológico efectivo. Mucho de su fisiopatología persiste sin ser develada, lo cual dificulta el desarrollo de maniobras terapéuticas.
Los corticosteroides han sido utilizados en el tratamiento del TEC en forma empírica durante décadas. Si bien gozan de una amplia base experimental a favor de sus actividades neuroprotectoras, estos notables resultados no han podido ser repetidos en la práctica clínica, posiblemente debido al carácter raramente aislado, complejo, eminentemente multifactorial y rápidamente evolutivo del TEC. Sin embargo, los datos obtenidos de la investigación clínica no permiten descartar ni asegurar un beneficio ni un efecto deletéreo moderado a partir del uso de esteroides en esta patología, por lo cual se requerirá un gran número de pacientes en búsqueda de resultados más representativos.
En los años por venir, quizá el estudio multicéntrico randomizado CRASH (Corticosteroid Randomization After Significant Head Injury)6 aporte información suficiente para la formulación de nuevas recomendaciones sobre el uso de esteroides en el TEC, como en su momento ocurriera con el Chinese Acute Stroke Trial- CAST (aspirina versus placebo) en el accidente cerebrovascular isquémico.
Bibliografía
1. Hall E. The neuroprotective pharmacology of methilprednisolone. J Neurosurg 1992; 76: 13-20.
2. Teasdale GM. Current status of neuroprotection trials for traumatic brain injury: lessons from animal models and clinical studies. Neurosurgery 1999; 45: 207-20,
3. Marmarou A. Pathophysiology of traumatic brain edema: current concepts. Acta Neurochir (Wien) (Suppl.) 2003; 86: 7-10
4. Alderson P, Roberts I. Corticosteroids in acute traumatic brain injury: a systematic review of randomised trials. BMJ 1997; 314: 1855-9.
5. Falkenstein E, Tillmann H, Feuring M, Wehling M. Multiple Actions of Steroid Hormones: A Focus on Rapid, Nongenomic Effects. Pharmacol Rev 2000; 52: 513-56.
6. MRC CRASH Trial National Coordinators. Update on progress in the international multicenter, randomized, controlled trial of corticosteroids after significant head injury (Medical Research Councill CASH Trial) Curr Open Crit Care 2003; 9: 92-7.
