Título
Hipertensión Endocraneana y Traumatismo Encefalo Craneano. Revisión Conceptual
Autor
H. Fontana
H, Belziti
Fecha
Junio 1995
Lugar de Realización
Servicio de Nurocirugía del Hospital de San Isidro, Provincia de Buenos Aires
Texto
Revista Argentina de Neurocirugía 9: 73, 1995
Actualización
Hipertensión Endocraneana y Traumatismo Encefalo Craneano. Revisión Conceptual
H. Fontana, H, Belziti
Servicio de Nurocirugía del Hospital de San Isidro, Provincia de Buenos Aires
Correspondencia: Dr. H. Fontana, Arrotea 746, Depto A (I406) Buenos Aires
RESUMEN
Aparece hipertensión endocraneana cuando hay un bloqueo a la circulación de LCR. Este se produce por ubicación estratégica de la masa respecto a las vías de LCR, o por desplazamiento y hernia encefálicos,
Los signos neurorradiológicos de hipertensión endocraneana (ocupación de la cisterna ambiens y dilatación ventricular) son fiables.
Cuando los acontecimientos se desarrollan en forma aguda, los síntomas del paciente son más bien del desplazamiento y hernia encefálicos, que de hipertensión endocraneana. Los síntomas del desplazamiento se deben probablemente a isquemia focal del tronco cerebral por distorsión de los vasos perforantes del tronco alto. Esta puede producir infartos o hemorragias que generen estado vegetativo persistente, o sean causa de muerte, antes que la HIC comprometa el flujo en forma difusa.
La cirugía corrige el desplazamiento y hernia encefálicos. Si no está indicada o es tardía, las terapéuticas médicas basadas en el control de la PIC, muchas veces no pueden revertir la hernia, y por ello, también pueden fallar en el control de la hipertensión endocraneana. La presencia de "rebote" significaría persistencia o recidiva del bloqueo. El descenso transitorio de los valores de PIC no significa necesariamente una mejoría de la situación del paciente.
El efecto deletéreo de la HIC se produce por disminución del flujo cerebral y eventual detención circulatoria, en etapas avanzadas y posiblemente irreversibles del proceso.
El registro de la PIC como el de otros parámetros globales, pasa por alto una serie importante de sucesos focales relacionadas con ella (presiones tisulares en los focas lesionales) que son de gran importancia flsiopatológica y terapéutica.
El monitoreo de la PIC en el tratamiento del TEC grave es útil para el diagnóstico de la hernia encefálica, el control del resultado de la terapéutica y en la indicación quirúrgica en casos dudosos. Las lesiones que producen edema cerebral difuso, generarán hipertensión endocraneana sólo si ocasionan bloqueo. Al no haber desplazamiento horizontal y ser el edema un actor etiológico en estos casos, el tratamiento médico tiene mejores perspectivas, si alcanza a revertir el bloqueo a tiempo.
Una interpretación fisiopatológica adecuada de los sucesos intracraneanos luego de unTEC cerrado, debe incluir sistemáticamente la acomodación de volumen y el desplazamiento y hernia encefálicos, para guiar una terapia coherente.
Palabras clave: hipertensión endocraneeana, traumatismo craneoencefálico, hernia encefálica
ABSTRACT
Sustained intracranial hypertension is due to a blockade to the circulation of CSF, produced by a strategic location of the mass in respect to the ventricular system, or hrough encephalic displacement and hemiation.
Occupation of the ambient cistern and ventricular dilatation are reliable neuroradiological signs of intracranial hypertension.
By acute development of intracranial hypertension, the symptoms of the patient are rather those of encephalic displacement and herniation.
The displacement symptoms are probably due tofocal ischemia by distortion of the higher brainstem perforating arteries, whichcan be followed by irreversible infarction or hemorrhage in their vascular areas, before the blood flow is compromised by the elevated ICP. Surgery may resolve displacement and herniation. 1f it is not indicated or is delayed, medical treatment based on the control of ICP, frequently fails, because it cannot revert the blockade. The "rebound effect" would mean persistence of herniation. Transient releaf of ICP does not necessarilymean, improvement in the condition of the patient.
The deleterious effect of elevated ICP is due to diminution of CBF and eventual cerebral circulatory arrest in advanced and possibly irreversible steps of the process.
The 1CP monitoring in the severely brain injured patient is usefulfor the diagnosis of brain herniation, the control of medical therapy andfor the indication of surgery in doubtful cases, Lesions that curse with diffuse cerebral edema and swelling will produce ICP elevation only if they cause brain herniation. As in most of those patients horizontal displacement is minor or nil, and edema and swelling are the principal ethiologic factors, medical treatment has the better prospect, if it can revert the tentorial blockade.
An adequate fisiopathological view of the intracranial events after a severe closed head injury, must systematically include volume accommodation and brain displacement to be a guide to a coherent therapy.
Key words: Increased intracranial pressure, Head trauma, Brain herniation
INTRODUCCION
Entre los adelantos incorporados al manejo del traumatismo encéfalocraneano grave (TEC), se encuentran el monitoreo de la presión intracraneana (PIC) y el tratamiento agresivo de la hipertensión endocraneana (HIC). Al promediar la década, nos encontramos manejando a nuestros pacientes mediante el recurso casi automático de tratar la hipertensión endocraneana sin profundizar el verdadero alcance y eventuales riesgos de las maniobras que realizamos y con un horizonte terapéutico limitado.
Intentamos un análisis fisiopatológico del proceso de HIC aguda y sus consecuencias para el manejo del neurotraumatizado grave en base a una revisión bibliográfica selectiva, como un pequeño aporte a la valoración de estas armas diagnósticas y terapéuticas y su mejor utilización. Las citas serán las mínimas necesarias y las más básicas, para sostener nuestras tesis, ya que se trata de una revisión crítica.
EXPOSICION
Hernia cerebral y PIC
Datos experimentales y clínicos6 han demostrado que se produce aumento de la presión intracraneana sostenido en el tiempo, sólo cuando se pierde la capacidad de desagotar de la cavidad craneana, una cantidad de LCR igual al aumento de volumen de la lesión expansiva.
Esta situación se da, cuando existe un bloqueo a la circulación de LCR ya sea éste no tumoral, como en las hidrocefalias, o tumoral, pudiendo la masa, en este caso, ocupar una posición estratégica en la vía de LCR, como en las hidrocefalias tumorales, o actuar a distancia, como en las masas supratentoriales, a través de un mecanismo de desplazamiento y hernia, que es posiblemente la causa más común de HIC. Esta aseveración se comprueba en el gráfico de Lofgren y Zwetnow15 de 1973, en donde a la curva presión volumen supratentorial, se le superpone la infratentorial, en un experimento de masa supratentorial (Gráfíco 1). El punto de divergencia de las curvas, corresponde a una falta de transmisión de la presión supratentorial a la cisterna magna, debida a la hernia tentorial.

Gráfico 1. Curvas de presión supratentorial (A) e infratentorial (B), durante un experimento de masa supratentorial. Reproducción muy levemente modificada de Lofgren y Zwetnow15, 1973
Una vez producido el bloqueo por cualquiera de los mecanismos mencionados, el LCR no sólo no puede ser desplazado fuera del cráneo para compensar el aumento de volumen de la masa, sino que comienza a acumularse, dando origen a una hidrocefalia31, que acentúa la hipertensión endocraneana. Esta hidrocefalia puede ser más o menos manifiesta de acuerdo con el momento evolutivo en que se estudie al paciente (tiempo transcurrido desde el momento del bloqueo), con la causa del proceso de HIC (tipo de lesión y velocidad de crecimiento de la masa) y con el tamaño del espacio subaracnoideo más allá del bloqueo (cuanto mayor sea este espacio, mayor será el lugar para que el ventrículo se dilate a presión constante).
Hernia (ocupación de la cisterna ambiens) primero, y dilatación mono, bi tri o tetraventricular después, son signos neurorradiológicos seguros de HIC10. La figura 1 muestra ejemplos de lo dicho.
En el momento de la hernia, los valores de PIC pueden ser normales, intermedios o altos18 (Tabla 1) dependiendo básicamente esta diferencia, de la velocidad de crecimiento de la masa36 y también, probablemente, del tamaño del espacio subaracnoideo. De todas maneras, posiblemente siempre, cambios conducentes a la hernia preceden al ascenso sostenido de la PIC37.

Fig. 1. Ejemplos de lesiones expansivas traumáticas con HIC. A. Hematoma extradural. B, Hematoma subdural subagudo. En ambos casos se observa dilatación monoventricular contralateral.
Tabla 1. PIC al momento de detectarse la aparición de la pupila oval. Pacientes con TEC grave.

Los síntomas, durante el desarrollo de este proceso, varían de acuerdo con el tiempo requerido para producir los cambios patológicos. Si éstos se desarrollan en forma rápida, prevalecen los síntomas del desplazamiento y hernia, mientras que si se instalan en forma lenta, aparecen los de HIC, aunque ésta existe en ambos casos.
La explicación más plausible de esta diferencia es la aparición de isquemias focales a nivel del tronco cerebral en el paciente agudo, que producen coma en etapas tempranas del proceso, cuando las cifras de PIC todavía no comprometen la presión de perfusión enforma difusa. Este fenómeno podría ser producido por la distorsión26 brusca de los vasos perforantes del tronco alto determinada principalmente por el desplazamiento horizontal, en el mismo instante en que comienza a desencadenarse el proceso de HIC por la hernia concomitante. Este mecanismo ha sido magistralmente descripto por Dott3 en su conferencia "Cerebro, tiempo y movimiento", bellamente demostrado en el trabajo experimental de Nagao y colaboradores24 y observado anatomopatológicamente en pacientes con TEC por Graham y colaboradores en 1978 y nuevamente8 en 1989 (Tabla 2).
Tabla 2. Lesiones isquémicas en dos grupos de pacientes fallecidos por TEC

La tolerancia encefálica a ésta isquemia por distorsión brusca, es mala, por lo que rápidamente pueden producirse infartos del tronco cerebral o hemorragias, que llevan al coma prolongado o a la muerte y que no pueden ser modificados sustancial mente por ningún tratamiento médico de la HIC si la cirugía (que actúa sobre el desplazamiento) ya ha sido realizada, fue tardía (Fig. 2), o no está indicada. Para nosotros, ésta es una de las bases físiopatológicas de la explicación del frecuente fracaso de las terapéuticas médicas de los cuadros de HIC aguda4, basados en el monitoreo de la PIC, y la mejor performance de los mismos, cuando no existe un proceso de desplazamiento horizontal23 y por otro lado, la mejoría de los resultados recientes con el tratamiento quirúrgico agresivo de las lesiones expansivas antes de que aparezcan los signos clínicos de desplazamiento y hernia14, 20.
Quisiéramos hacer notar que, al parecer, algunas de estas isquemias centrales pueden ser detectadas por la TC, si el paciente no fallece precozmente y se puede repetir el estudio. Debemos tener en cuenta que algunas de ellas pueden producirse en el mismo momento del accidente y se trataría en este caso, de una lesión primaria y no secundaria1, 3. Una zona frecuentemente afectada, es la rodilla de la cápsula interna y polo anterior del tálamo (ver Tabla 2 y Fig. 3). La figura 4 muestra el perfil angiográfico de un paciente con hematoma subdural agudo. La arteria comunicante posterior se encuentra arqueada sobre la clinoides posterior y distorsionada por el enclavamiento. De este vaso, nacen las aa. tálamo perforantes anteriores, que irrigan el polo anterior del tálamo13.
La aparición del bloqueo, modifica la respuesta del sistema intracraneano al aumento de volumen. Mientras que inicialmente se trata de un sistema elástico, con compliance alta y elastancia baja, luego del bloqueo se transforma en un sistema rígido, con elastancia alta y compliance baja (Gráfico 2)2,22, 27.

Fig 2. Probable caso de cirugía tardía. El pacientefue estudiado y operado luego de su descompensación clínica. A pesar de la evacuación del hematoma, el cuado de HIC no cede por aparición de edema hemisférico, que mantiene el desplazamiento y hernia. Obsérvese hidrocefalia contralateral en ambos momentos.

Fig. 3. Lesiones isquémicas profundas detectadas por TC en pacientes con TEC grave. A, Hematoma subdural agudo operado, B. Hematoma subdural subagudo.

Fig. 4. Anfiografia en paciente con hematoma subdural agudo. En el perfil se observa distorsión de la arteria comunicante posterior sobre la apófisis clinoides posterior. De este vaso, nace las arterias que nutren las porciones anteriores del tálamo,
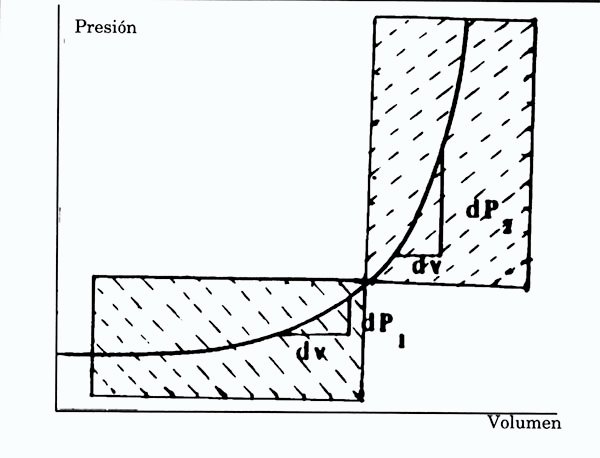
Gráfico 2. La curva presión-volumen con sus dos sectores: horizontal o de elastancia baja y vertical o de elastancia alta. El "punto de fractura" corresponde al bloqueo tentorial. En el sector vertical, pequeñas extracciones de volumen pueden tener éxito en el descenso tensional, pero el "rebote" será fácil y frecuente, cuando volúmenes similares sean recuperados por edema o acumulación de LCR. La disminución de la elastancia, si se consigue, permite acomodar volúmenes algo mayores, pero no resuelve etiológicamente la situación
En este estado, toda disminución de volumen del contenido intracraneano por encima del bloqueo, como se obtiene mediante el drenaje de LCR, utilización de diuréticos osmóticos o manejo del volumen sanguíneo encefálico mediante la hiperventilación o los barbitúricos, producirá un descenso de la PIC, pero más difícilmente de la elastancia, y estará sujeto a un fenómeno de rebote, cuando los volúmenes retirados sean reemplazados por la constante producción de LCR, que no circula, o edema, a partir de la lesión primaria, y, más importante desde el punto de vista del resultado, pocas veces podrá revertir el bloqueo, causante de la cascada fisiopatológica. La presencia de rebote de la PIC, significa persistencia del bloqueo o recidiva de éste.
La peor maniobra según nuestro razonamiento, es el drenaje de LCR para bajar los valores de PIC, en un paciente con sistema ventricular desplazado, ya que si bien se obtiene un descenso transitorio de aquéllos, se favorece el desplazamiento encefálico, al acentuar el gradiente tensional entre los comportamientos supratentoriales. El descenso transitorio de los valores de PIC no significa necesariamente una mejoría en la situación del enfermo.
PIC y perfusión cerebral
El efecto de la hipertensión endocraneana es una disminución de la presión de perfusión de acuerdo a la fórmula:
PP = PAM - PV + PIC
PP: presión de perfusión; PAM: presión arterial media; PV: presión venosa
que puede comprometer el flujo sanguíneo cerebral. Se acepta que esto sucede, cuando la presión de perfusión cae por debajo de 40 mmHg16. Trabajos experimentales11 y clínicos12, 16 han demostrado que en etapas iniciales del proceso, con elevaciones modestas a moderadas de la PIC, el flujo no sólo no desciende, sino que puede aumentar11. dependiendo este comportamiento del método utilizado para elevar la PIC y de otras condiciones experimentales. De acuerdo con esta interpretación fisiopatológica, no todas las hiperemias asociadas a HIC en el TEC grave, serán consecuencia directa de la lesión primaria y causa de hipertensión endocraneana, sino consecuencia de la misma. Así vista, esta hiperemia inicial, corresponde a la respuesta autorreguladora de presión12, reflejo que se produce por caída de la presión transmural a nivel de los vasos de resistencia y significa un primer nivel de desacople metabólico,
La congestión por vasoparálisis, que puede encontrarse en los focos lesionales, debida posiblemente a efecto directo del traumatismo, o en etapas fínales del proceso de HIC, se diferencia de la anterior, en que en este caso, los vasos han perdido su respuesta refleja a la pCO2 y no se contraen con la hiperventilación (segundo nivel de desacople metabólico).
Con elevaciones más acentuadas de la PIC, el flujo sanguíneo cerebral cae, produciéndose isquemia difusa, y una eventual detención circulatoria intracraneana, causa de muerte encefálica. Según la Tabla 2, este tipo de isquemia, se observa en la necropsia solamente en menos del 28 al 42% de los pacientes fallecidos por TEC y que tenían HIC8.
Posiblemente, cuando la HIC actúa favorecida por otros factores, pueden aparecer isquemias focales o facilitarse la isquemia difusa.
La asociación de HIC e hipotensión, podría producir una disminución relativa de la PP que favorezca las isquemias de última pradera, apareciendo lesiones en los límites de los territorios arteriales8. Según la Tabla 2, estas lesiones se dan en menos del 25 al 13% de los pacientes fallecidos con TEC e HIC.
La falla autorregulatoria en los focos lesionales, podría favorecer la isquemia en los mismos, con valores de PIC que no comprometen el flujo global. No disponemos, por el momento, de un método diagnóstico y terapéutico práctico para acceder al control de este tipo de alteraciones focales del flujo, que podrían acentuarse con algunas de las maniobras para descender la PIC12.
La PIC como factor causal
Hay consenso en que los datos estadísticos asignan un carácter de mal pronóstico a la presencia de hipertensión endocraneana en el paciente con TEC grave4, 21,23
La asociación estadística altamente significativa entre dos variables, no autoriza a concluir sin más, una relación de causalidad entre ellas17. Para poder establecer este tipo de relación, además de la asociación, la desaparición de una, (PIC elevada) debe hacer desaparecer a la otra (fallecimiento) en forma sistemática, cosa que no siempre sucede. Sin embargo, últimamente la literatura, le asigna este carácter productivo a la HIC, como P. ej. Marmarou y colaboradores, cuando aseveran que "la elevación sostenida de la PIC puede tener efectos directos sobre el tejido neural, aunque exista adecuada perfusión"21.
Muchas veces, las variables están asociadas estadísticamente a través de una tercera que las explica a ambas y es el verdadero factor causal17 (lesión primaria más desplazamiento y hernia en nuestro caso). De hecho, la presencia de hernia (falta de visualización de las cisternas en TC) tiene un valor predictivo similar al de la PIC elevada en el TEC grave33, 34.
No encontramos apoyo en la literatura, ni nos parece razonable, que la hipertensión endocraneana pueda actuar como factor etiológico, si no es comprometiendo la circulación cerebral por el descenso de la presión de perfusión, más allá de la capacidad de autorregulación, en etapas avanzadas e irreversibles del proceso. Estas son las razones, según nuestra opinión, por las cuales la disminución de la presión de perfusión no fue tan buen predictor de resultado, como la PIC elevada (signo de hernia), en el mencionado trabajo de Marmarou y colaboradores21, llevándolos a postular otros hipotéticos efectos de la HIC.
Opinamos que el concepto de presión de perfusión tiene mucho más valor clínico cuando es relativo, por descenso de la TA sistémica de causa extraneurológica en presencia de HIC, que en los casos en que desciende exclusivamente por HIC, ya que en éstos, cuando se llega a amenazar la perfusión, según nuestro razonamiento, suele quedar muy poco por hacer.
Presión intracraneana o presiones intracraneanas?
El hecho de que la hipertensión endocraneana sostenida sea la consecuencia de un proceso de desplazamiento y hernia, nos habla de la existencia de gradientes de presión, según los cuales, el encéfalo se desplaza. Esto genera enseguida, el concepto asociado al de HIC, que es el de lesión focal, proceso a partir del cual se producirán presiones tisulares mayores que las de las áreas vecinas, que pueden ser causa de isquemia secundaria focal, y que podrán o no generar un proceso de hipertensión endocraneana.
Así pues, la PIC que se mide, es la resultante de una serie de diferentes presiones tisulares, del LCR y de la sangre en distintas zonas del endocráneo, que puede no representar adecuadamente a algunas de ellas, ya sea en defecto25, 12 o en exceso.
Es un fenómeno global, consecuencia de fenómenos locales, que quedan oscurecidos, en segundo plano, cuando el diagnóstico y la terapia se concentran en la HIC.
Con el monitoreo de éste como de otros parámetros globales (como la saturación de oxigeno yugular o el flujo sanguíneo global), podemos pues, estar obviando procesos tremendamente importantes desde el punto de vista fisiopatológico, que suceden en las áreas de lesión primaria.
Lo mismo puede aplicarse a los criterios terapéuticos. No se puede negar que los diuréticos osmóticos y la hiperventilación, que son la base de la terapia médica de la HIC, actúan sobre las áreas menos afectadas por el traumatismo y en las zonas sanas29, en donde la integridad de la barrera hematoencefálica permite el efecto osmótico y, la preservación de la regulación química, la vasoconstricción de la hipocapnia. Los focos lesionales, podrían afectarse aún más o acentuarse los gradientes tensionales, en algún paciente, como consecuencia de estas medidas terapéuticas, sin que tengamos por el momento, un acceso sencillo para el control de estos efectos indeseados de las mismas.
Utilidad del monitoreo de la PIC
Toutant y colaboradores decían en 1984, "parece que los regímenes terapéuticos actuales no son adecuados para producir una sobrevida útil en la gran mayoría de pacientes en los cuales las cisternas basales están ausentes en la primer TC" (el subrayado es nuestro), y hacían un reclamo para que se comenzara un régimen de terapia más temprana33.
Para Ropper28 el "límite en el cual PIC y edema cerebral se hacen intratables" corresponde a una PIC de 25 mm de Hg. Esta cifra está por debajo de los valores que suelen comprometer la perfusión, pero representa un valor próximo a la PIC media de un grupo de pacientes agudos recientemente enclavados18 (ver Tabla 1).
Es nuestra opinión que la posible mejora producida en el manejo del TEC grave en nuestros días, se debe más bien ala incorporación de la TC, del tratamiento quirúrgico precoz y de los cuidados del neurointensivismo, que al control de la PIC, como parecen insinuarlo algunos trabajos que describimos a continuación.
Stuart32 presenta en 1983, una mortalidad de 34% en pacientes con TEC grave, sin monitoreo de la PIC, cifra comparable a las actuales, mas allá de críticas por posibles sesgos estadísticos.
El grupo de pacientes de Eisenberg y colaboradores4 tratado con barbitúricos y en el que la PIC fue eficientemente descendida por este método, no mostraron mejoría de los resultados, respecto del tratamiento convencional (Tabla 2).
Tampoco resultó efectivo el tratamiento preventivo con barbitúricos de un grupo de pacientes con TEC grave35.
Sin embargo, es dificil encontrar en la actualidad un Servicio de Neurocirugía en donde no se controle la PIC como parte del manejo del paciente con TEC grave. Si este parámetro se observa como un síntoma más del cuadro que se está tratando, que se modifíca de acuerdo con la respuesta que el paciente tiene al tratamiento, un epifenómeno, su registro es útil, especialmente en el postoperatorio del HSD agudo y de la contusión cerebral y en la lesión encefálica difusa.
El monitoreo de la PIC en el TEC grave está indicado, de acuerdo con nuestro razonamiento, para:
1) Diagnóstico de la hernia encefálica: puesto que el aumento de PIC se debe a la misma, todo valor de PIC mayor que las cifras límite superior de la PVC (presión venosa central= 0- 10 mm Hg), especialmente si se aleja de la PVC actual del paciente, nos deben hacer pensar en este diagnóstico, si no tenemos un estudio neurorradiológico previo que lo demuestre.
Debemos agradecer a las investigaciones clínicas generadas en parte por el monitoreo sistemático de la PIC, el concepto de precocidad de la aplicación del armamentario terapéutico en el manejo del TEC grave, lo cual ha sido poco felizmente califícado como agresivo. El modelo propuesto por Saul y Ducker30 en 1982, debe ser tenido especialmente en cuenta en este sentido. Ellos sugieren comenzar el tratamiento agresivo con valores de PIC superiores a 15 mm de Hg.
2) Objetivo de la terapia: la terapia no debe estar dirigida al control de la PIC, que es un síntoma, sino que debe ser lo más etiológica posible, siendo los valores de PIC una guía acerca del resultado que estamos teniendo con la misma. Entre otras cosas, éste es un llamado a que desde este punto de vista, generemos terapias distintas de las actuales, lo cual requerirá una mejor comprensión de los procesos que se desarrollan a nivel de la lesión primaria. Tengamos en cuenta que el tratamiento actual de la hipertensión endocraneana está en realidad dirigido básicamente contra la hinchazón cerebral en sus vertientes de edema y congestión.
Un descenso de los valores de PIC sostenido en el tiempo (es decir sin rebote) puede indicar que el tratamiento es efectivo, ya que significaría una reversión de la hernia encefálica.
Si no se han generado daños secundarios por desplazamiento y hernia, y la lesión primaria lo permite, la mejoría sostenida de la PIC debería acompañarse de mejoría clínica.
3) Indicación de cirugía en casos dudosos en que inicialmente se decidió terapéutica médica: puesto que se trata de procesos mecánicos, la terapéutica quirúrgica puede ser reconsiderada en algunos casos en que inicialmente se desechó, sobre todo si existe desplazamiento y la terapia médica no da resultado (focos considerados no quirúrgicos inicialmente, lesión difusa IV).
Edema cerebral e hipertensión endocraneana
Agradecemos a los editores la sugerencia de incluir este ítem en la elaboración del tema que nos ocupa.
Con edema cerebral queremos denotar aquí, el aumento de tamaño de uno o preferentemente ambos hemisferios de causa traumática sin o con escasa lesión demostrable radiológicamente, sin entrar en diferenciaciones académicas sobre si es debido a un aumento de la cantidad de líquido tisular cualquiera sea su tipo, o a un aumento del volumen sanguíneo (congestión), o a ambos. Lo que nos importa pues, es lo que radiológicamente denominamos efecto de masa sin lesión, que se manifiesta en la tomografía por colapso de los espacios subaracnoideos, disminución del tamaño ventricular y, de ser unilateral, desplazamiento de la línea media9.
Es común la acepción que si existe edema, debe existir hipertensión endocraneana, sobre todo, en casos de edema difuso. No ha sido éste, el resultado de investigaciones directamente dirigidas a determinar por la observación de la tomografía computada, si un paciente presenta hipertensión endocraneana, Haar10 y colaboradores observaron que los signos tomográficos de edema, eran malos predictores de HIC y esta observación ha sido repetida por otros.
La mejor evolución y menor incidencia de HIC en las lesiones difusas Tipo I y II de la clasificación tomográfica de Marshall19 de los TCE coincide con el concepto expresado de que no siempre edema es sinónimo de HEC.
Un paciente con edema cerebral difuso tendrá HIC, cuando presente hernia tentorial generadora del bloqueo necesario, de acuerdo con la interpretación físiopatológica esbozada previamente, que se manifestará tomográficamente por la no visualización de las cisternas peritroncales. En las lesiones difusas tipo III (con bloqueo cisternal), la incidencia de HIC es mayor y el pronóstico es peor19. No estamos, sin embargo, de acuerdo con la tendencia actual de calificar solamente a estos pacientes como portadores de edema, porque tratándose de un proceso dinámico, pacientes con edema sin bloqueo cisternal inicial, pueden bloquearse más tarde. Sería además, interesante tema de investigación prospectiva, si en algún caso de lesión subcortical difusa, no sea ésta la zona más afectada inicialmente por el edema, con colapso de los espacios subaracnoideos corticales, y si este bloqueo fluminal difuso pueda ser causa de HIC antes .que se produzca hernia tentorial.
La hernia generada por estos procesos, será prevalentemente de tipo central, con distorsión vertical del tronco y los vasos y lesiones secundarias de isquemia y hemorragia de predominio en la calota peduncular 1, 5. En este sentido, es de desear nuevamente, el desarrollo de la posibilidad de evaluar estos pacientes agudos por RNM, dada la capacidad de este estudio de detectar el desplazamiento axial del tronco encefálicos, con ventaja sobre la TC.
El tamaño ventricular será variable, de acuerdo al momento fisiopatológico en que sea realizado el estudio y atento a la causa en juego, como lo es en general en cualquier caso de HIC, según lo hicimos notar al principio de esta disquisición.
Antes del bloqueo, con edema difuso y sin HIC, los ventrículos serán pequeños. Inmediatamente después de la hernia y ya con HIC, los ventrículos seguirán pequeños, Notemos sin embargo, que el proceso de hidrocefalia ha comenzado, por haberse instalado el bloqueo con la hernia (hidrocefalia: acumulación de LCR en los espacios que normalmente lo contienen, comprimiendo el parénquima cerebral). En su progresiva dilatación, deberían pasar por un período de normalidad respecto a su tamaño, que podría dar un carácter de notable inocencia al estudio tomográfíco, de no tenerse en cuenta el estado de las cisternas basales. Es dificil que existiendo edema, los ventrículos puedan dilatarse más allá de un aumento modesto de su tamaño.
Es de notar que, con todos los espacios de LCR colapsados antes del bloqueo, debido al tipo de proceso fisiopatológico, la rigidez del sistema debería ser máxima en estos casos, con aumentos inmediatos y extremos de la PIC. Salvando las diferencias y, a manera de ejemplo, la situación tiene cierta similitud con la disfunción valvular aguda en paciente válvulo dependiente con ventrículo pequeño.
Como dijimos antes, al no existir desplazamiento horizontal o ser éste menor, y por el tipo de alteración, en que el edema juega un papel etiológico importante, son éstos los pacientes que más pueden benefíciarse del tratamiento médico de la HIC y del drenaje de LCR. Su fracaso estará dado por la gravedad de la lesión primaria, la incapacidad para revertir la hernia a tiempo, generándose así lesiones irreversibles del tronco alto, o por persistencia definitiva de ésta, produciéndose la muerte encefálica por HIC no tratable.
DISCUSION
Hemos presentado los hechos repitiendo conceptos que por obvios suelen ser dejados de lado por los trabajos más recientes pero que pueden ser útiles para recordarnos la base teórica de los desarrollos actuales, especialmente a los más jóvenes, que no han vivido la evolución de estas ideas, y permitirnos un análisis critico de las mismas.
La práctica de la medicina nos enseña que la aplicación dogmática de protocolos terapéuticos de cualquier tipo, si bien permite la estandarización y comparación de procedimientos, no puede ser usada en forma indiscriminada, encontrándose muy pronto, amplios grupos de pacientes en los cuales el protocolo no puede ser utilizado parcial o completamente, por lo que se impone una adaptación de la terapéutica al paciente, guiada por el juicio clínico, que se apoya en un conocimiento profundo de la fisiopatología y en la interpretación acertada de los matices que la enfermedad presenta en cada individuo.
El problema del tratamiento del neurotraumatizado grave parece irse circunscribiendo para los próximos años, a la prevención de la lesión secundaria por isquemia. Nos parece muy importante establecer claramente desde el inicio si lo que se desea prevenir es la isquemia focal o la difusa, porque los sistemas de monitoreo actuales nos permiten un abordaje de esta última, pero más dificilmente de la primera, sobre todo cuando es profunda, y por otro lado, los métodos terapéuticos suelen estar dirigidos a la primera, sin tener en cuenta que pueden agravar seriamente la segunda, dejándonos la tranquilidad espiritual de que "hemos combatido la hipertensión endocraneana".
La esperanza cifrada en el posible efecto protector de los barbitúricos, en esta patología, todavía no ha sido comprobada en la clínica, más allá de la impresión de cada neurointensivista y presenta una serie de riesgos nada despreciables35.
CONCLUSIONES
Los fenómenos intracraneanos que se producen luego de un traumatismo craneoencefálico cerrado grave, pueden ser comprendidos desde dos puntos de vista complementarios. Uno, el de la acomodación de volumen, que es el enfoque de la PIC. Otro, que llamaríamos dinámico, es el de los desplazamientos encefálicos. Uno y otro tienen implicancias causales y están complejamente imbricados en el resultado sintomatológico fmal en cada paciente. El juicio clínico guiado por una adecuada interpretación fisiopatológica, orientará el equipo tratante en cada caso, hacia la obtención del mejor resultado posible.
Hemos tratado de demostrar que la tendencia actual es hacia la interpretación primera, lo cual tiene la ventaja de estandarizar la terapéutica médica del TEC, pero, como vimos, entraña riesgos en algunos pacientes y deja oscuridades en la interpretación de algunos hechos, mientras que la incorporación de la segunda, proveería al tratamiento de la posibilidad de adaptarlo a las características del padecimiento de cada paciente, mediante una interpretación más exhaustiva de la situación.
BIBLIOGRAFIA
1. Adams JH: The neuropathology of head injuries, En Vinken PJ, Bruyn GW (Eds): Handbook of Clinical Neurology, New York, American Elsevier, 1975, Vol 1, Part I, pp. 35-65,
2. Cohadon F: Physiologie de la pression intracranienne, Physiopathologie générale des hipertensions intracraniennes, Neurochirugie 20: 489524, I974,
3. Dott NM: Brain, movement and time, Brit Med J: 12-16, 1960,
4. Eisenberg H, Frankowski R. Contant Ch, Marshall L, Walker M y The CCNSTC: High-dose barbiturate control of elevated intracranial pressure in patients with severe head injury, J Neurosurg 69: 1523, 1988,
5. Feldmann E, Gandy SE, Becker R, Zimmerman R, 'Thaler HT, Posner JB, Plum F: MRI demonstrates descending transtentorial herniation, Neurology 36: 697-701, 1988,
6. Fontana H: Hipertensión endocraneana, Boletín del Centro Neurológico del Hospital Francés 5: 3-9, 1978,
7. Gennarelli T, Spielman G, LangfItt T, Gildenberg P, Harrington T, Jane J, Marshall L, Miller J, Pitts L: Influence of the tipe of intracranial lesion on outcome from severe head injury, J Neurosurg 56: 2632, 1982,
8. Graham D, Ford I, Hume Adams J, Doyle D, Teasdeale G, Lawrence A, McLellan D: Ischaemic brain damage is still common in fatal non missile head injury, J Neurol Neurosurg Psych 53: 346350, 1989,
9. Grossman CB: MRI and CT of the head and spine, Baltimore, Williams and Wilkins, 1990,
10. Haar F, Sadhu V, Pinto R, Gildenberg P, Sampson J: Can CT scan findings predict intracranial pressure in closed head injury patients? En: Shulman, Marmarou, Miller, Becker, Hochwald y Brock (Eds): Intracranial Pressure IV, Berlín, Springer, 1980: 48-53,
11. Johnston I, Rowan J, Harper A, Jennet W: Raised intracranial pressure and cerebral blood flow, J Neurol Neurosurg Psych 35: 285-296, 1972,
12, Langfitt T, Obrist W: Cerebral blood flow. En: Willdns R y Rengachary S (eds,): Neurosurgery. New York, McGraw-Hill Book Co,, I985, Vol 2: 1167-I173,
13. Lazhortes G: Vascularisarion et circulation cérébrales. Paris, Masson, 1961.
14. Lobato R, Rivas J, Gómez P, Castañeda M, Cañizal J, Saravia R, Cabrera A, Muñoz M: Head-injured patients who talk and deteriorate finto coma.J Neurosurg 75: 256-261, 1991,
15. Lofgren J, Zwetnow N: Cranial and spinal components of the cerebrospinal fluid pressure-volume curve, Acta Neurol Scandinav 49: 575-585, 1973.
16. Lundberg N, Kjallquist A, Kullberg G, Pontén U, Sundbarg G: Non-operative management of intracranial hypertension, Adv and Tech Stand Neurosurg Springer, Wien 1: 3-59, 1973.
17. MacMahon B, Pugh T: Principios y métodos de epidemiología. México, La Prensa Médica Mexicana, I983.
18. Marshall L, Barba D, Toole B, Bowers S: The oval pupil: clinical significance and relationship to intracranial hypertension. J
Neurosurg 58: 566568, 1983,
19. Marshall LF, Marshall SB, Klauber MR, van Berkum Clark M, Eisenberg HM, Jane JA, Luerssen TG, Marmarou A, Foulkes MA: A new classiflcation of head injury based on computarized tomography, J Neurosurg 75: S14-S20, I991,
20. Marshall L, Toole B. Bowers S: The National Traumatic Coma Data Bank, Part 2: patients who talk and deteriorate: implications for treatement. J Neurosurg 59: 285-288, 1983.
21. Marmarou A, Anderson R, Ward J, Chou S, Young H, Eisenberg H, Foulkes M, Marshall L, Jane J: Impact of ICP instability and hypotension on out-come in patients with severe head trauma. J Neurosurg 75: 959-966, 1991,
22. Miller J: Volume and pressure in the craniospinal axis, Clin Neurosurg 22: 321-331, 1974,
23. Miller J, Butterworth J. Gudeman S, Faulkner J, Choi S, Selhorst J, Harbison J, Lutz H, Young H, Becker D: Further experience in the management of severe head injury, J Neurosurg 54: 289-299, 1981.
24. Nagao S, Sunami N, Tsutsui T, Honma Y, Momma F, Nishiura T, Nishimoto A: Acute intracranial hypertension and brain-stem blood flow, J Neurosurg 60: 566-571, 1984,
25. Pitts LH: Brain trauma and ischemia, En: Protection of the brain from ischemia, Weinstein PR, Faden Al, Eds, Baltimore, I990.
Williams & Wilkins, Pp, 171-181,
26. Ropper A: A preliminary MRI study of the geometry of brain displacement and level of conciousness with acute intracranial masses, Neurology 39: 622-627, 1989,
27. Ropper A: Coma and acute raised intracranial pressure. En Asbury, McKhann y McDonald (Eds.). Diseases fo the nervous system. Clinical Neurobiology. 2a. Ed, Philadelphia, Saunders. Vol II, I992: 978-988,
28. Ropper A: In favor of intracranial pressure monitoring and agressive therapy in neurologic practice. Arch Neurol 42: 1194-1195, 1985.
29. Ropper AH: Treatment of intracranial hypertension. En: Neurological and neurosurgical intensive care. Ropper AH Ed. New York, 1993, Rayen press: 29-52,
30. Saul T, Ducker T: Effect of intracranial pressure monitoring and aggressive treatment on mortality in severe head injury, J Neurosurg 56: 498-503, 1982.
31. Stovring J: Descending tentorial herniation: findings on computed tomography, Neuroradiology 14: 101-105, 1977.
32. Stuart G, Marry G, Smith J, Yelland J: Severe head injury managed without intracranial pressure monitoring, J Neurosurg 59: 601-605, 1983,
33. Toutant S, Klauber M, Marshall L, Toole B, Bowers S, SeelingJ, Varnell J: Absent or compressed basal cisterns on first CT scan: ominous predictors of outcome in severe head injury, J Neurosurg 61: 691-694, 1984,
34. van Dongen K, Braakman R, Gelpke G: The prognostic value of computarized tomography in coma-tose head-injuried patients, J Neurosurg 62: 383388, 1983.
35. Ward J, Becker D, Miller D, Choi S, Marmarou A, Wood Ch, Newlon P, Keenan R: Failure of prophylactic barbiturate coma in the treatment of severe head injury, J Neurosurg 62: 383-388, 1985,
36. Weinstein J, Langfitt T, Bruno L, Zaren H, Jackson J: Experimental study of patterns of brain distortion and ischemia produced by an intracranial mass, J Neurosurg 28: 513-522, 1968,
37. Yoneda S, Matsuda M, Handa H, Gotoh H, Tsuda E: Dynamics of transtentorial herniation. En: Shulman, Marmarou, Miller,
Becker, Hochwald y Brock (Eds.): Intracranial Pressure IV. Berlin, Springer, 1980: 106-110,
Actualización
Hipertensión Endocraneana y Traumatismo Encefalo Craneano. Revisión Conceptual
H. Fontana, H, Belziti
Servicio de Nurocirugía del Hospital de San Isidro, Provincia de Buenos Aires
Correspondencia: Dr. H. Fontana, Arrotea 746, Depto A (I406) Buenos Aires
RESUMEN
Aparece hipertensión endocraneana cuando hay un bloqueo a la circulación de LCR. Este se produce por ubicación estratégica de la masa respecto a las vías de LCR, o por desplazamiento y hernia encefálicos,
Los signos neurorradiológicos de hipertensión endocraneana (ocupación de la cisterna ambiens y dilatación ventricular) son fiables.
Cuando los acontecimientos se desarrollan en forma aguda, los síntomas del paciente son más bien del desplazamiento y hernia encefálicos, que de hipertensión endocraneana. Los síntomas del desplazamiento se deben probablemente a isquemia focal del tronco cerebral por distorsión de los vasos perforantes del tronco alto. Esta puede producir infartos o hemorragias que generen estado vegetativo persistente, o sean causa de muerte, antes que la HIC comprometa el flujo en forma difusa.
La cirugía corrige el desplazamiento y hernia encefálicos. Si no está indicada o es tardía, las terapéuticas médicas basadas en el control de la PIC, muchas veces no pueden revertir la hernia, y por ello, también pueden fallar en el control de la hipertensión endocraneana. La presencia de "rebote" significaría persistencia o recidiva del bloqueo. El descenso transitorio de los valores de PIC no significa necesariamente una mejoría de la situación del paciente.
El efecto deletéreo de la HIC se produce por disminución del flujo cerebral y eventual detención circulatoria, en etapas avanzadas y posiblemente irreversibles del proceso.
El registro de la PIC como el de otros parámetros globales, pasa por alto una serie importante de sucesos focales relacionadas con ella (presiones tisulares en los focas lesionales) que son de gran importancia flsiopatológica y terapéutica.
El monitoreo de la PIC en el tratamiento del TEC grave es útil para el diagnóstico de la hernia encefálica, el control del resultado de la terapéutica y en la indicación quirúrgica en casos dudosos. Las lesiones que producen edema cerebral difuso, generarán hipertensión endocraneana sólo si ocasionan bloqueo. Al no haber desplazamiento horizontal y ser el edema un actor etiológico en estos casos, el tratamiento médico tiene mejores perspectivas, si alcanza a revertir el bloqueo a tiempo.
Una interpretación fisiopatológica adecuada de los sucesos intracraneanos luego de unTEC cerrado, debe incluir sistemáticamente la acomodación de volumen y el desplazamiento y hernia encefálicos, para guiar una terapia coherente.
Palabras clave: hipertensión endocraneeana, traumatismo craneoencefálico, hernia encefálica
ABSTRACT
Sustained intracranial hypertension is due to a blockade to the circulation of CSF, produced by a strategic location of the mass in respect to the ventricular system, or hrough encephalic displacement and hemiation.
Occupation of the ambient cistern and ventricular dilatation are reliable neuroradiological signs of intracranial hypertension.
By acute development of intracranial hypertension, the symptoms of the patient are rather those of encephalic displacement and herniation.
The displacement symptoms are probably due tofocal ischemia by distortion of the higher brainstem perforating arteries, whichcan be followed by irreversible infarction or hemorrhage in their vascular areas, before the blood flow is compromised by the elevated ICP. Surgery may resolve displacement and herniation. 1f it is not indicated or is delayed, medical treatment based on the control of ICP, frequently fails, because it cannot revert the blockade. The "rebound effect" would mean persistence of herniation. Transient releaf of ICP does not necessarilymean, improvement in the condition of the patient.
The deleterious effect of elevated ICP is due to diminution of CBF and eventual cerebral circulatory arrest in advanced and possibly irreversible steps of the process.
The 1CP monitoring in the severely brain injured patient is usefulfor the diagnosis of brain herniation, the control of medical therapy andfor the indication of surgery in doubtful cases, Lesions that curse with diffuse cerebral edema and swelling will produce ICP elevation only if they cause brain herniation. As in most of those patients horizontal displacement is minor or nil, and edema and swelling are the principal ethiologic factors, medical treatment has the better prospect, if it can revert the tentorial blockade.
An adequate fisiopathological view of the intracranial events after a severe closed head injury, must systematically include volume accommodation and brain displacement to be a guide to a coherent therapy.
Key words: Increased intracranial pressure, Head trauma, Brain herniation
INTRODUCCION
Entre los adelantos incorporados al manejo del traumatismo encéfalocraneano grave (TEC), se encuentran el monitoreo de la presión intracraneana (PIC) y el tratamiento agresivo de la hipertensión endocraneana (HIC). Al promediar la década, nos encontramos manejando a nuestros pacientes mediante el recurso casi automático de tratar la hipertensión endocraneana sin profundizar el verdadero alcance y eventuales riesgos de las maniobras que realizamos y con un horizonte terapéutico limitado.
Intentamos un análisis fisiopatológico del proceso de HIC aguda y sus consecuencias para el manejo del neurotraumatizado grave en base a una revisión bibliográfica selectiva, como un pequeño aporte a la valoración de estas armas diagnósticas y terapéuticas y su mejor utilización. Las citas serán las mínimas necesarias y las más básicas, para sostener nuestras tesis, ya que se trata de una revisión crítica.
EXPOSICION
Hernia cerebral y PIC
Datos experimentales y clínicos6 han demostrado que se produce aumento de la presión intracraneana sostenido en el tiempo, sólo cuando se pierde la capacidad de desagotar de la cavidad craneana, una cantidad de LCR igual al aumento de volumen de la lesión expansiva.
Esta situación se da, cuando existe un bloqueo a la circulación de LCR ya sea éste no tumoral, como en las hidrocefalias, o tumoral, pudiendo la masa, en este caso, ocupar una posición estratégica en la vía de LCR, como en las hidrocefalias tumorales, o actuar a distancia, como en las masas supratentoriales, a través de un mecanismo de desplazamiento y hernia, que es posiblemente la causa más común de HIC. Esta aseveración se comprueba en el gráfico de Lofgren y Zwetnow15 de 1973, en donde a la curva presión volumen supratentorial, se le superpone la infratentorial, en un experimento de masa supratentorial (Gráfíco 1). El punto de divergencia de las curvas, corresponde a una falta de transmisión de la presión supratentorial a la cisterna magna, debida a la hernia tentorial.

Gráfico 1. Curvas de presión supratentorial (A) e infratentorial (B), durante un experimento de masa supratentorial. Reproducción muy levemente modificada de Lofgren y Zwetnow15, 1973
Una vez producido el bloqueo por cualquiera de los mecanismos mencionados, el LCR no sólo no puede ser desplazado fuera del cráneo para compensar el aumento de volumen de la masa, sino que comienza a acumularse, dando origen a una hidrocefalia31, que acentúa la hipertensión endocraneana. Esta hidrocefalia puede ser más o menos manifiesta de acuerdo con el momento evolutivo en que se estudie al paciente (tiempo transcurrido desde el momento del bloqueo), con la causa del proceso de HIC (tipo de lesión y velocidad de crecimiento de la masa) y con el tamaño del espacio subaracnoideo más allá del bloqueo (cuanto mayor sea este espacio, mayor será el lugar para que el ventrículo se dilate a presión constante).
Hernia (ocupación de la cisterna ambiens) primero, y dilatación mono, bi tri o tetraventricular después, son signos neurorradiológicos seguros de HIC10. La figura 1 muestra ejemplos de lo dicho.
En el momento de la hernia, los valores de PIC pueden ser normales, intermedios o altos18 (Tabla 1) dependiendo básicamente esta diferencia, de la velocidad de crecimiento de la masa36 y también, probablemente, del tamaño del espacio subaracnoideo. De todas maneras, posiblemente siempre, cambios conducentes a la hernia preceden al ascenso sostenido de la PIC37.

Fig. 1. Ejemplos de lesiones expansivas traumáticas con HIC. A. Hematoma extradural. B, Hematoma subdural subagudo. En ambos casos se observa dilatación monoventricular contralateral.
Tabla 1. PIC al momento de detectarse la aparición de la pupila oval. Pacientes con TEC grave.

Los síntomas, durante el desarrollo de este proceso, varían de acuerdo con el tiempo requerido para producir los cambios patológicos. Si éstos se desarrollan en forma rápida, prevalecen los síntomas del desplazamiento y hernia, mientras que si se instalan en forma lenta, aparecen los de HIC, aunque ésta existe en ambos casos.
La explicación más plausible de esta diferencia es la aparición de isquemias focales a nivel del tronco cerebral en el paciente agudo, que producen coma en etapas tempranas del proceso, cuando las cifras de PIC todavía no comprometen la presión de perfusión enforma difusa. Este fenómeno podría ser producido por la distorsión26 brusca de los vasos perforantes del tronco alto determinada principalmente por el desplazamiento horizontal, en el mismo instante en que comienza a desencadenarse el proceso de HIC por la hernia concomitante. Este mecanismo ha sido magistralmente descripto por Dott3 en su conferencia "Cerebro, tiempo y movimiento", bellamente demostrado en el trabajo experimental de Nagao y colaboradores24 y observado anatomopatológicamente en pacientes con TEC por Graham y colaboradores en 1978 y nuevamente8 en 1989 (Tabla 2).
Tabla 2. Lesiones isquémicas en dos grupos de pacientes fallecidos por TEC

La tolerancia encefálica a ésta isquemia por distorsión brusca, es mala, por lo que rápidamente pueden producirse infartos del tronco cerebral o hemorragias, que llevan al coma prolongado o a la muerte y que no pueden ser modificados sustancial mente por ningún tratamiento médico de la HIC si la cirugía (que actúa sobre el desplazamiento) ya ha sido realizada, fue tardía (Fig. 2), o no está indicada. Para nosotros, ésta es una de las bases físiopatológicas de la explicación del frecuente fracaso de las terapéuticas médicas de los cuadros de HIC aguda4, basados en el monitoreo de la PIC, y la mejor performance de los mismos, cuando no existe un proceso de desplazamiento horizontal23 y por otro lado, la mejoría de los resultados recientes con el tratamiento quirúrgico agresivo de las lesiones expansivas antes de que aparezcan los signos clínicos de desplazamiento y hernia14, 20.
Quisiéramos hacer notar que, al parecer, algunas de estas isquemias centrales pueden ser detectadas por la TC, si el paciente no fallece precozmente y se puede repetir el estudio. Debemos tener en cuenta que algunas de ellas pueden producirse en el mismo momento del accidente y se trataría en este caso, de una lesión primaria y no secundaria1, 3. Una zona frecuentemente afectada, es la rodilla de la cápsula interna y polo anterior del tálamo (ver Tabla 2 y Fig. 3). La figura 4 muestra el perfil angiográfico de un paciente con hematoma subdural agudo. La arteria comunicante posterior se encuentra arqueada sobre la clinoides posterior y distorsionada por el enclavamiento. De este vaso, nacen las aa. tálamo perforantes anteriores, que irrigan el polo anterior del tálamo13.
La aparición del bloqueo, modifica la respuesta del sistema intracraneano al aumento de volumen. Mientras que inicialmente se trata de un sistema elástico, con compliance alta y elastancia baja, luego del bloqueo se transforma en un sistema rígido, con elastancia alta y compliance baja (Gráfico 2)2,22, 27.

Fig 2. Probable caso de cirugía tardía. El pacientefue estudiado y operado luego de su descompensación clínica. A pesar de la evacuación del hematoma, el cuado de HIC no cede por aparición de edema hemisférico, que mantiene el desplazamiento y hernia. Obsérvese hidrocefalia contralateral en ambos momentos.

Fig. 3. Lesiones isquémicas profundas detectadas por TC en pacientes con TEC grave. A, Hematoma subdural agudo operado, B. Hematoma subdural subagudo.

Fig. 4. Anfiografia en paciente con hematoma subdural agudo. En el perfil se observa distorsión de la arteria comunicante posterior sobre la apófisis clinoides posterior. De este vaso, nace las arterias que nutren las porciones anteriores del tálamo,

Gráfico 2. La curva presión-volumen con sus dos sectores: horizontal o de elastancia baja y vertical o de elastancia alta. El "punto de fractura" corresponde al bloqueo tentorial. En el sector vertical, pequeñas extracciones de volumen pueden tener éxito en el descenso tensional, pero el "rebote" será fácil y frecuente, cuando volúmenes similares sean recuperados por edema o acumulación de LCR. La disminución de la elastancia, si se consigue, permite acomodar volúmenes algo mayores, pero no resuelve etiológicamente la situación
En este estado, toda disminución de volumen del contenido intracraneano por encima del bloqueo, como se obtiene mediante el drenaje de LCR, utilización de diuréticos osmóticos o manejo del volumen sanguíneo encefálico mediante la hiperventilación o los barbitúricos, producirá un descenso de la PIC, pero más difícilmente de la elastancia, y estará sujeto a un fenómeno de rebote, cuando los volúmenes retirados sean reemplazados por la constante producción de LCR, que no circula, o edema, a partir de la lesión primaria, y, más importante desde el punto de vista del resultado, pocas veces podrá revertir el bloqueo, causante de la cascada fisiopatológica. La presencia de rebote de la PIC, significa persistencia del bloqueo o recidiva de éste.
La peor maniobra según nuestro razonamiento, es el drenaje de LCR para bajar los valores de PIC, en un paciente con sistema ventricular desplazado, ya que si bien se obtiene un descenso transitorio de aquéllos, se favorece el desplazamiento encefálico, al acentuar el gradiente tensional entre los comportamientos supratentoriales. El descenso transitorio de los valores de PIC no significa necesariamente una mejoría en la situación del enfermo.
PIC y perfusión cerebral
El efecto de la hipertensión endocraneana es una disminución de la presión de perfusión de acuerdo a la fórmula:
PP = PAM - PV + PIC
PP: presión de perfusión; PAM: presión arterial media; PV: presión venosa
que puede comprometer el flujo sanguíneo cerebral. Se acepta que esto sucede, cuando la presión de perfusión cae por debajo de 40 mmHg16. Trabajos experimentales11 y clínicos12, 16 han demostrado que en etapas iniciales del proceso, con elevaciones modestas a moderadas de la PIC, el flujo no sólo no desciende, sino que puede aumentar11. dependiendo este comportamiento del método utilizado para elevar la PIC y de otras condiciones experimentales. De acuerdo con esta interpretación fisiopatológica, no todas las hiperemias asociadas a HIC en el TEC grave, serán consecuencia directa de la lesión primaria y causa de hipertensión endocraneana, sino consecuencia de la misma. Así vista, esta hiperemia inicial, corresponde a la respuesta autorreguladora de presión12, reflejo que se produce por caída de la presión transmural a nivel de los vasos de resistencia y significa un primer nivel de desacople metabólico,
La congestión por vasoparálisis, que puede encontrarse en los focos lesionales, debida posiblemente a efecto directo del traumatismo, o en etapas fínales del proceso de HIC, se diferencia de la anterior, en que en este caso, los vasos han perdido su respuesta refleja a la pCO2 y no se contraen con la hiperventilación (segundo nivel de desacople metabólico).
Con elevaciones más acentuadas de la PIC, el flujo sanguíneo cerebral cae, produciéndose isquemia difusa, y una eventual detención circulatoria intracraneana, causa de muerte encefálica. Según la Tabla 2, este tipo de isquemia, se observa en la necropsia solamente en menos del 28 al 42% de los pacientes fallecidos por TEC y que tenían HIC8.
Posiblemente, cuando la HIC actúa favorecida por otros factores, pueden aparecer isquemias focales o facilitarse la isquemia difusa.
La asociación de HIC e hipotensión, podría producir una disminución relativa de la PP que favorezca las isquemias de última pradera, apareciendo lesiones en los límites de los territorios arteriales8. Según la Tabla 2, estas lesiones se dan en menos del 25 al 13% de los pacientes fallecidos con TEC e HIC.
La falla autorregulatoria en los focos lesionales, podría favorecer la isquemia en los mismos, con valores de PIC que no comprometen el flujo global. No disponemos, por el momento, de un método diagnóstico y terapéutico práctico para acceder al control de este tipo de alteraciones focales del flujo, que podrían acentuarse con algunas de las maniobras para descender la PIC12.
La PIC como factor causal
Hay consenso en que los datos estadísticos asignan un carácter de mal pronóstico a la presencia de hipertensión endocraneana en el paciente con TEC grave4, 21,23
La asociación estadística altamente significativa entre dos variables, no autoriza a concluir sin más, una relación de causalidad entre ellas17. Para poder establecer este tipo de relación, además de la asociación, la desaparición de una, (PIC elevada) debe hacer desaparecer a la otra (fallecimiento) en forma sistemática, cosa que no siempre sucede. Sin embargo, últimamente la literatura, le asigna este carácter productivo a la HIC, como P. ej. Marmarou y colaboradores, cuando aseveran que "la elevación sostenida de la PIC puede tener efectos directos sobre el tejido neural, aunque exista adecuada perfusión"21.
Muchas veces, las variables están asociadas estadísticamente a través de una tercera que las explica a ambas y es el verdadero factor causal17 (lesión primaria más desplazamiento y hernia en nuestro caso). De hecho, la presencia de hernia (falta de visualización de las cisternas en TC) tiene un valor predictivo similar al de la PIC elevada en el TEC grave33, 34.
No encontramos apoyo en la literatura, ni nos parece razonable, que la hipertensión endocraneana pueda actuar como factor etiológico, si no es comprometiendo la circulación cerebral por el descenso de la presión de perfusión, más allá de la capacidad de autorregulación, en etapas avanzadas e irreversibles del proceso. Estas son las razones, según nuestra opinión, por las cuales la disminución de la presión de perfusión no fue tan buen predictor de resultado, como la PIC elevada (signo de hernia), en el mencionado trabajo de Marmarou y colaboradores21, llevándolos a postular otros hipotéticos efectos de la HIC.
Opinamos que el concepto de presión de perfusión tiene mucho más valor clínico cuando es relativo, por descenso de la TA sistémica de causa extraneurológica en presencia de HIC, que en los casos en que desciende exclusivamente por HIC, ya que en éstos, cuando se llega a amenazar la perfusión, según nuestro razonamiento, suele quedar muy poco por hacer.
Presión intracraneana o presiones intracraneanas?
El hecho de que la hipertensión endocraneana sostenida sea la consecuencia de un proceso de desplazamiento y hernia, nos habla de la existencia de gradientes de presión, según los cuales, el encéfalo se desplaza. Esto genera enseguida, el concepto asociado al de HIC, que es el de lesión focal, proceso a partir del cual se producirán presiones tisulares mayores que las de las áreas vecinas, que pueden ser causa de isquemia secundaria focal, y que podrán o no generar un proceso de hipertensión endocraneana.
Así pues, la PIC que se mide, es la resultante de una serie de diferentes presiones tisulares, del LCR y de la sangre en distintas zonas del endocráneo, que puede no representar adecuadamente a algunas de ellas, ya sea en defecto25, 12 o en exceso.
Es un fenómeno global, consecuencia de fenómenos locales, que quedan oscurecidos, en segundo plano, cuando el diagnóstico y la terapia se concentran en la HIC.
Con el monitoreo de éste como de otros parámetros globales (como la saturación de oxigeno yugular o el flujo sanguíneo global), podemos pues, estar obviando procesos tremendamente importantes desde el punto de vista fisiopatológico, que suceden en las áreas de lesión primaria.
Lo mismo puede aplicarse a los criterios terapéuticos. No se puede negar que los diuréticos osmóticos y la hiperventilación, que son la base de la terapia médica de la HIC, actúan sobre las áreas menos afectadas por el traumatismo y en las zonas sanas29, en donde la integridad de la barrera hematoencefálica permite el efecto osmótico y, la preservación de la regulación química, la vasoconstricción de la hipocapnia. Los focos lesionales, podrían afectarse aún más o acentuarse los gradientes tensionales, en algún paciente, como consecuencia de estas medidas terapéuticas, sin que tengamos por el momento, un acceso sencillo para el control de estos efectos indeseados de las mismas.
Utilidad del monitoreo de la PIC
Toutant y colaboradores decían en 1984, "parece que los regímenes terapéuticos actuales no son adecuados para producir una sobrevida útil en la gran mayoría de pacientes en los cuales las cisternas basales están ausentes en la primer TC" (el subrayado es nuestro), y hacían un reclamo para que se comenzara un régimen de terapia más temprana33.
Para Ropper28 el "límite en el cual PIC y edema cerebral se hacen intratables" corresponde a una PIC de 25 mm de Hg. Esta cifra está por debajo de los valores que suelen comprometer la perfusión, pero representa un valor próximo a la PIC media de un grupo de pacientes agudos recientemente enclavados18 (ver Tabla 1).
Es nuestra opinión que la posible mejora producida en el manejo del TEC grave en nuestros días, se debe más bien ala incorporación de la TC, del tratamiento quirúrgico precoz y de los cuidados del neurointensivismo, que al control de la PIC, como parecen insinuarlo algunos trabajos que describimos a continuación.
Stuart32 presenta en 1983, una mortalidad de 34% en pacientes con TEC grave, sin monitoreo de la PIC, cifra comparable a las actuales, mas allá de críticas por posibles sesgos estadísticos.
El grupo de pacientes de Eisenberg y colaboradores4 tratado con barbitúricos y en el que la PIC fue eficientemente descendida por este método, no mostraron mejoría de los resultados, respecto del tratamiento convencional (Tabla 2).
Tampoco resultó efectivo el tratamiento preventivo con barbitúricos de un grupo de pacientes con TEC grave35.
Sin embargo, es dificil encontrar en la actualidad un Servicio de Neurocirugía en donde no se controle la PIC como parte del manejo del paciente con TEC grave. Si este parámetro se observa como un síntoma más del cuadro que se está tratando, que se modifíca de acuerdo con la respuesta que el paciente tiene al tratamiento, un epifenómeno, su registro es útil, especialmente en el postoperatorio del HSD agudo y de la contusión cerebral y en la lesión encefálica difusa.
El monitoreo de la PIC en el TEC grave está indicado, de acuerdo con nuestro razonamiento, para:
1) Diagnóstico de la hernia encefálica: puesto que el aumento de PIC se debe a la misma, todo valor de PIC mayor que las cifras límite superior de la PVC (presión venosa central= 0- 10 mm Hg), especialmente si se aleja de la PVC actual del paciente, nos deben hacer pensar en este diagnóstico, si no tenemos un estudio neurorradiológico previo que lo demuestre.
Debemos agradecer a las investigaciones clínicas generadas en parte por el monitoreo sistemático de la PIC, el concepto de precocidad de la aplicación del armamentario terapéutico en el manejo del TEC grave, lo cual ha sido poco felizmente califícado como agresivo. El modelo propuesto por Saul y Ducker30 en 1982, debe ser tenido especialmente en cuenta en este sentido. Ellos sugieren comenzar el tratamiento agresivo con valores de PIC superiores a 15 mm de Hg.
2) Objetivo de la terapia: la terapia no debe estar dirigida al control de la PIC, que es un síntoma, sino que debe ser lo más etiológica posible, siendo los valores de PIC una guía acerca del resultado que estamos teniendo con la misma. Entre otras cosas, éste es un llamado a que desde este punto de vista, generemos terapias distintas de las actuales, lo cual requerirá una mejor comprensión de los procesos que se desarrollan a nivel de la lesión primaria. Tengamos en cuenta que el tratamiento actual de la hipertensión endocraneana está en realidad dirigido básicamente contra la hinchazón cerebral en sus vertientes de edema y congestión.
Un descenso de los valores de PIC sostenido en el tiempo (es decir sin rebote) puede indicar que el tratamiento es efectivo, ya que significaría una reversión de la hernia encefálica.
Si no se han generado daños secundarios por desplazamiento y hernia, y la lesión primaria lo permite, la mejoría sostenida de la PIC debería acompañarse de mejoría clínica.
3) Indicación de cirugía en casos dudosos en que inicialmente se decidió terapéutica médica: puesto que se trata de procesos mecánicos, la terapéutica quirúrgica puede ser reconsiderada en algunos casos en que inicialmente se desechó, sobre todo si existe desplazamiento y la terapia médica no da resultado (focos considerados no quirúrgicos inicialmente, lesión difusa IV).
Edema cerebral e hipertensión endocraneana
Agradecemos a los editores la sugerencia de incluir este ítem en la elaboración del tema que nos ocupa.
Con edema cerebral queremos denotar aquí, el aumento de tamaño de uno o preferentemente ambos hemisferios de causa traumática sin o con escasa lesión demostrable radiológicamente, sin entrar en diferenciaciones académicas sobre si es debido a un aumento de la cantidad de líquido tisular cualquiera sea su tipo, o a un aumento del volumen sanguíneo (congestión), o a ambos. Lo que nos importa pues, es lo que radiológicamente denominamos efecto de masa sin lesión, que se manifiesta en la tomografía por colapso de los espacios subaracnoideos, disminución del tamaño ventricular y, de ser unilateral, desplazamiento de la línea media9.
Es común la acepción que si existe edema, debe existir hipertensión endocraneana, sobre todo, en casos de edema difuso. No ha sido éste, el resultado de investigaciones directamente dirigidas a determinar por la observación de la tomografía computada, si un paciente presenta hipertensión endocraneana, Haar10 y colaboradores observaron que los signos tomográficos de edema, eran malos predictores de HIC y esta observación ha sido repetida por otros.
La mejor evolución y menor incidencia de HIC en las lesiones difusas Tipo I y II de la clasificación tomográfica de Marshall19 de los TCE coincide con el concepto expresado de que no siempre edema es sinónimo de HEC.
Un paciente con edema cerebral difuso tendrá HIC, cuando presente hernia tentorial generadora del bloqueo necesario, de acuerdo con la interpretación físiopatológica esbozada previamente, que se manifestará tomográficamente por la no visualización de las cisternas peritroncales. En las lesiones difusas tipo III (con bloqueo cisternal), la incidencia de HIC es mayor y el pronóstico es peor19. No estamos, sin embargo, de acuerdo con la tendencia actual de calificar solamente a estos pacientes como portadores de edema, porque tratándose de un proceso dinámico, pacientes con edema sin bloqueo cisternal inicial, pueden bloquearse más tarde. Sería además, interesante tema de investigación prospectiva, si en algún caso de lesión subcortical difusa, no sea ésta la zona más afectada inicialmente por el edema, con colapso de los espacios subaracnoideos corticales, y si este bloqueo fluminal difuso pueda ser causa de HIC antes .que se produzca hernia tentorial.
La hernia generada por estos procesos, será prevalentemente de tipo central, con distorsión vertical del tronco y los vasos y lesiones secundarias de isquemia y hemorragia de predominio en la calota peduncular 1, 5. En este sentido, es de desear nuevamente, el desarrollo de la posibilidad de evaluar estos pacientes agudos por RNM, dada la capacidad de este estudio de detectar el desplazamiento axial del tronco encefálicos, con ventaja sobre la TC.
El tamaño ventricular será variable, de acuerdo al momento fisiopatológico en que sea realizado el estudio y atento a la causa en juego, como lo es en general en cualquier caso de HIC, según lo hicimos notar al principio de esta disquisición.
Antes del bloqueo, con edema difuso y sin HIC, los ventrículos serán pequeños. Inmediatamente después de la hernia y ya con HIC, los ventrículos seguirán pequeños, Notemos sin embargo, que el proceso de hidrocefalia ha comenzado, por haberse instalado el bloqueo con la hernia (hidrocefalia: acumulación de LCR en los espacios que normalmente lo contienen, comprimiendo el parénquima cerebral). En su progresiva dilatación, deberían pasar por un período de normalidad respecto a su tamaño, que podría dar un carácter de notable inocencia al estudio tomográfíco, de no tenerse en cuenta el estado de las cisternas basales. Es dificil que existiendo edema, los ventrículos puedan dilatarse más allá de un aumento modesto de su tamaño.
Es de notar que, con todos los espacios de LCR colapsados antes del bloqueo, debido al tipo de proceso fisiopatológico, la rigidez del sistema debería ser máxima en estos casos, con aumentos inmediatos y extremos de la PIC. Salvando las diferencias y, a manera de ejemplo, la situación tiene cierta similitud con la disfunción valvular aguda en paciente válvulo dependiente con ventrículo pequeño.
Como dijimos antes, al no existir desplazamiento horizontal o ser éste menor, y por el tipo de alteración, en que el edema juega un papel etiológico importante, son éstos los pacientes que más pueden benefíciarse del tratamiento médico de la HIC y del drenaje de LCR. Su fracaso estará dado por la gravedad de la lesión primaria, la incapacidad para revertir la hernia a tiempo, generándose así lesiones irreversibles del tronco alto, o por persistencia definitiva de ésta, produciéndose la muerte encefálica por HIC no tratable.
DISCUSION
Hemos presentado los hechos repitiendo conceptos que por obvios suelen ser dejados de lado por los trabajos más recientes pero que pueden ser útiles para recordarnos la base teórica de los desarrollos actuales, especialmente a los más jóvenes, que no han vivido la evolución de estas ideas, y permitirnos un análisis critico de las mismas.
La práctica de la medicina nos enseña que la aplicación dogmática de protocolos terapéuticos de cualquier tipo, si bien permite la estandarización y comparación de procedimientos, no puede ser usada en forma indiscriminada, encontrándose muy pronto, amplios grupos de pacientes en los cuales el protocolo no puede ser utilizado parcial o completamente, por lo que se impone una adaptación de la terapéutica al paciente, guiada por el juicio clínico, que se apoya en un conocimiento profundo de la fisiopatología y en la interpretación acertada de los matices que la enfermedad presenta en cada individuo.
El problema del tratamiento del neurotraumatizado grave parece irse circunscribiendo para los próximos años, a la prevención de la lesión secundaria por isquemia. Nos parece muy importante establecer claramente desde el inicio si lo que se desea prevenir es la isquemia focal o la difusa, porque los sistemas de monitoreo actuales nos permiten un abordaje de esta última, pero más dificilmente de la primera, sobre todo cuando es profunda, y por otro lado, los métodos terapéuticos suelen estar dirigidos a la primera, sin tener en cuenta que pueden agravar seriamente la segunda, dejándonos la tranquilidad espiritual de que "hemos combatido la hipertensión endocraneana".
La esperanza cifrada en el posible efecto protector de los barbitúricos, en esta patología, todavía no ha sido comprobada en la clínica, más allá de la impresión de cada neurointensivista y presenta una serie de riesgos nada despreciables35.
CONCLUSIONES
Los fenómenos intracraneanos que se producen luego de un traumatismo craneoencefálico cerrado grave, pueden ser comprendidos desde dos puntos de vista complementarios. Uno, el de la acomodación de volumen, que es el enfoque de la PIC. Otro, que llamaríamos dinámico, es el de los desplazamientos encefálicos. Uno y otro tienen implicancias causales y están complejamente imbricados en el resultado sintomatológico fmal en cada paciente. El juicio clínico guiado por una adecuada interpretación fisiopatológica, orientará el equipo tratante en cada caso, hacia la obtención del mejor resultado posible.
Hemos tratado de demostrar que la tendencia actual es hacia la interpretación primera, lo cual tiene la ventaja de estandarizar la terapéutica médica del TEC, pero, como vimos, entraña riesgos en algunos pacientes y deja oscuridades en la interpretación de algunos hechos, mientras que la incorporación de la segunda, proveería al tratamiento de la posibilidad de adaptarlo a las características del padecimiento de cada paciente, mediante una interpretación más exhaustiva de la situación.
BIBLIOGRAFIA
1. Adams JH: The neuropathology of head injuries, En Vinken PJ, Bruyn GW (Eds): Handbook of Clinical Neurology, New York, American Elsevier, 1975, Vol 1, Part I, pp. 35-65,
2. Cohadon F: Physiologie de la pression intracranienne, Physiopathologie générale des hipertensions intracraniennes, Neurochirugie 20: 489524, I974,
3. Dott NM: Brain, movement and time, Brit Med J: 12-16, 1960,
4. Eisenberg H, Frankowski R. Contant Ch, Marshall L, Walker M y The CCNSTC: High-dose barbiturate control of elevated intracranial pressure in patients with severe head injury, J Neurosurg 69: 1523, 1988,
5. Feldmann E, Gandy SE, Becker R, Zimmerman R, 'Thaler HT, Posner JB, Plum F: MRI demonstrates descending transtentorial herniation, Neurology 36: 697-701, 1988,
6. Fontana H: Hipertensión endocraneana, Boletín del Centro Neurológico del Hospital Francés 5: 3-9, 1978,
7. Gennarelli T, Spielman G, LangfItt T, Gildenberg P, Harrington T, Jane J, Marshall L, Miller J, Pitts L: Influence of the tipe of intracranial lesion on outcome from severe head injury, J Neurosurg 56: 2632, 1982,
8. Graham D, Ford I, Hume Adams J, Doyle D, Teasdeale G, Lawrence A, McLellan D: Ischaemic brain damage is still common in fatal non missile head injury, J Neurol Neurosurg Psych 53: 346350, 1989,
9. Grossman CB: MRI and CT of the head and spine, Baltimore, Williams and Wilkins, 1990,
10. Haar F, Sadhu V, Pinto R, Gildenberg P, Sampson J: Can CT scan findings predict intracranial pressure in closed head injury patients? En: Shulman, Marmarou, Miller, Becker, Hochwald y Brock (Eds): Intracranial Pressure IV, Berlín, Springer, 1980: 48-53,
11. Johnston I, Rowan J, Harper A, Jennet W: Raised intracranial pressure and cerebral blood flow, J Neurol Neurosurg Psych 35: 285-296, 1972,
12, Langfitt T, Obrist W: Cerebral blood flow. En: Willdns R y Rengachary S (eds,): Neurosurgery. New York, McGraw-Hill Book Co,, I985, Vol 2: 1167-I173,
13. Lazhortes G: Vascularisarion et circulation cérébrales. Paris, Masson, 1961.
14. Lobato R, Rivas J, Gómez P, Castañeda M, Cañizal J, Saravia R, Cabrera A, Muñoz M: Head-injured patients who talk and deteriorate finto coma.J Neurosurg 75: 256-261, 1991,
15. Lofgren J, Zwetnow N: Cranial and spinal components of the cerebrospinal fluid pressure-volume curve, Acta Neurol Scandinav 49: 575-585, 1973.
16. Lundberg N, Kjallquist A, Kullberg G, Pontén U, Sundbarg G: Non-operative management of intracranial hypertension, Adv and Tech Stand Neurosurg Springer, Wien 1: 3-59, 1973.
17. MacMahon B, Pugh T: Principios y métodos de epidemiología. México, La Prensa Médica Mexicana, I983.
18. Marshall L, Barba D, Toole B, Bowers S: The oval pupil: clinical significance and relationship to intracranial hypertension. J
Neurosurg 58: 566568, 1983,
19. Marshall LF, Marshall SB, Klauber MR, van Berkum Clark M, Eisenberg HM, Jane JA, Luerssen TG, Marmarou A, Foulkes MA: A new classiflcation of head injury based on computarized tomography, J Neurosurg 75: S14-S20, I991,
20. Marshall L, Toole B. Bowers S: The National Traumatic Coma Data Bank, Part 2: patients who talk and deteriorate: implications for treatement. J Neurosurg 59: 285-288, 1983.
21. Marmarou A, Anderson R, Ward J, Chou S, Young H, Eisenberg H, Foulkes M, Marshall L, Jane J: Impact of ICP instability and hypotension on out-come in patients with severe head trauma. J Neurosurg 75: 959-966, 1991,
22. Miller J: Volume and pressure in the craniospinal axis, Clin Neurosurg 22: 321-331, 1974,
23. Miller J, Butterworth J. Gudeman S, Faulkner J, Choi S, Selhorst J, Harbison J, Lutz H, Young H, Becker D: Further experience in the management of severe head injury, J Neurosurg 54: 289-299, 1981.
24. Nagao S, Sunami N, Tsutsui T, Honma Y, Momma F, Nishiura T, Nishimoto A: Acute intracranial hypertension and brain-stem blood flow, J Neurosurg 60: 566-571, 1984,
25. Pitts LH: Brain trauma and ischemia, En: Protection of the brain from ischemia, Weinstein PR, Faden Al, Eds, Baltimore, I990.
Williams & Wilkins, Pp, 171-181,
26. Ropper A: A preliminary MRI study of the geometry of brain displacement and level of conciousness with acute intracranial masses, Neurology 39: 622-627, 1989,
27. Ropper A: Coma and acute raised intracranial pressure. En Asbury, McKhann y McDonald (Eds.). Diseases fo the nervous system. Clinical Neurobiology. 2a. Ed, Philadelphia, Saunders. Vol II, I992: 978-988,
28. Ropper A: In favor of intracranial pressure monitoring and agressive therapy in neurologic practice. Arch Neurol 42: 1194-1195, 1985.
29. Ropper AH: Treatment of intracranial hypertension. En: Neurological and neurosurgical intensive care. Ropper AH Ed. New York, 1993, Rayen press: 29-52,
30. Saul T, Ducker T: Effect of intracranial pressure monitoring and aggressive treatment on mortality in severe head injury, J Neurosurg 56: 498-503, 1982.
31. Stovring J: Descending tentorial herniation: findings on computed tomography, Neuroradiology 14: 101-105, 1977.
32. Stuart G, Marry G, Smith J, Yelland J: Severe head injury managed without intracranial pressure monitoring, J Neurosurg 59: 601-605, 1983,
33. Toutant S, Klauber M, Marshall L, Toole B, Bowers S, SeelingJ, Varnell J: Absent or compressed basal cisterns on first CT scan: ominous predictors of outcome in severe head injury, J Neurosurg 61: 691-694, 1984,
34. van Dongen K, Braakman R, Gelpke G: The prognostic value of computarized tomography in coma-tose head-injuried patients, J Neurosurg 62: 383388, 1983.
35. Ward J, Becker D, Miller D, Choi S, Marmarou A, Wood Ch, Newlon P, Keenan R: Failure of prophylactic barbiturate coma in the treatment of severe head injury, J Neurosurg 62: 383-388, 1985,
36. Weinstein J, Langfitt T, Bruno L, Zaren H, Jackson J: Experimental study of patterns of brain distortion and ischemia produced by an intracranial mass, J Neurosurg 28: 513-522, 1968,
37. Yoneda S, Matsuda M, Handa H, Gotoh H, Tsuda E: Dynamics of transtentorial herniation. En: Shulman, Marmarou, Miller,
Becker, Hochwald y Brock (Eds.): Intracranial Pressure IV. Berlin, Springer, 1980: 106-110,
