REV ARGENT NEUROC | VOL. 31, N° 1 : 1-9 | 2017
Clipado de aneurismas de la arteria cerebral anterior distal: revisión anatómica y presentación de casos
Marcos D. Chiarullo,1 Pablo A. Rubino,1 Román P. Arévalo,1 Jorge Lambre,1 Mariano B. Pirozzo,1 Jorge Mura2
1Hospital Alta Complejidad en Red “El Cruce”, Florencio Varela. Buenos Aires. Argentina
2Instituto de Neurocirugía Asenjo. Universidad de Chile. Santiago, Chile
RESUMEN
Objetivos: Revisar las consideraciones anatómicas y quirúrgicas de los aneurismas de la arteria cerebral anterior distal y sus abordajes. Exponer nuestra casuística en esta patología.
Material y Método: Un total de 4 especímenes cadavéricos previamente fijados con formalina e inyectados con silicona, fueron disecados bajo visión microscópica para el estudio anatómico de la arteria cerebral anterior y sus abordajes. Asimismo, se realizó un análisis retrospectivo de una serie de 15 pacientes portadores de esta patología que fueron resueltos con técnica microquirúrgica en nuestra institución.
Resultados: Los abordajes pterional e inter hemisférico anterior lograron exponer la totalidad de la arteria cerebral anterior distal y el origen de sus ramas en los estudios cadavéricos. En cuanto a la serie de casos, un total de 15 pacientes portadores de aneurismas de la arteria cerebral anterior distal fueron intervenidos quirúrgicamente entre septiembre de 2009 y septiembre de 2016. La distribución de dichos aneurismas fue la siguiente: 3 del segmento infracalloso, 8 del segmento precalloso y 4 del segmento supracalloso de la arteria cerebral anterior. Catorce aneurismas fueron alcanzados mediante abordaje interhemisférico anterior y uno mediante el abordaje pterional. Los estudios de control demostraron la exclusión total del aneurisma en todos los pacientes. No se observó mortalidad o morbilidad agregada en nuestra serie.
Conclusión: Los estudios de laboratorio permitieron conocer en detalle la anatomía de la ACA distal y las consideraciones de sus abordajes. Si bien se necesitan estudios comparativos, creemos que la cirugía continúa teniendo vigencia en la resolución de este tipo de aneurismas.
Palabras claves: Aneurismas; Arteria Cerebral Anterior; Abordaje Pterional; Abordaje Interhemisférico
ABSTRACT
Objectives: (1) To describe the anatomical and surgical features of distal anterior cerebral artery (ACA) aneurysms, and approaches to accessing them; and (2) to review their management in live patients.
Materials and Methods: Four cadaveric specimens previously formalin-fixed and silicone-injected were dissected under microscopic vision to anatomically study the ACA and various approaches to accessing it. A retrospective study then was performed to analyze our own series of 15 patients with distal ACA aneurisms successfully treated micro-surgically.
Results: In cadavers, both the pterional and anterior interhemispheric approach exposed the entire distal ACA, including the origin of its branches. Between September 2009 and September 2016, we operated upon 15 patients with distal ACA aneurysms: three within the infracallosal segment, eight in the precallosal segment, and four in the supracallosal segment of the ACA. Fourteen of these aneurysms were accessed via an anterior inter-hemispheric approach, and one via a pterional approach. Follow-up imaging demonstrated complete exclusion of the aneurysm in all patients, and no patient died or suffered significant long-term morbidity.
Conclusion: Both in cadavers and live patients, pterional and anterior inter-hemispheric approaches provide excellent ACA exposure. While controlled studies remain necessary, we believe that surgery continues to be a valid option in the management of distal ACA aneurisms.
Keywords: Aneurysms; Anterior Cerebral Artery; Pterional Approach; Interhemispheric Approach
INTRODUCCIÓN
Los aneurismas de la arteria cerebral anterior (ACA) distal, se definen como aquellos ubicados en el segmento post comunicante de dicha arteria. Generalmente se localizan en el origen de las ramas que nacen de este segmento, aunque pueden verse también en sus sucesivas divisiones.
Estos aneurismas son incluidos dentro del denominado grupo de aneurismas infrecuentes. Según la base de datos de aneurismas intracraneales de la universidad de Finlandia, sobre un total de 3005 aneurismas cerebrales documentados, los de la ACA distal dan cuenta del 5,4% del total. De estos, 0,8% corresponden a aneurismas originados en ramas del segmento infracalloso, 4% en ramas originadas en el segmento precalloso y 0,6% a ramas originadas en los segmentos supracallosos.1,2 Los más frecuentes ocurren en el origen de la arteria calloso marginal la cual, si bien tiene un origen variable, la mayoría de la veces se origina del segmento precalloso (A3) de la ACA.3
El objetivo de esta revisión es exponer las consideraciones anatómicas de la ACA y los detalles inherentes a los abordajes quirúrgicos de la patología aneurismática de esta arteria. Por último, se realiza la presentación de nuestra serie de casos de aneurismas de la ACA distal resueltos con técnica microquirúrgica.
MATERIAL Y MÉTODO
Un total de 4 especímenes cadavéricos previamente fijados con formalina e inyectados con silicona roja y azul para diferenciar arterias y venas respectivamente fueron disecados bajo visión microscópica (Carl Zeiss Microscopy Ltd; Cambridge) en el laboratorio de neuroanatomía microquirúrgica del Dr. Albert Rhoton Jr. del departamento de neurocirugía de la Universidad de Florida, EE.UU. Concomitantemente, se realizó un estudio observacional, descriptivo, retrospectivo analizando en detalle las historias clínicas de 15 pacientes portadores de la patología en nuestro hospital, entre septiembre de 2009 y septiembre de 2016. Se analizaron además imágenes pre, intra y postoperatorias.
RESULTADOS
Consideraciones anatómicas
Arteria cerebral anterior
Surge como la más medial y de menor calibre de las ramas de bifurcación de la arteria carótida interna (ICA), la cual ocurre inmediatamente debajo de la sustancia perforada anterior (SPA). Al alcanzar la línea media, la ACA se une con la contralateral a través de la arteria comunicante anterior (AcomA) (fig. 1A). Posteriormente, la arteria penetra en la fisura interhemisférica y asciende en un recorrido aproximadamente vertical, por debajo de la rodilla del cuerpo calloso (CC). Luego, bordea al mismo primero anterior y luego superiormente, terminando, como un fino vaso, por detrás del esplenio del CC en el plexo coroideo del techo del tercer ventrículo (fig. 1B, C, D y E).
En su recorrido, la ACA da arterias perforantes que irrigan estructuras profundas y ramas corticales que irrigan la parte más medial de la cara orbitaria del lóbulo frontal, los dos tercios anteriores de la cara medial y el margen superior de la cara lateral del hemisferio cerebral.
En el 50% de los casos, la ACA izquierda es anterior a la derecha. De esta manera, la AcomA tiene una disposición oblicua o anteroposterior (fig. 2D). En el 30%, la ACA derecha es anterior a la izquierda y en el 20%, ambas ACAs son paralelas.4
La ACA se divide en dos: segmento pre comunicante o A1 y segmento post comunicante. Este último posee a su vez un segmento infracalloso o A2, precalloso o A3, supracalloso o A4 y post calloso o A5.4-6
Arteria cerebral anterior proximal o pre comunicante (A1)
Se extiende desde el origen de la ACA en la bifurcación carotídea, la cual sucede en la cisterna carotídea, debajo de la SPA y lateral al quiasma óptico (QO). Desde allí, la arteria se dirige medial y anteriormente cruzando el QO, penetrando en la cisterna de la lámina terminalis y alcanzando la línea media. Ambos segmentos A1 se unen en la línea media por la AcomA4-6 (fig. 1A, D, 2D y 3B).
En la mayoría de los casos, un segmento A1 es dominante en relación al otro. Esta es una característica anátomo-patológica de relevancia, ya que el 85% de los aneurismas de la AcomA se dan en presencia de un segmento A1 hipoplásico.3
Arteria comunicante anterior
Representando una parte fundamental en la conformación del polígono de Willis (fig. 1A), esta arteria comunica ambas ACAs. Los múltiples estudios anatómicos de esta arteria dan cuenta de la amplia variabilidad que existe en cuanto a su localización, orientación, longitud, diámetro y morfología. De esta manera, la AcomA puede estar localizada encima del QO (70%) o por encima del nervio óptico (30%).14 Dependiendo de la relación espacial de una ACA con respecto a la otra, la AcomA puede tener, en orden de frecuencia, una orientación oblicua, antero-posterior o transversal. El largo y el diámetro promedio de esta arteria es de 2,5 y 1,6 mm respectivamente. En un corte transversal puede tener forma triangular, redondeada o plana.4
Las arterias perforantes de la AcomA nacen generalmente de su cara posterior o superior. Muy raramente lo hacen desde la cara anterior o inferior. Irrigan de manera variable al infundíbulo, QO, hipotálamo anterior, lámina terminalis, rostrum y rodilla del CC, comisura blanca anterior, septum pellucidum y parte de las columnas anteriores del fornix. La arteria subcallosa irriga al rostrum y rodilla del CC.15 Los aneurismas proximales de A2 pueden involucrar alguna de estas ramas perforantes.4,7,8
Arteria cerebral anterior distal o post comunicante (A2-A5)
Segmento infracalloso (A2)
Se extiende desde la unión de A1 con la AcomA hasta la unión del rostrum con la rodilla de CC donde comienza el segmento A3. Desde su origen, asciende en un recorrido vertical por delante de la lámina terminalis, en la cisterna que recibe el mismo nombre, ubicándose por debajo de la parte anterior del CC (figs. 2B, C, D y 3B).
Este segmento da tres ramas mayores: la arteria recurrente de Heubner (RecA) y las arterias orbitofrontal (OFA) y la frontopolar (FPA).
La RecA nace de la parte más distal de A1, de la unión A1-A2 o de la parte más proximal de A2 (lo más frecuente). Raramente puede nacer de la OFA. Desde allí, se dirige paralela y en sentido inverso al segmento A1 pasando por la bifurcación de la ICA y la parte más proximal de la arteria cerebral media (MCA) para terminar en la SPA. Puede estar ausente (3%), encontrarse como única rama, estar duplicada (12%) o triplicada. Realiza su ingreso a la SPA posterior a su división en múltiples ramas (hasta 12 ramas) o como un tronco único, dividiéndose posteriormente (fig. 2D). Irriga la cabeza del núcleo caudado, y la parte anterior del núcleo lenticular, brazo anterior de la cápsula interna y el fascículo uncinado.
La OFA corre anterior e inferiormente e irriga al nervio y tracto olfatorio, al girus recto y a los girus fronto-basales mediales. La FPA se dirige anteriormente para irrigar la cara medial y lateral del polo frontal (figs. 1C, D y 3B).

Figura 1: Anatomía de la arteria cerebral anterior. A) Visión superior del polígono de Willis. El segmento A1 de la arteria cerebral anterior se origina en la bifurcación carotídea, corre anterior y medialmente. Por encima del quiasma óptico la arteria cerebral anterior se une con la contralateral a través de la arteria comunicante anterior. Nótese que la arteria cerebral anterior izquierda es anterior a la derecha. B) Visión de la cara medial del hemisferio cerebral y la hoz cerebral. La arteria cerebral anterior se encuentra íntegramente por detrás y debajo del borde libre de la hoz del cerebro, lo que permite el acceso unilateral a ambas arterias. C) Visión de la cara medial del hemisferio cerebral. La hoz ha sido removida preservando el seno longitudinal inferior. El segmento A2 asciende en un recorrido vertical por debajo de la rodilla del cuerpo calloso. El segmento A3 bordea anteriormente a la rodilla del cuerpo calloso. El segmento A4 y A5 se extiende por encima del cuerpo calloso y termina como un fino vaso por detrás del esplenio del cuerpo calloso. Nótese la arteria calloso marginal originándose de la unión de los segmentos A2 – A3. D) Visión de la arteria cerebral anterior y sus ramas mediante una disección de la porción anterior de la fisura interhemisférica. Obsérvese los segmento A1, A2 y A3 y las arterias orbitofrontal y frontopolar. E) Disección de la fisura interhemisférica desde una visión superior. Se observa el segmento A4 y A5 sobre la rodilla y el cuerpo del cuerpo calloso. AcomA., Arteria comunicante anterior; Corp., cuerpo; Falx., hoz cerebral; Genu., rodilla del cuerpo calloso; ICA., arteria carótida interna; III N., tercer par craneal; MCA., arteria cerebral media; ON., nervio óptico; PcomA., arteria comunicante posterior; Rec. A., arteria recurrente de Heubner; SCA., arteria cerebelosa superior; Segm., segmento; Splen., splenium; Rost., rostrum; Talamop. A., arteria tálamo perforantes. Ambas arterias pueden originarse también del segmento A1 aunque esto es infrecuente. El segmento A2 da además, un promedio de 4 arterias perforantes basales que se dirigen posteriormente e irrigan la parte anterior del hipotálamo, septum pellucidum, comisura blanca anterior y pilares del fornix.
4-6 Segmento precalloso (A3) Se extiende desde la unión del rostrum con la rodilla del CC y termina en el punto donde la arteria se hace horizontal. El segmento A3, como también el segmento A4 y A5, corre por el surco calloso en el 60% de los casos. Puede hacerlo también por el surco del cíngulo en el 33% o por el girus de cíngulo en el 7% restante (figs. 1B, C, D y 3B).
El segmento A3 da la arteria calloso marginal (CMA) las arterias frontales internas anterior, media y posterior. Estas últimas son variables y pueden nacer de troncos comunes o incluso estar ausentes. Cuando están presentes, irrigan la cara medial y lateral del girus frontal superior.
La CMA es la mayor y la más importante de las ramas de la ACA distal. Si bien su origen más frecuente es en A3 (73%), puede originarse además de A2 o A4. Esta arteria está ausente en el 9% al 18% de los casos. Cuando está presente, su diámetro promedio es de 1,8 mm. Desde su origen corre por el surco del cíngulo, paralela a la ACA distal y se divide en dos o más ramas corticales. El origen de la CMA es el sitio más frecuente de asiento de aneurismas de la ACA distal (fig. 1B y C).
4-6 Segmento supra y post calloso (A4 y A5) El segmento A4 se origina en el punto en que la arteria se hace horizontal para recorrer la cara superior del CC. El reparo anatómico para la división de estos dos segmentos es la sutura coronal. Las ramas corticales más importantes son la arteria frontal interna posterior (la cual también puede nacer de A3), la arteria paracentral y las arterias parietal superior e inferior. Irrigan de adelante hacia atrás, la parte posterior del girus frontal superior, parte del girus del cíngulo, área premotora, motora y sensitiva de la cara medial, precunea y la parte adyacente de la cunea (figs. 1B, C, E y 3D).
4-6 Variantes anatómicas de la ACA distal La ACA ácigos (0,2 al 4%) es una variante anátomo-patológica en donde ambos segmentos A2 se encuentran unidos formando un tronco común que irriga ambos hemisferios. Esta variante es un reconocido factor predisponente para la formación de aneurismas del tope de la ACA ácigos ya que el 80% de las ACA ácigos son asiento de aneurismas de este tipo. En la ACA bihemisférica (0,2 al 12%), un segmento A2 es hipoplásico y la A2 dominante da ramas que irrigan ambos hemisferios. En el caso de la triplicación del segmento A2 (3 al 13%), el ramo medio de la triplicación irriga al CC.
9
Abordajes a los aneurismas de la arteria cerebral anterior distal
Abordaje pterional
Este abordaje permite, mediante la vía subfrontal lateral o trans-silviana, el acceso microquirúrgico a los aneurismas proximales del segmento A2.
El posicionamiento cefálico de la cabeza del paciente, previamente fijada con cabezal de tres pines, se realiza mediante los cinco movimientos descriptos por Yasargil: tracción, elevación, deflexión, rotación y lateralización (fig. 2A).10,11
Luego del peinado y tricotomía con máquina eléctrica sobre el área de incisión, realizamos la marcación arciforme, partiendo 1 cm. por delante y por encima del trago, a fin de evitar lesionar la arteria temporal superficial y terminando sobre la línea media en el sitio de implantación capilar. Luego de la colocación de los campos, se realiza la incisión del cuero cabelludo, la cual se puede efectuar según necesidad, en un solo plano (tipo miocutánea) o en diferentes planos mediante disección interfascial del músculo temporal (fig. 2B). Realizamos la craneotomía mediante 4 agujeros de trépanos unidos con cierra de Gigli o craneótomo. Comenzamos con el primer agujero de trepano inmediatamente superior y posterior a la sutura fronto-cigomática. El segundo agujero lo ubicamos 2 cm. anterior y medial al agujero previo. El tercero en la parte más posterior de la línea temporal superior expuesta y el cuarto en la parte media de la escama del temporal (fig. 2C). Luego del drilado del techo y la pared lateral de la órbita, que tiene como finalidad aumentar el ángulo de visión quirúrgica, se realiza la apertura de duramadre mediante una incisión en forma de herradura con base hacia la órbita y una descarga a nivel temporal. En algunas ocasiones, puede requerirse complementar este abordaje con la remoción del techo y pared lateral de la órbita y la arcada cigomática (abordaje orbito-cigomático) aumentando de esta forma el ángulo de visión quirúrgica (fig. 2D).3,10-13
Abordaje inter hemisférico anterior
Este tipo de abordajes permite exponer la parte distal del segmento A1 y la comunicante anterior, la ACA distal y el origen de sus ramas. Debido a que dichos segmentos de la arteria pericallosa se encuentran por detrás y debajo del borde libre de la hoz del cerebro (fig. 1B), se puede acceder a ambas arterias desde uno u otro lado de la misma, optándose por el lado derecho de ser posible.
Luego de la fijación con cabezal de tres pines, la cabeza del paciente es colocada en posición neutra, con una elevación de 20 grados por encima del nivel cardíaco.
El tipo de incisión puede variar dependiendo de la localización del aneurisma.
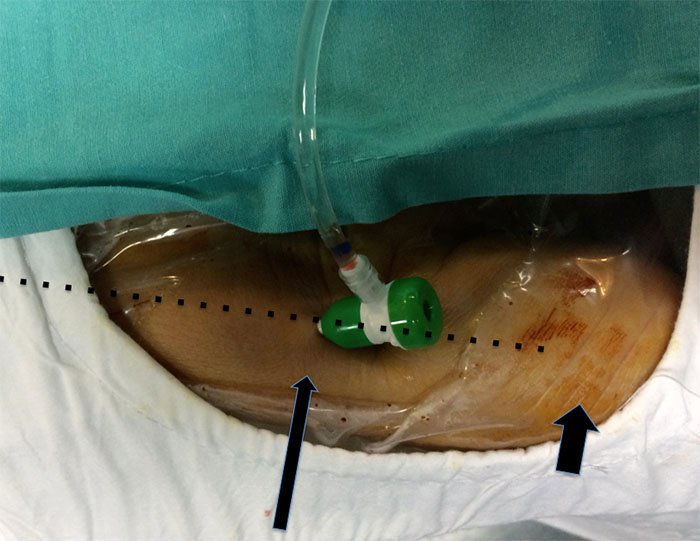
Para todos los aneurismas de la ACA distal puede realizarse una incisión coronal siguiendo la sutura del mismo nombre o paralela y levemente anterior a la está (fig. 3A). Para aneurismas del segmento A4 y A5 puede realizarse también una incisión en forma de herradura de pedículo anterior o lateral. Independientemente de la elección de la incisión, la tricotomía deberá realizarse paralela a ésta con un margen de 2 cm. (fig. 3C).

Figura 2: Abordaje pterional. A) Movimientos de posicionamiento cefálico descriptas por Yasargil mediante tracción, elevación, deflexión, rotación y lateralización. B) Recuadro (superior izquierdo): posición cefálica final y marcación. Incisión arciforme, elevación subperióstica del colgajo y disección interfascial del músculo temporal. Obsérvese que el panículo adiposo interfascial ha sido elevado para prevenir la lesión del ramo frontal del nervio facial. C) El músculo temporal ha sido elevado desde su fascia profunda y rebatido caudalmente. La craneotomía fue realizada mediante cuatro agujeros de trepano unidos con craneótomo. La duramadre temporal y frontal ha sido expuesta. El techo y pared lateral de la órbita han sido drilados para aumentar el ángulo de visión quirúrgica. D) Vista trans-silviana de la arteria carótida supraclinoidea y su bifurcación, ambos segmento A1, arteria comunicante anterior, arteria recurrente de Heubner y ambos segmentos A2. La ACA izquierda es anterior a la derecha. Nótese el alcance de este abordaje al segmento proximal de A2. AcomA., Arteria comunicante anterior; ICA., arteria carótida interna; III N., tercer par craneal; Lam. Term., lámina terminalis; ON., nervio óptico; PcomA., arteria comunicante posterior; Rec. A., arteria recurrente de Heubner; Segm., segmento.

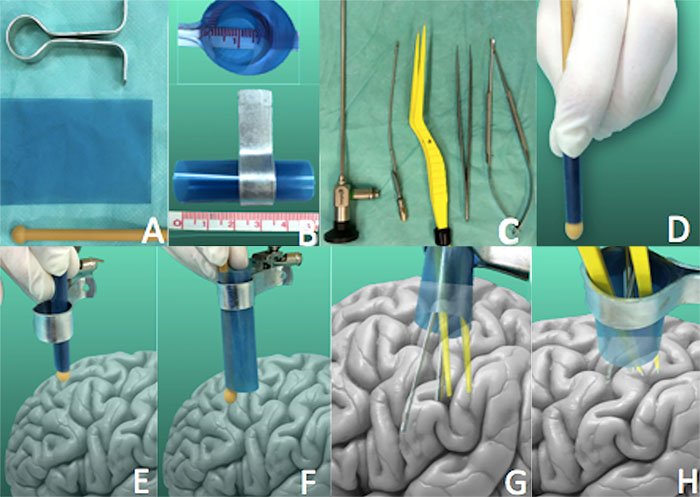
Figura 3: Abordaje interhemisférico anterior. A) Recuadro (inferior izquierdo): posición cefálica neutra. Se realizó incisión coronal. El colgajo frontal fue rebatido anteriormente. El periostio ha sido preservado vascularizado para ser utilizado en caso de ser necesario. B) Recuadro (inferior derecho): se realizó la craneotomía frontal pasante a la línea media, exponiendo el seno longitudinal superior. Luego de la apertura dural, se observa la vista anterior de la fisura interhemisférica con la arteria cerebral anterior en sus segmentos A1 distal, infracalloso o A2 y precalloso o A3 y el origen de sus ramas. Nótese el acceso que este abordaje permite a la porción distal de A1, a la AcomA, y al segmento A2 y A3 en toda su extensión. C) Recuadro (superior derecho): posición cefálica neutra, con mínima elevación y flexión. Variante en herradura de la incisión para el abordaje interhemisférico anterior a los segmentos A4 y A5. Nótese la exposición pre y postcoronal en dos tercios y un tercio de la extensión anteroposterior respectivamente. La incisión permite además la exposición de la sutura coronal (línea media). D) Recuadro (inferior izquierdo): la craneotomía pasante a la línea media, mediante agujeros de trepano unidos con craneótomo, permite la exposición del seno longitudinal superior. Se realizó la apertura de la duramadre con base hacia el seno longitudinal superior y posterior disección de la fisura interhemisférica. Se observa el cuerpo calloso en el fondo de la fisura interhemisférica. Nótese la exposición que este abordaje permite a los segmentos A4 y A5 de la ACA. AcomA., Arteria comunicante anterior; Corp. Call., cuerpo calloso; Genu., rodilla del cuerpo calloso; Lam. Term., lámina terminalis; Quiasm., quiasma; Segm., segmento; Sup. Long. Sin., seno longitudinal superior.
Luego de la colocación de los campos, se procede a incidir por la marcación previa hasta el plano subperióstico.
Se realiza el legrado del colgajo el cual se ancla mediante anzuelos de retracción.
Es importante lograr una amplia exposición del hueso frontal hasta las eminencias supraorbitarias, en el caso de aneurismas del segmento A2 y A3 y de un colgajo óseo pre y post coronal en el caso de aneurismas de segmento A4 y A5 (figs. 3, 4 y 5).
En todos los casos realizamos una craneotomía pasante a la línea media en al menos 1 cm., de forma tal que permita exponer el seno longitudinal superior (SLS) para poder movilizarlo medialmente junto con la hoz cerebral (fig. 3B y D). Es importante realizar un colgajo óseo amplio en sentido rostro caudal a fin de poder acceder por delante y/o por detrás de las venas puentes que llegan al SLS desde la cara lateral del hemisferio cerebral, sin necesidad de coagularlas y seccionarlas.14 La apertura dural se realiza en forma de herradura con base hacia el SLS.
Mediante técnica microquirúrgica, se realiza la disección interhemisférica, colocándose separadores autoestáticos o cilindros de algodón para mantener la apertura de la fisura (fig. 3B y D).3,15,16
CASOS CLÍNICOS
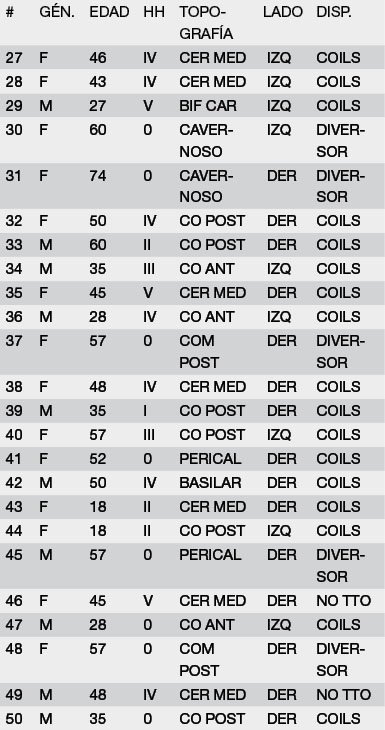
TABLA 1: CASOS CLÍNICOS
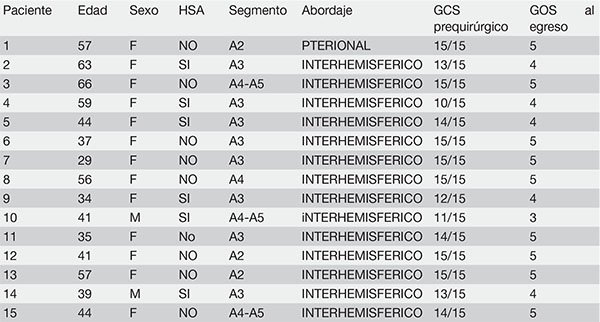
La serie quirúrgica se compone de 15 pacientes, con un neto predominio femenino (n=13 - 86,67%). El promedio de edad fue de 46,8 años.
La mayor parte de nuestros pacientes fueron portadores de aneurismas incidentales, sin sintomatología jerarquizable; sin embargo, se registraron 6 casos (15%) de hemorragia subaracnoidea (HSA) vinculada a la rotura del aneurisma pericalloso en cuestión. No se registraron casos de hidrocefalia tardía relacionada a HSA.
Los pacientes que fueron incluidos en esta serie portaban los siguientes aneurismas:
- 3 casos de aneurismas del segmento A2.
- 8 casos de aneurismas del segmento A3.
- 4 casos de aneurismas del segmento A4-A5.
Todos ellos, a excepción de un caso de aneurisma de A2, fueron abordados mediante el abordaje interhemisférico anterior.
En lo que respecta a los resultados quirúrgicos de esta serie, se registró un Glasgow Outcome Score (GOS) al alta de 4-5 en 14 casos, y un único caso de GOS 3, quien se encuentra bajo estricta actividad fisiokinésica con buena evolución.
La tabla 1 reúne los datos de la presente serie quirúrgica.
DISCUSIÓN
Los aneurismas de la ACA distal se definen como aquellos localizados a nivel de los segmentos postcomunicantes de dicha arteria. Generalmente nacen en el origen de las diferentes ramas de dicho segmento. Perlmutter y Rhoton Jr. y cols. publicaron en el año 1978 una descripción detallada de los diferentes segmentos de la ACA dividiéndola en un segmento precomunincante o A1, un segmento infracalloso o A2, un segmento precalloso o A3, un segmento supracalloso o A4 y un segmento postcalloso o A5. La sutura coronal divide estos últimos dos segmentos.4-6
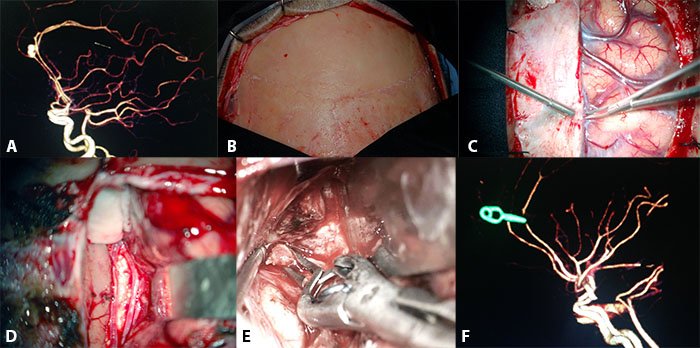
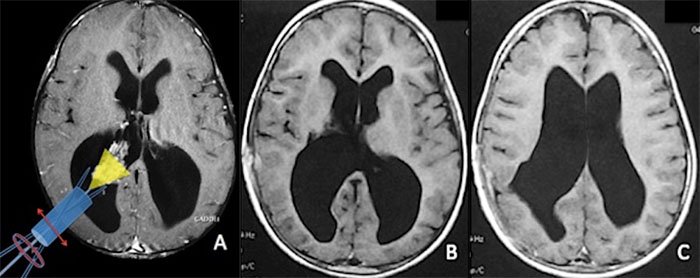
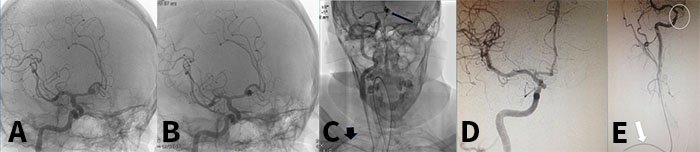
Figura 4: A) Angio-TC que evidencia aneurisma del segmento A3 (precalloso) derecho. B) Incisión coronal. Nótese la exposición pre y postcoronal. C) Apertura dural en herradura con base hacia el seno longitudinal superior. D) Fotografía bajo microscopio quirúrgico en la que se observa la disección finalizada de la fisura interhemisférica, en cuyo fondo se aprecian ambas arterias pericallosas descansando sobre el cuerpo calloso, de aspecto nacarado. E) Clipado microquirúrgico del aneurisma inmediatamente por delante de la rodilla del cuerpo calloso mediante la utilización de un clip recto corto. F) Control de angio-TC postoperatoria mostrando el correcto clipado y la completa exclusión del aneurisma.

Figura 5: A) Angiografía digital que objetiva aneurisma del segmento A2 (infracalloso) izquierdo. En el ángulo inferior derecho se aprecian los cortes tomográficos que demuestran la presencia de hemocisterna generalizada y más precisamente en relación a la cara anterior del cuerpo calloso en el sector más anterior y declive de la fisura interhemisférica. B-C) Abordaje interhemisférico anterior mediante craneotomía bifrontal basal. D) Se aprecia domo aneurismático inmediatamente inferior al genu del cuerpo calloso, cercano a la unión A2-A3. E) Clipado microquirúrgico del aneurisma mediante clip curvo. F) Control de angio-TC postoperatorio mostrando el correcto clipado y la completa exclusión del aneurisma.
Lehecka y col. afirman que estos aneurismas dan cuenta del 5,4% del total de los aneurismas cerebrales. De estos, 0,8% corresponden a aneurismas originados en ramas del segmento infracalloso, 4% en ramas originadas en el segmento precalloso y 0,6% a ramas originadas en los segmentos supracallosos. El alto porcentaje de los aneurismas del segmento precalloso (70% del total de aneurismas de la ACA distal) se debe a que el sitio más frecuente de asiento de estos aneurismas es el origen de la CMA, la cual si bien tiene un origen variable, nace más frecuentemente del segmento A3.1,2
El abordaje pterional descripto por Yasargil en el año 1984 permite el acceso a la patología aneurismática de la circulación anterior. No obstante, en lo que respecta a los aneurismas de la ACA distal, es limitado solo a la porción más proximal del segmento A2.10-13
El abordaje interhemisférico y sus múltiples variaciones introducidas desde su descripción original, permite el acceso a la porción distal de A1, la AcomA y a la totalidad de los segmento A2 a A5.
Hernesniemi y col. entre otros, han utilizado con éxito este abordaje, según lo descripto en sus publicaciones, para el tratamiento de los aneurismas de la ACA distal.6-8,17-20
En nuestra serie, el origen más frecuente de los aneurismas de la ACA distal fue el nacimiento de la arteria calloso marginal en el segmento A3 de la arteria pericallosa. Hemos utilizado el abordaje pterional para el acceso a los aneurismas de la porción más proximal del segmento A2 mientras que el resto de los aneurismas de la ACA distal debieron ser clipados por vía interhemisférica anterior. Dichas variables se correlacionaron ampliamente con nuestros hallazgos de laboratorio y lo descripto en la bibliografía.
CONCLUSIÓN
El conocimiento detallado de la anatomía de la ACA y sus variantes anatómicas es indispensable para la resolución quirúrgica de los aneurismas que de ella se originan. Los abordajes pterional e interhemisférico anterior y sus variantes lograron el acceso a la totalidad de los aneurismas de la ACA distal presentados en nuestra serie. Por tal motivo, el estudio y entrenamiento exhaustivo en el desarrollo de estos abordajes es una herramienta fundamental en el arsenal del neurocirujano. Se logró la exclusión completa, definitiva y con buenos resultados en la totalidad de los casos de nuestra serie. Si bien se requiere de estudios comparativos, creemos que el tratamiento microquirúrgico de los aneurismas de la ACA distal, continúa siendo un técnica vigente y efectiva en la resolución de esta patología.
BIBLIOGRAFÍA
- Lehecka M, Dashtu R, Hernesniemi J, et al. Microneurosurgical management of the aneurysms at A2 segment of anterior cerebral artery (proximal pericallosal artery) and its frontobasal branches. Surg Neurol 2008;70(3):232-46.
- Lehecka M, Niemela M, Seppanen J, et al. No long-term excess mortality in 280 patients with ruptured distal anterior cerebral artery aneurysms. Neurosurgery 2007;60(2):235-41.
- Rhoton Jr. Al. Aneurysms. Neurosurgery 2002;51(1 Suppl):121-158.
- Rhoton Jr. Al. The supratentorial arteries. Neurosurgery 2002;51(4 suppl):S53-S120.
- Perlmutter D, Rhoton Jr. Al. Microsurgical anatomy of the anterior cerebral – anterior comunicanting – recurrent artery complex. J Neurosurg 1976;45(3):259-76.
- Perlmutter D, Rhoton Jr. Al. Microsurgical anatomy of the distal anterior cerebral artery. J Neurosurg 1978;49(2):204-28.
- Hernesniemi J, Dashti R, Lehecka M, et al. Microneurosurgical management of anterior communicanting artery aneurysms. Surg Neurol 2008;70(1):8-28.
- Yasargil MG. Anterior cerebral artery complex. In: Yasargil MG, editor. Microneurosurgery, Vol. I. Stuttgart: Georg Thieme Verlag; 1984. p. 92-128.
- Baptista AG. Studies on the Arteries of the Brain. Ii. the Anterior Cerebral Artery : Some Anatomic Features and Their Clinical Implications. Neurology. 1963;13:825–835.
- Yasargil MG. Interfascial pterional (frontotemporosphenoidal) craniotomy, in Yasargil MG (ed): Microneurosurgery. Stuttgart, Georg Thieme Verlag, 1984, Vol. 1, pp. 215-220.
- Yasargil MG, Reichman MV, Kubik S. Preservatión of the frontotemporal branch of the facial nerve usingthe interfascial temporalis flap for pterional craniotomy. J Neurosurg (1987) 67:464–466.
- Chaddad-Neto F, Campos Filho JM, Dória-Netto HL, Faria MH, Carvalhal Ribas G. Evandro Oliveira. The pterional craniotomy: tips and tricks. Arq Neuropsiquiatr (2012) 9:727-732.
- Chiarullo M, Seclen Voscoboinik D, Vallejos Taccone W, Rubino P, et al. Abordaje pterional: alcances y revisión de la técnica quirúrgica. Rev Argent Neuroc 2014;28(4):156-161.
- Rhoton Jr. Al. The cerebral vein. Neurosurgery 2002;15(4 suppl):S159-S205.
- Yasargil MG, Carter LP. Saccular aneurysms of the distal anterior cerebral artery. J Neurosurg 1974;40(2):218-23.
- Yasargil MG. Distal anterior cerebral aneurysms. In: Yasargil MG, editor. Microneurosurgery, Vol. II. Stuttgart: Georg Thieme Verlag; 1984. p. 224-31.
- Hernesniemi J, Tapaninaho A, Vapalahti M, et al. Saccular aneurysmsof the distal anterior cerebral artery and its branches. Neurosurg 1992;31(6):994-9.
- Lehecka M, Dashtu R, Hernesniemi J, et al. Microneurosurgical management of the aneurysms at A3 segment of anterior cerebral artery. Surg Neurol 2008;70(2):134-51.
- Lehecka M, Lehto H, Niemela M, et al. Distal anterior cerebral artery aneurysms: treatment and outcome analysis of 501 patients. Neurosurg 2008;62(3):590-601.
- Ture U, Yasargil MG, Krisht AF. The arteries of the corpus callosum: a microsurgical anatomic study. Neurosurgery 1996;39(6):1075-85.
Comentario
El presente trabajo muestra el estado actual del tratamiento microquirúrgico de los aneurismas de la arteria cerebral anterior distal. Fue enriquecido con una excelente ilustración y descripción anatómica. Nos obliga a utilizar con propiedad la nomenclatura de estos aneurismas por su real ubicación anatómica de los segmentos arteriales, ya que en la jerga se los denomina y engloba como pericallosos.
En mi experiencia estos aneurismas son múltiples con cierta frecuencia pudiendo acompañar otros que se han roto, obligando a veces a tratarlos en conjunto.
Los resultados clínicos fueron muy buenos, aunque no se ha brindado información de si los controles post-clipado fueron realizados con angiografía digital u otro método.
El conocimiento anatómico y el manejo los abordajes a realizar para clipar estos aneurismas tal como lo presenta el artículo, son de gran utilidad para los neurocirujanos en formación (y no solo) para tratar exitosamente esta patología.
En presencia de arterias tortuosas y un cayado aórtico elongado, como se ve en pacientes añosos y/o hipertensos, el tratamiento endovascular de este tipo de aneurismas distales puede ser extremadamente dificultoso, con el resultante aumento de complicaciones.
Flavio Requejo
Hospital J P Garrahan
Comentario
Los autores nos presentan un trabajo pulcro, conciso y claro sobre anatomía con aplicación microquirúrgica para la resolución de los aneurismas de la ACA distal, y sus resultados. En el mismo se destaca la excelencia iconográfica de las disecciones cadavéricas e imágenes operatorias. La fortaleza metodológica de la presente comunicación se funda en el tamaño de su serie, considerando la baja prevalencia de esta patología. Se documentan dos de los quince casos reportados. Conceptualmente pertinente, ya que como es bien establecido, la patología aneurismática de esta región presenta una peor historia natural recomendándose siempre su tratamiento; siendo en nuestro criterio el clipado microquirúrgico el procedimiento de elección. Las características morfológicas y configuracionales de estas lesiones (sésiles, ateromatosas, micóticas) colocan a las terapias endovasculares en un rol secundario. La resolución quirúrgica de los aneurismas de esta localización ofrecen múltiples desafíos: la cisura interhemisférica y la cisterna del cuerpo calloso son espacios estrechos, las venas frontales ascendentes a menudo restringen el área de trabajo, existe una gran variabilidad anatómica de los ramos arteriales distales, la profundidad de la hoz del cerebro puede ser escasa y por tanto ambas circunvoluciones cinguladas pueden estar densamente adheridas, la angiografía digital no siempre esclarece la lateralidad del vaso madre, el aneurisma suele presentarse en una posición más proximal a la supuesta, el fondo del saco aneurismático habitualmente apunta hacia el cirujano y el control proximal se consigue muchas veces tardíamente. Como aporte al contenido del presente trabajo y a título personal, preferimos para la resolución de estos aneurismas (A2-A5) un abordaje precallosal con una craneotomía por sobre el seno neumático frontal, lo que disminuye el trayecto de disección en la mayoría de los casos (A3), pero fundamentalmente nos permite un precoz y óptimo control del vaso aferente. Asimismo por este abordaje se puede resolver un aneurisma de la arteria comunicante anterior asociado, sin dificultades. En relación a la lateralidad del abordaje utilizamos el lado derecho, excepto cuando exista un hematoma intraparenquimatoso frontal donde debemos sospechar que la cúpula del aneurisma pueda estar densamente fijada a la pia del girus cingular, o incluso dentro del mismo, limitando así la retracción del lóbulo ipsilateral; por lo que accederemos de forma contralateral al hematoma. En tal caso la evacuación del mismo, si fuera necesaria para mejorar las condiciones de las cisternas, se puede realizar por un ojal practicado en la hoz del cerebro o por debajo de su borde inferior. Este trabajo se constituye en una importante referencia por el valor cuantitativo de la serie, su prolija revisión anatómica y la demostración de la eficacia de la técnica que se desprende de sus resultados.
Claudio Centurión
Clínica Privada Vélez Sársfield. Córdoba, Argentina
Comentario
El artículo reporta una interesante serie de aneurismas de la arteria cerebral distal revisando la anatomía microquirúrgica relacionada y los abordajes quirúrgicos realizados en estos pacientes. Es una serie valiosa en cuanto a la cantidad de pacientes operados en los siete años de observación y se asocia a una revisión de extrema utilidad para la correcta comprensión anatómica microquirúrgica del abordaje de estos aneurismas. La maravillosa iconografía presentada es uno de los pilares en que se basa la utilidad y aplicabilidad de este artículo. Los abordajes están presentados de manera clara y precisa. Personalmente, para los abordajes de estos aneurismas, me gusta analizar durante la planificación prequirúrgica, la ubicación de las venas puentes en el tiempo venoso de la angiografía. Este pequeño detalle permite definir con mayor precisión la ubicación anteroposterior de la craneotomía frontal medial para encontrar el “gap” necesario, disminuyendo el riesgo de lesión de las venas. Otro detalle a tener en cuenta, es la mayor dificultad existente en el abordaje de estos aneurismas cuando son del segmento A2 o A3 en relación a los más posteriores. La primera fase de disección en el abordaje interhemisférico se realiza a través de la cisura interhemisférica. Una vez disecadas y liberadas las densas bridas aracnoideas que fijan el borde superomedial del hemisferio cerebral a la duramadre lateral al seno longitudinal, se accede a esta cisura de fácil disección donde solo existen pocas y delicadas bridas aracnoideas. Por debajo del límite inferior de la hoz y hasta el techo de la cisterna pericallosa hay otra zona de densas bridas aracnoideas entre la piamadre de las superficies mediales de ambos lóbulos frontales, posiblemente relacionadas a la presencia cercana del seno longitudinal inferior y a la entrada al mismo de venas profundas. Esta zona de transición, de difícil disección por las firmes adherencias, se va agrandando de atrás para adelante. Es relativamente pequeña a nivel del cuerpo del cuerpo calloso y más amplia a nivel de A2 haciendo necesaria una disección delicada durante un mayor trayecto en los casos de aneurismas de A2 y A3. En cuanto a las consideraciones finales, coincido plenamente con los autores en que el tratamiento microquirúrgico de estos aneurismas continúa siendo una técnica vigente y efectiva para su resolución, no solo por la clara superioridad sobre las técnicas endovasculares en cuanto a efectividad en el cierre completo de los aneurismas, sino por las características estructurales particulares de los aneurismas de esta ubicación. De hecho, en nuestra experiencia en pacientes de mal grado (Hunt y Hess IV y V), donde nuestra indicación primaria general es el tratamiento endovascular, los aneurismas de la arteria cerebral distal fueron el grupo en el que más frecuentemente realizamos un “crossover” a la indicación microquirúrgica debido a la tendencia de estos a presentar un cuello amplio, generalmente de la dimensión del diámetro arterial, haciendo riesgosa la embolización con coils, por el peligro de migración de espiras del coil al vaso madre.
Matteo M. Baccanelli
Servicio de Neurocirugía, Hospital Italiano de Buenos Aires
Comentario
Los autores presentan una serie de 15 pacientes portadores de aneurismas de la arteria cerebral anterior en su segmento post comunicante, que fueron tratados, de manera exitosa en todos los casos, por tratamiento microquirúrgico. Además, el trabajo está prolijamente complementado con una serie de disecciones anatómicas de alta calidad que ayudan didácticamente a comprender mejor este tipo de patologías. Un trabajo reciente de revisión sistemática y meta-análisis concluyó que el tratamiento quirúrgico de estos aneurismas está asociado a un resultado angiográfico superior en comparación con el tratamiento endovascular (95% de oclusión completa en el grupo microquirúrgico VS 68% en el grupo endovascular). Además, no notaron diferencia sustancial en la morbilidad y mortalidad comparando ambos grupos, siendo la morbilidad y mortalidad del 15% y 9% en el grupo microquirúrgico y del 14% y 7% en el grupo endovascular.1 En definitiva, las dos modalidades de tratamiento (microquirúrgica o endovascular) son válidas, y la decisión deberá depender de cada caso puntual y fundamentalmente de la experiencia y disponibilidad en cada centro médico.
Álvaro Campero
Hospital Padilla, S.M. de Tucumán
BIBLIOGRAFÍA
- Petr O, Coufalová L, Rehwald R, Glodny B, Benes V: Safety and efficacy of surgical and endovascular treatment for distal anterior cerebral artery aneurysms: a systematic review and meta-analysis. World Neurosurgery (Epub ahead of print).































 Premio video “Dr. José Benaim” Neuropinamar 2016
Premio video “Dr. José Benaim” Neuropinamar 2016







