REV ARGENT NEUROC | VOL. 33, N° 1: 1-XX | 2019
ARTÍCULO ORIGINAL
Anatomia Microquirúrgica y Abordajes al Central Core Cerebral
Premio Junior “Dr. Jorge Shilton”, Neuropinamar 2018
Matias Baldoncini1,2, Maximiliano Zarco1, Julio César Pérez Cruz3, Agustín Conde1, Wellerson Sabat Rodrigues1
1Servicio de Neurocirugía Hospital Petrona V. de Cordero, San Fernando, Bs. As., 2Laboratorio de Neuroanatomía Microquirúrgica –LaNeMic- II Cátedra de Anatomia, Facultad de Medicina Universidad de Buenos Aires. 3Academia de Anatomía, Escuela Superior de Medicina, IPN. Lic. Neurociencias, Facultad de Medicina, UNAM.
Matías Baldoncini
drbaldoncinimatias@gmail.com
RESUMEN
Objetivos: A través del estudio cadavérico dividir al central core cerebral (CCC) en diferentes áreas y proponer para cada sector el abordaje neuroquirurgico correspondiente. Como objetivo secundario analizaremos la anatomía neuroquirúrgico cortical y subcortical del CCC.
Introducción : El CCC es descripto como un bloque que descansa sobre el tronco del encéfalo. Incluye la ínsula, capsula extrema, claustro, capsula externa, núcleo lenticular, capsula interna, núcleo caudado y el tálamo.
Material y Métodos: Se estudiaron 12 hemisferios cerebrales humanos adultos y una cabeza en el –LaNeMic- de la Universidad de Buenos Aires, analizamos 9 casos de patologías neuroquirúrgicas del CCC y dibujos digitales de los abordajes propuestos para cada sector del CCC. Se tomaron fotografías de cada disección y las mediciones obtenidas con calibre digital.
Resultados: Dividimos al CCC en un sector medial, intermedio y lateral; con subdivisiones específicas para el lateral y medial. La proyección lateral del foramen de Monro se encontró en el tercer giro corto de la ínsula con las distancias: MILA: 23,95 mm; MILP: 22,92 mm; SLS: 14,99 mm y SLI: 13,76 mm. Proponemos los siguientes abordajes: abordaje transcalloso homolateral, abordaje transcalloso contralateral, abordaje trans-fisura coroidea, abordaje trans-esplenial, acceso trans-parietal ingresando al surco intraparietal y abordaje trans-silviano.
Discusión: Se deben analizar los estudios preoperatorios del paciente, comprendiendo las lesiones según la ubicación y de ese modo seleccionar el abordaje más preciso y seguro.
Conclusiones: Se provee a través de este trabajo una descripción de los límites y anatomía del CCC, empleando disecciones cerebrales, análisis de casos operados y de medidas útiles para el neurocirujano.
Palabras Claves: Central Core Cerebral, Abordajes Neuroquirúrgico, Neuroanatomía, Microcirugía
ABSTRACT
Objectives: Through the cadaveric study, we divide the cerebral central core (CCC) in different areas and propose the corresponding neurosurgical approach for each sector. As a secondary objective, we will analyze the cortical and subcortical microsurgical anatomy of the CCC.
Introduction: The CCC is described as a block that rests on the trunk of the brain. It includes the insula, extreme capsule, claustro, external capsule, lenticular nucleus, internal capsule, caudate nucleusand thalamus.
Material and Methods: We studied 12 adult human brain hemispheres and one head in the -LaNeMic- of the University of Buenos Aires, analyzed 9 cases of CCC neurosurgical pathologies and digital drawings of the approaches proposed for each sector of the CCC. Photographs of each dissection and measurements obtained with digital caliber were taken.
Results: We divide the CCC into a medial, intermediate and lateral sector; with specific subdivisions for the lateral and medial. The lateral projection of the foramen of Monro was found in the third short gyri of the insula with the distances: MILA: 23.95mm; MILP: 22.92mm; SLS: 14.99mm and SLI: 13.76mm. We propose the following approaches: ipsilateral transcallosal approach, contralateral transcallosal approach, choroidal trans-fissure approach, trans-splennial approach, trans-parietal access entering the intraparietal sulcus, and trans-silvian approach.
Discussion: The preoperative studies of the patient should be analyzed, understanding the lesions according to the location and in this way selecting the most accurate and safe approach.
Conclusions: A description of the limits and anatomy of the CCC is provided through this work, using brain dissections, analysis of operated cases and useful measurements for the neurosurgeon.
Keywords: Cerebral Central Core, Neurosurgical Approaches, Neuroanatomy, Microsurgery
OBJETIVOS
El objetivo principal de nuestro trabajo es, a través del estudio cadavérico dividir al central core cerebral en diferentes áreas y proponer para cada sector el abordaje neuroquirúrgico correspondiente, ejemplificando con casos de patología en este sector.
Como objetivo secundario con la disección y dibujos digitales de los especímenes, analizaremos la anatomía microquirúrgica cortical y subcortical de esta región topográfica, proyectando puntos profundos en la superficie con sus respectivas mediciones, analizando las estructuras vasculares y los fascículos cerebrales que discurren en el central core cerebral.
INTRODUCCIÓN
El central core cerebral es un área topográfica localizada entre la cisterna silviana hacia lateral, el ventrículo lateral y tercer ventrículo hacia medial. Es descripto como un bloque que descansa sobre el tronco del encéfalo. Incluye la corteza insular, cápsula extrema, claustro, capsula externa, núcleo lenticular, capsula interna, núcleo caudado y el tálamo.
Adicionalmente se encuentra rodeado por un grupo de fibras de asociación cortas y largas, fibras comisuras y de proyección. Esta sustancia blanca localizada entre los surco periinsulares y ventrículo lateral es conocida como istmo cerebral11. Conecta funcionalmente los núcleos del central core con el resto del hemisferio, así mismo separa anatómicamente la cisterna silviana del sistema ventricular. Siendo morfológicamente el centro del cerebro, integra diversos tipos de información sensitiva, motora, cognitiva y emocional. Son pocos autores2,4,5 que reconocen al central core como una región distinta en el cerebro e importante a la hora de planificar su acceso. Desde un punto de vista estrictamente neuroquirúrgico, es útil su diferenciación ya que contiene estructuras elocuentes, de localización profunda, con relaciones cisternales y ventriculares complejas. Es por esto que dividimos al central core cerebral, proponiendo los diferentes abordajes neuroquirúrgicos hacia cada sector para patologías ubicadas dentro de esta importante región anatómica.
MATERIAL Y MÉTODOS
La anatomía cortical y subcortical del central core cerebral fue estudiada en 12 hemisferios cerebrales humanos adultos en el Laboratorio de Neuroanatomía Microquirúrgica –LaNeMic- de la II cátedra de anatomía de la Universidad de Buenos Aires. En dos hemisferios cerebrales se realizaron cortes axiales y coronales, luego se realizó tinción cerebral con técnica de Mulligam21. Los restantes hemisferios fueron fijados en formol al 10% durante un mes y luego congelados durante 30 días más, esto siguiendo las guías de Ludwing & Klingler13 y otros autores26. Es a través de esta técnica que se permite la expansión del agua que existe entre los fascículos cerebrales formando cristales de hielo, facilitando la disección posteriormente.
Se utilizó una cabeza humana, previamente inyectada con silicona roja y azul y fijados con solución acuosa de formaldehído diluida al 10% durante 30 días, luego de realizar la craneotomía se congeló durante un mes, permitiendo combinar la coloración de los vasos del central core y la disección de los núcleos y fascículos que lo constituyen. Siguiendo la técnica propuesta por Carvalhal Ribas et al.4, en los 12 hemisferios se obtuvieron datos morfométricos, transfixiando con alfileres desde la cara medial a través del foramen de Monro para analizar la proyección de este sobre la superficie insular. Luego de obtener la proyección lateral del foramen de Monro (PLFM), se midió la distancia desde este punto hacia el surco limitante superior e inferior de la ínsula; finalmente se trazaron dos planos coronales delimitando el borde anterior y posterior del núcleo lenticular, denominándoles margen ínsula lenticular anterior y posterior respectivamente. Todas las mediciones fueron obtenidas de modo manual sobre cada espécimen con el uso de un calibre digital.
Para realizar las disecciones se emplearon dos microscopios de magnificación de 6X, 10X y 40X, instrumental romo y elementos de diéresis: tijeras de microcirugía curvas y rectas, micro-pinzas rectas y decolador modelo Penfield n7 recto y curvo, espátulas de madera y cerebrales, rectas y curvas. Las fotografías adjuntas se efectuaron con trípode y fueron tomadas con una cámara Nikon® D7200 con objetivo Micro Nikon® 40 mm F2.8 y flash anular. Esta fue configurada empleando un diafragma variable, velocidad de obturación 100, ISO 250, flash anular 1/128.
Finalmente, proponemos las diferentes estrategias de abordajes neuroquirúrgicos para patologías del central core cerebral según la división topográfica propuesta, luego de realizarlos en cadáveres en la Universidad de Buenos Aires La.Ne.Mic. y con casos del servicio de Neurocirugía del Hospital P.V. de Cordero de San Fernando.
Para completar nuestro trabajo de investigación incorporamos dibujos digitales realizados específicamente para este artículo por la Srta. Evelin Nieva, para destacar la anatomía de la región y división microquirúrgica a través de los abordajes craneales.
RESULTADOS
Anatomía del Central Core Cerebral
La cara lateral del central core cerebral (CCC) corresponde a la superficie insular que se encuentra en la profundidad de la cisterna silviana al retraer los opérculos frontoparietal y temporal. La superficie insular está rodeada por el surco circular compuesto por un surco limitante anterior, superior e inferior. El surco circular se interrumpe en el borde antero inferior de la superficie insular por el limen de la ínsula que presenta forma de C, el mismo posee un punto superior e inferior4,8,17,22,25,30,31.
El punto superior del limen se une al surco limitante anterior en el lóbulo frontal llamándose por E. C. Ribas & Col. ¨punto frontal del limen¨4. El punto inferior se une al surco limitante inferior en el lóbulo temporal y se refiere como "punto temporal del limen"4.
El surco limitante anterior se extiende desde el punto frontal del limen hasta el punto en el cual se cruza con el surco limitante superior, al cual se refiere como punto insular anterior, coincidiendo en la superficie de la fisura silviana con el punto silviano anterior. El surco limitante superior se continúa hacia el borde posterior de la ínsula llamado punto insular posterior4,8 en el cual se une con el surco limitante inferior. El surco limitante inferior se extiende desde el punto insular posterior al punto del limen temporal.
La cara medial está limitada inferiormente por el surco hipotalámico, anteriormente por la cabeza del núcleo caudado y superiormente por el cuerpo del núcleo caudado, atravesando en su trayecto el área septal, del fórnix, tercer ventrículo, asta frotal y cuerpo del ventrículo lateral.
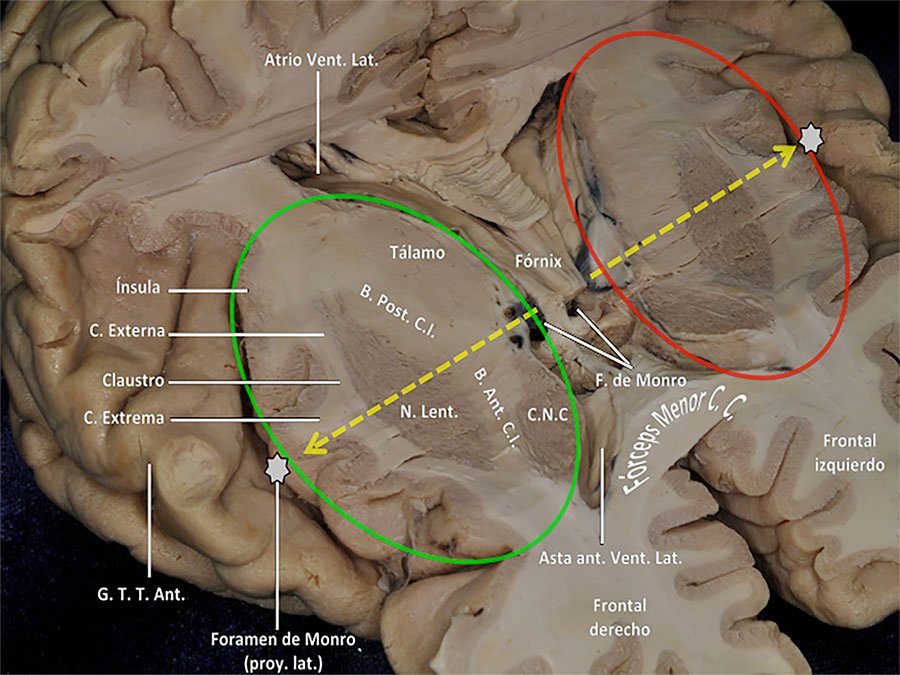
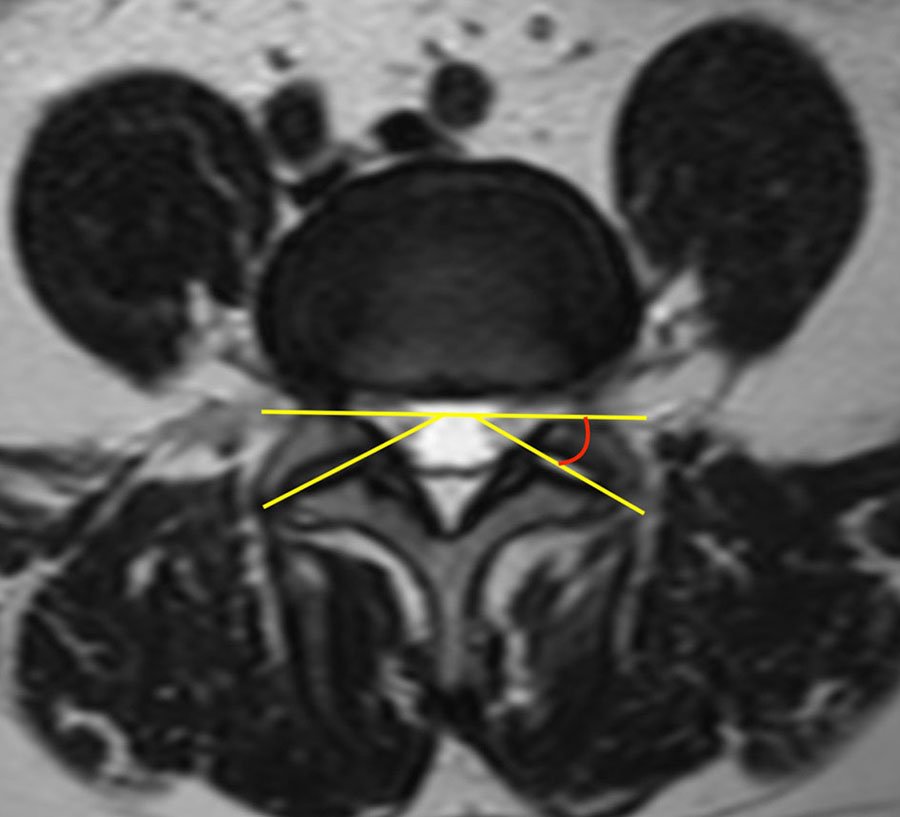
Figura 1: Se observa un corte axial a nivel frontoparietal que atraviesa ambos central core cerebrales en el punto del foramen de Monro, se graficó con flechas amarillas la proyección del foramen sobre la superficie insular. En elipse verde se delimita el central core derecho, en rojo el izquierdo. Por delante y detrás del núcleo lenticular la cápsula extrema, externa e interna se continúan sin plano de demarcación, por este motivo se realizaron las mediciones desde estos márgenes a la proyección del foramen de Monro.
La cara anterior es un plano imaginario que se extiende desde el surco limitante anterior pasando a través del borde anterior de la cabeza del núcleo caudado y finaliza en el asta anterior del ventrículo lateral superiormente y en el borde anterior de la región septal inferiormente, como puede observarse en las figuras 1 y 2. El borde superior se encuentra representado por un plano que conecta el surco limítate superior a nivel del cuerpo y atrio del ventrículo lateral, justo por encima del cuerpo del núcleo caudado.
El borde posterior del central core cerebral es una línea que une el punto insular posterior al borde posterior del núcleo pulvinar atravesando el borde anterior del atrio del ventrículo lateral4. El borde inferior del central core está representado por un plano que se dirige medialmente conectando el surco limitante inferior de la ínsula al atrio y al cuerno temporal del ventrículo lateral.
Estructuras laterales del Central Core Cerebral
La ínsula es de forma triangular con el ápex dirigido de manera anterior e inferior hacia el limen insular, un ligero relieve de corteza que cubre el fascículo uncinado; se encuentra rodeada por el surco circular que se divide en tres bordes: anterior, superior e inferior6,24,29,36. El borde anterior se localiza en la profundidad de la pars triangularis del giro frontal inferior; el borde superior separa la ínsula de los lóbulos frontal y parietal; finalmente el borde inferior separa la ínsula del lóbulo temporal.

Figura 2: A) Se observa un corte axial por arriba del foramen de Monro, donde se ha teñido con técnica de Mulligam para resaltar en azul las estructuras grises del central core cerebral (CCC). En círculo verde se demarca el CCC derecho visto desde arriba con sus estructuras constitutivas. En círculo magenta señalando el surco limitante anterior de la ínsula. Vale destacar que en esta sección se pueden identificar los límites anterior y posterior del CCC4. B) Corte coronal del hemisferio cerebral derecho a nivel del tálamo, en círculo rojo señalando el surco limitante superior de la ínsula y en amarillo el inferior.
Los surcos y giros de la ínsula se dirigen de manera postero superior en forma radiada desde el apex a nivel del limen insular36. El surco central de la ínsula es un surco relativamente constante que se extiende de inferior a superior y de anterior a posterior, prácticamente paralelo a surco central en la convexidad. El mismo divide la ínsula en un lóbulo anterior formado por giros insulares cortos y un lóbulo posterior formado por giros insulares largos, anterior y posterior29.
Por debajo de la corteza de la ínsula se encuentra un grupo delgado de fibras cortas de asociación llamado cápsula extrema, que conecta los giros insulares adyacentes entre sí y se proyectan en la profundidad del surco limitante superior e inferior a las áreas operculares18,29,32.
Retirando estas fibras delgadas nos encontramos con el claustro y cápsula externa, ambos divididos en una porción ventral y dorsal. La capsula externa dorsal está formado por fibras de proyección claustrocorticales que conectan el claustro y la corteza entre corteza motora suplementaria anteriormente y porción posterior del lóbulo parietal posteriormente. La cápsula externa vental se encuentra formada por el fascículo fronto occipital inferior por arriba y fascículo uncinado por debajo. El claustro dorsal se localiza entre la capsula extrema y externa. El claustro ventral se encuentra formado por islotes de sustancia gris interpuesto en la capsula externa ventral que se extiende lateralmente a la amígdala.
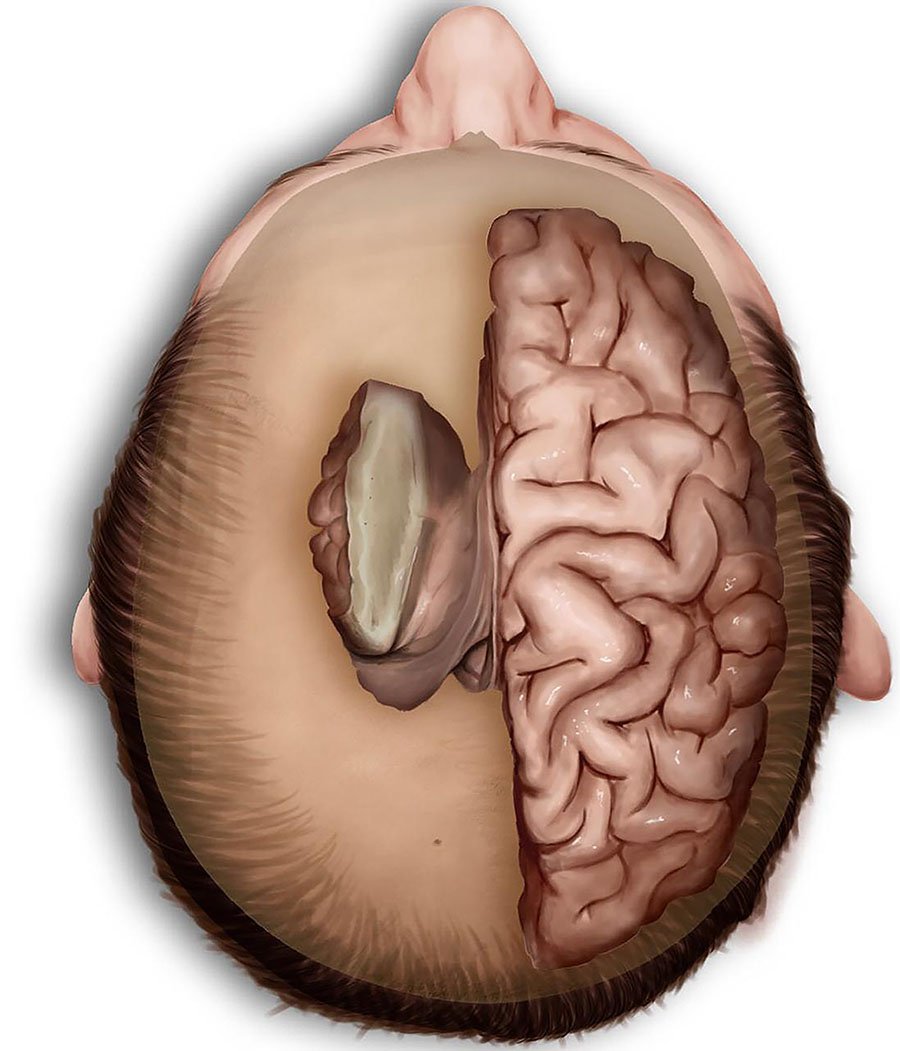
Figura 3: Ilustración artística y representación gráfica del central core cerebral (CCC) izquierdo, se destaca la superficie ventricular del núcleo caudado, superficie ventricular del tálamo izquierdo y el fórnix cubriendo la superficie dorsal del tálamo, formando de tal manera la fisura coroidea. Esta fisura divide al segmento medial del CCC en un sector ventricular y otro cisternal. El sector ventricular a su vez está relacionado con el asta frontal, cuerpo y atrio del ventrículo lateral y, además con la superficie talámica del tercer ventrículo. Es esta división del central core cerebral medial la cual proponemos ya que permite clasificarlo en relación a los diferentes abordajes para accesos a la patología neuroquirúrgica de esta zona.
El fascículo uncinado son fibras de asociación que conectan el lóbulo frontal y temporal. Se localiza profundo al limen de la ínsula asumiendo la misma morfología de "C". Se encuentra en la porción inferior del surco limitante anterior y la porción anterior del surco limitante inferior.
El fascículo fronto occipital inferior conecta los giros frontales superior y medio a los lóbulos temporal, pariental y occipital. Se relaciona inmediatamente superior al fascículo uncinado y posee una porción cóncava que engloba la superficie inferior del núcleo putamen.
El núcleo lenticular se encuentra situado entre la capsula interna y capsula externa. Es dividido en tres segmentos por dos capas de sustancia blanca, la lámina medular medial y lateral32,33. El segmento lateral, el putamen, es el más prominente de los tres. Los dos segmentos remanentes forman el globo pálido. El putamen presenta un color más oscuro y es de mayor tamaño respecto al globo pálido; el globo pálido presenta mayor consistencia y una apariencia más clara debido a la mayor cantidad de fibras que discurren a su través.
En una sección coronal a través de los hemisferios cerebrales (fig. 2B) el núcleo lenticular tiene una forma triangular y presenta tres caras (lateral, superomedial e inferior). La superficie lateral se separa de la corteza insular por una capa de materia blanca que a su vez se subdivide en dos por una fina capa de sustancia gris, el claustro, en cápsula extrema y cápsula externa. La superficie superomedial corresponde a la cápsula interna y en su porción anterior posee un puente de sustancia gris que se conecta con la cabeza del núcleo caudado, llamándose este segmento cuerpo estriado. La superficie inferior se relaciona con la comisura anterior y se separa de la asta temporal del ventrículo lateral a través de una capa de tejido neural donde se reconoce la cola del núcleo caudado4,33.
La comisura anterior, es un fascículo de conexión interhemisférica que atraviesa la superficie ventral del central core cerebral y en este sector forma parte del mismo, conectando principalmente los lóbulos temporales. Cuando atraviesa la línea media se relaciona con la sustancia perforada anterior y luego se divide en una extensión ventral y en relación con el surco olfatorio y una extensión lateral directamente al lóbulo temporal. La extensión lateral está localizada en el canal de Gatriolet formado por la superficie anterior del globo pálido.
La cápsula externa y claustro se encuentra dividida en una porción ventral y dorsal. La cápsula externa dorsal está formado por fibras de proyección claustrocorticales que conectan el claustro y la corteza entre corteza motora suplementaria anteriormente y porción posterior del lóbulo parietal posteriormente. La capsula externa vental se encuentra formada por el fascículo fronto occipital inferior por arriba y fascículo uncinado por debajo; hacia medial hemos encontrado además un pequeño grupo de fibras dependientes de la comisura anterior que se dirigen en sentido anteroposterior hacia la región parietal. El claustro dorsal se localiza entre la cápsula extrema y externa. El claustro ventral se encuentra formado por islotes de sustancia gris interpuesto en la capsula externa ventral que se extiende lateralmente a la amigdala33.
Estructuras intermedias del Central Core Cerebral
La cápsula interna representa las fibras de proyección localizadas entre el núcleo lenticular hacia lateral; caudado y tálamo hacia medial. Se continúa superiormente con la corona radiada, e inferiormente con los pedúnculos cerebrales del tronco encefálico. En un plano axial través de los hemisferios cerebrales, como se observa en las figuras 1 y 2A, la cápsula interna presenta una forma de "V" con el vértice hacia medial relacionada directamente con el foramen de Monro y por ende, la división entre asta frontal y porción central del ventrículo lateral.
La misma se divide en cinco porciones: brazo anterior, entre la cabeza del núcleo caudado y el núcleo lenticular, una rodilla en directa relación con el foramen de Monro y un brazo posterior entre el tálamo y el núcleo lenticular, una porción retrolenticular por detrás del núcleo lenticular y por último una porción sublenticular por debajo del mismo.

Figura 4: A) Primer paso en la disección, se retira la calota craneal, luego la corteza de la superficie lateral del hemisferio cerebral izquierdo, para exponer el FLS: fascículo longitudinal superior con su pars arcuata, en íntima relación con el surco limitante superior e inferior de la ínsula. Se observa la ACM: Arteria Cerebral media. B) Fotografía a mayor aumento localizada sobre el lóbulo de la ínsula izquierda. LI: límen de la ínsula, SLA-SLS-SLI: surcos limitantes anterior, superior e inferior de la ínsula, de color verde, amarillo y azul respectivamente. Señalados en puntos blancos. PFL: punto frontal del límen PIA: punto insular anterior PIP: punto insular posterior PTL: punto temporal del límen. Con un punto color magenta se demarca la PLFM: proyección lateral del forámen de Monro, por delante y detrás del mismo en líneas blancas en sentido coronal proyectando los márgenes ínsula lenticular anterior y posterior. C) Luego de retirar la corteza de los giros cortos y largos de la ínsula, se observa una delgada capa de fibras llamada cápsula extrema, más gruesa en los puntos donde se encontraban previamente los giros insulares, más delgada en el sitio de los surcos se la ínsula. D) Por debajo de la cápsula extrema nos encontramos con una capa delgada de sustancia gris llamada claustro y debajo del mismo un grupo de fibras llamada cápsula externa; ambos de dividen en un sector dorsal y otro ventral. En el sector más anterior de la superficie externa insular y, por debajo de la corteza del límen encontramos un grupo de fibras de asociación largas que hacia frontal y temporal se dividen en FU: fascículo unciforme y FOF: fronto occipital inferior. En este paso de la disección se conservan los surcos limitantes de la ínsula, ya que el central core se encuentra desarrollado dentro de los mismos. Inyectado con silicona roja se observa la arteria cerebral media con sus ramos superior e inferior. Este último relacionado con el surco limitante inferior y el ramo superior brida sus ramos M2 sobre la superficie insular, relacionados directamente con el sector superficial del central core lateral. E) Se procedió a retirar la cápsula externa, para descubrir la superficie lateral del NL: núcleo lenticular, el cual se constituye como un escudo externo de sustancia gris que protege la cápsula interna. Tras retirar parte del putámen y globo pálido se identifican las Art. Lent. Est. Lat.: arterias lenticuloestriadas laterales y medial a las mismas las fibras de orientación cefalocaudal de la C. Int: cápsula interna, la cual se extiende más allá de los márgenes anterior y posterior del núcleo lenticular. F) Último paso de la disección del central core desde lateral, donde se destaca la presencia de la cápsula interna con su brazo anterior, posterior y rodilla, demarcada de modo ovoideo por la morfología que le imprime la cara medial del núcleo lenticular. Un dato anatómico y microquirúrgico importante es que no existe una demarcación entre las cápsulas extrema, externa e interna en la periferia del núcleo lenticular. Por esto realizamos las mediciones en el plano coronal del límite anterior y posterior del mismo, representado en líneas discontinuas, denominándolos: margen ínsulo lenticular anterior y posterior.
Estructuras mediales del Central Core Cerebral
El tálamo es una estructura de forma ovoide situada por encima del mesencéfalo, posee una superficie medial, lateral, superior , inferior, anterior y posterior. La superficie lateral es convexa y adherida al núcleo caudado superiormente y al segmento posterior de la capsula interna inferiormente. La superficie medial posee una superficie cubierta de ependimo llamada superficie ventricular y una superficie extraventricular o cisternal, relacionada con la cisterna cuadrigeminal. Forma la pared lateral del ventrículo lateral en sus dos tercios anteriores y se relaciona con el coliculo superior en su tercio posterior. La superficie superior se divide, por la estría medular talámica, en dos mitades; medial y lateral. La mitad lateral se relaciona con el núcleo caudado y constituye el piso del cuerpo lateral del ventrículo lateral, la mitad medial se encuentra relacionada a la tela coroidea y el fórnix; mientras que la superficie inferior se recuesta sobre el mesencéfalo. El borde posterior representado por el núcleo del Pulvinar, es subdividido por la fisura coroidea en un segmento medial o cuadrigeminal y lateral o ventricular17,25,30, esto muy importante ya que permite dividir este sector según el abordaje quirúrgico a emplear. El borde anterior se divide en dos mitades medial y lateral, la mitad lateral se relaciona con la cabeza del núcleo caudado y la mitad medial forma el límite posterior del forámen de Monro. El núcleo caudado se divide en una cabeza, cuerpo y cola6,8,25. La cabeza se localiza en el aspecto lateral del borde anterior del tálamo, el cuerpo se ubica en la superficie superior del tálamo. El fórnix se encuentra formado por fibras hipocampomamilares que se originan en el hipocampo, subiculo y giro dentado del lóbulo temporal, pasa posteriormente para transformarse en la crura del fornix25. Ambas cruras se unen en la confluencia del atrio con el cuerpo de ventrículo lateral para formar el cuerpo del fórnix el cual corre anteriormente a través del borde superomedial del tálamo, hasta el borde anterior del mismo, punto en el cual se divide en dos columnas que se curvan para formar el limite anterior del foramen de Monro. Esta estructura se relaciona con el ventrículo lateral. El cuerpo del fórnix se localiza en la porción medial del cuerpo del ventrículo lateral, la crura del fórnix se encuentran en el borde medial del atrio; y la fimbria del fórnix se encuentran en la porción medial del cuerno temporal.
La fisura coroidea es una hendidura entre el tálamo y el fórnix a lo largo de la cual el plexo coroideo a nivel de los ventrículos laterales se adhiere y a través de la cual se podría exponer la arteria coroidea anterior y postero medial25. La misma presenta una forma de "C" que se extiende desde el foramen de Monro, a través del cuerpo, atrio y por último al asta temporal del ventrículo lateral; por lo tanto esta fisura se extiende alrededor de las superficies inferior, superior y posterior del tálamo. El borde lateral del fórnix forma el borde medial de la fisura coroidea y el tálamo el borde lateral de la fisura coroidea, a través de las tenías del fórnix y talámica respectivamente25. La misma puede ser dividida en un cuerpo, entre el cuerpo del fórnix y el tálamo, una porción atrial entre las cruras del fórnix y el núcleo pulvinar del tálamo y una porción temporal entre la fimbria del fórnix y la estría terminalis (o el surco tálamoestriado) en la cara ventral del tálamo. Abriendo la porción del cuerpo se expone el tercer ventrículo, la porción atrial la cisterna cuadrigeminal y la porción temporal expone la cisterna ambient25,35.
Mediciones del Central Core Cerebral
Sobre los 12 hemisferios cerebrales se demarcó la proyección lateral del forámen de Monro (PLFM), para luego medir las distancias entre este punto y los margenes ínsulo lenticular anterior (MILA) y posterior (MILP); además la distancia entre el PLFM y los surcos limitantes superior (SLS) e inferior (SLI) de la ínsula, obteniendo los siguientes resultados en la Tabla 1:
Tabla 1: Tabla con las mediciones en milímetros de las distancias desde la proyección lateral del foramen de Monro hacia el surco limitante superior e inferior y hacia los márgenes ínsulo lenticular anterior y posterior.
|
Hemisferios
|
PLFM-SLS
|
PLFM-SLI
|
PLFM-MILA
|
PLFM-MILP
|
|
Hemisferio 1
|
20,61 mm
|
14 mm
|
20,59 mm
|
21,49 mm
|
|
Hemisferio 2
|
17,78 mm
|
12,53 mm
|
23,68 mm
|
20,79 mm
|
|
Hemisferio 3
|
11,62 mm
|
14 mm
|
22,19 mm
|
19,81 mm
|
|
Hemisferio 4
|
16,35 mm
|
13,53 mm
|
21,98 mm
|
24,60 m
|
|
Hemisferio 5
|
11,82 mm
|
14 mm
|
24,20 mm
|
26,64 mm
|
|
Hemisferio 6
|
16,35 mm
|
13,53 mm
|
28,65 mm
|
24,20 mm
|
|
Hemisferio 7
|
11,82 mm
|
9,88 mm
|
27,77 mm
|
23,15 mm
|
|
Hemisferio 8
|
10,60 mm
|
10,90 mm
|
27,74 mm
|
22,53 mm
|
|
Hemisferio 9
|
10,50 mm
|
14,39 mm
|
22,85 mm
|
18,37 mm
|
|
Hemisferio 10
|
18,79 mm
|
20,81 mm
|
21,79 mm
|
23 mm
|
|
Hemisferio 11
|
17,67 mm
|
12,63 mm
|
24,68 mm
|
27,33 mm
|
|
Hemisferio 12
|
16 mm
|
15 mm
|
21,35 mm
|
23,22 mm
|
|
Promedios
|
14,99 mm
|
13,76 mm
|
23,95 mm
|
22,92 mm
|
Subdivisiones del central Core Cerebral
Con fines neuroquirúrgicos se han realizado divisiones del central core cerebral en general o en particular en gliomas insulares14,15,19,37 o para cavernomas localizados a nivel del tálamo20. Sin embargo, no existen trabajos que presenten los diferentes abordajes neuroquirúrgicos para el acceso al CCC y a partir de los mismos dividir al CCC en diferentes regiones. Por lo que hemos dividido al central core cerebral en un sector medial, intermedio y lateral.

Figura 5: Representación en disecciones de modo gráfico de lesiones en el CCC según la clasificación propuesta. A) Apertura de fisura silviana donde se observa la superficie insular, CCLA – CCLM – CCLP: Central Core Lateral Anterior, Medio y Posterior, respectivamente. B) Corte axial sobre los ventrículos laterales donde se observa la superficie dorsal del CCC medial. Relacionado con la asta anterior del ventrículo se encuentra la cabeza del núcleo caudado y lo dividimos en un sector medial y otro lateral. CAM – CAL: Caudado anterior medial y lateral. En la porción central9,17 o cuerpo del ventrículo lateral se encuentra el tálamo hacia medial y cuerpo del núcleo caudado hacia lateral. Proponemos la división en TAM: Tálamo anterior medial, correspondiendo a la superficie dorsal del tálamo en la proximidad de la fisura coroidea. TAL: Tálamo anterior lateral, la superficie relacionada con el cuerpo del núcleo caudado (NC) y, finalmente; CM: Caudado medio, corresponde al cuerpo del NC. TPL: Tálamo posterior lateral, corresponde a la superficie pulvinar ventricular (atrio) y CP: Caudado posterior, siendo la cola del NC a nivel atrial. C. Corte sagital del encéfalo, observando al CCC desde medial. TPM: Tálamo posterior medial, corresponde a la superficie del pulvinar medial a la fisura coroidea, en relación a la cisterna cuadrigeminal. T3V: Tálamo en III ventrículo, se extiende desde la fisura coroidea hasta el surco hipotalámico de la superficie ventricular.
Las estructuras mediales incluyen el tálamo y núcleo caudado, los componentes laterales abarcan putámen, globo pálido, capsula externa, claustro, capsula extrema, corteza insular, comisura anterior, fascículo uncinado y el fascículo frontooccipital inferior. Quedando como elemento intermedio y divisorio la cápsula interna con su brazo anterior, posterior y rodilla que coincide topográficamente con el foramen de Monro.
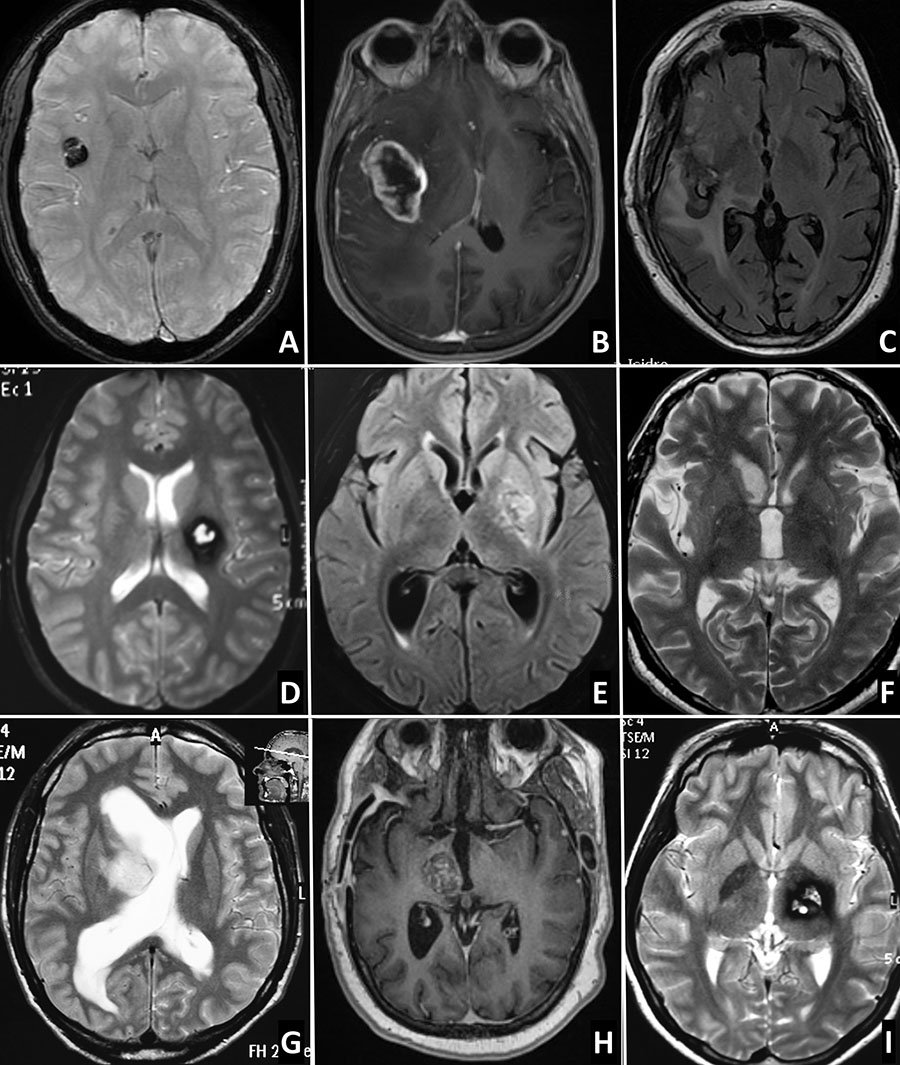
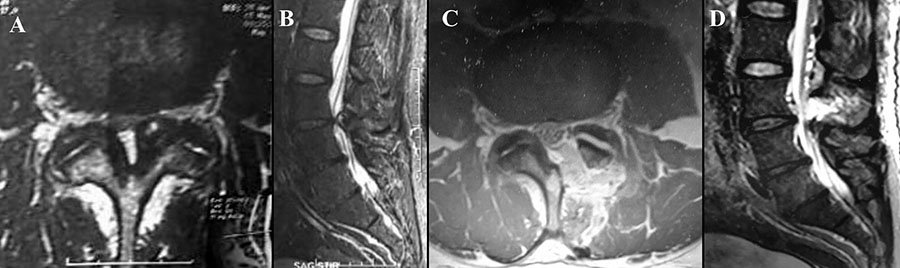
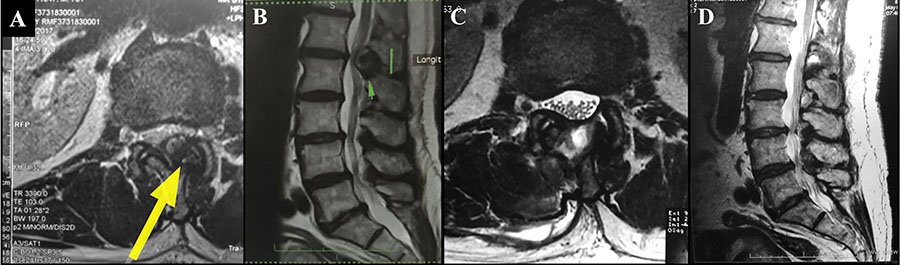
Figura 6: Se muestran RM de pacientes con patología del Central Core Cerebral. A) Cavernoma a nivel de ínsula derecha y cápsula extrema, con halo de hemosiderina que se extiende hasta claustro, se encuentra proyectado en el punto lateral del foramen de Monro. B) Glioblastoma Multiforme con extenso compromiso insular derecho. C) Astrocitoma anaplásico insular posterior derecho, localizado por detrás del plano lentículo insular posterior, llegando en profundidad hasta capsula externa. D) Cavernoma lenticular izquierdo, con halo de hemosideina que se extiende hasta brazo posterior de cápsula interna. E) Glioma de bajo grado lenticular izquierdo. F) Subependimoma de cabeza de núcleo caudado derecho, localizado medialmente. G) Glioblastoma localizado a nivel del cuerpo del núcleo caudado derecho. H) Cavernoma talámico derecho con expresión pial a nivel pulvinar atrial. I.)Cavernoma talámico izquierdo con halo de hemosiderina en relación con cápsula interna.
Se proponen 2 subdivisiones del central core lateral, una de ellas a partir de un plano coronal que pasa por la proyección lateral del foramen de Monro y otro plano axial a través del mismo. De este modo se divide en 4 sectores: anterosuperior, posterosuperior, posteroinferior y anteroinferior; los cuales fueran divididos en zonas I, II, III y IV por Nader Sanai & Col.14 respectivamente. La segunda subdivisión que proponemos es a través de dos líneas coronales que demarcan la proyección sobre la corteza de la ínsula de los bordes anterior y posterior del núcleo lenticular. A estos planos los hemos designado como: margen insulo-lenticular anterior y posterior, como puede verse en la fig. 4 A y B. Por lo tanto, delimitamos al CCC lateral en un sector anterior (CCLA), medio (CCLM) y posterior (CCLP), siendo el segmento medio el más seguro cuando se abordan patologías profundas a la corteza insular ya que en el segmento anterior y posterior las capsulas extrema, externa e interna no presentan límite de separación entre ellas.
Dividimos al central core medial en relación a los sectores del ventrículo lateral y tercer ventrículo con los que se relaciona. En la asta anterior del ventrículo lateral se encuentra la cabeza del núcleo caudado y lo dividimos en un sector medial y otro lateral; caudado anterior medial (CAM) y lateral (CAL). La porción central8,29 o cuerpo del ventrículo lateral se encuentra el tálamo hacia medial y cuerpo del núcleo caudado hacia lateral; para lo cual proponemos la división en: tálamo anterior medial (TAM), correspondiendo a la superficie dorsal del tálamo en la proximidad de la fisura coroidea y tálamo anterior lateral (TAL) en relación con el núcleo caudado, lateral a la estría medular talámica. Finalmente, encontramos al sector caudado medio (CM), corresponde a la cola del núcleo caudado.
La superficie posterior del tálamo, se encuentra dividida por la fisura coroidea en un segmento intraventricular en el atrio al cual denominamos tálamo posterior lateral (TPL) y un segmento extraventricular medial o cisternal, en relación con la cisterna cuadrigeminal: tálamo posterior medial (TPM). El último sector del CCC medial lo constituye la superficie talámica en relación al tercer ventrículo: T3V: tálamo en III ventrículo, se extiende desde la fisura coroidea hasta el surco hipotalámico de la superficie ventricular.
Abordajes Neuroquirúrgicos al Central Core Cerebral
Como anteriormente se mencionó existen trabajos aislados de divisiones del CCC, pero ninguno orientado a los corredores microquirúrgicos. Luego de analizar la anatomía del central core cerebral, proponemos los siguientes abordajes: abordaje transcalloso homolateral, abordaje transcalloso contralateral, abordaje trans-fisura coroidea, abordaje trans-esplenial, acceso trans-parietal ingresando al surco intraparietal y abordaje trans-silviano.
A continuación en la tabla 2 se enumeran las divisiones del central core cerebral con cada abordaje.
Tabla 2: Se resume en la siguiente tabla las subdivisiones propuestas a partir de este trabajo del CCC en la primera columna y en la segunda, los abordajes neuroquirúrgicos propuestos según nuestra experiencia para cada sector.
|
Regiones del Central Core Cerebral
|
Abordajes Neuroquirurgicos al CCC
|
|
Central Core Cerebral Lateral
|
|
|
Central Core Lateral Anterior
|
Abordaje Frontotemporal Transilviano
|
|
Central Core Lateral Medio
|
Abordaje Frontotemporal Transilviano
|
|
Central Core Lateral Posterior
|
Abordaje Frontotemporal Transilviano
|
|
Central Core Cerebral Medial
|
|
|
Caudado Anterior Medial
|
Abordaje Transcalloso Homolateral
|
|
Caudado Anterior Lateral
|
Abordaje Transcalloso Contralateral
|
|
Tálamo Anterior Medial
|
Abordaje Transcalloso Homolateral
|
|
Tálamo Anterior Lateral
|
Abordaje Transcalloso Contralateral
|
|
Caudado Medio
|
Abordaje Transcalloso Contralateral
|
|
Tálamo Posterior Medial
|
Abordaje Transcalloso Transesplenial
|
|
Tálamo Posterior Lateral
|
Abordaje Trans-surco Intraparietal
|
|
Caudado Posterior
|
Abordaje Trans-surco Intraparietal
|
|
Tálamo III Ventrículo
|
Abordaje Trans-fisura Coroidea
|

Figura 7: Ilustraciones artísticas de las vías de abordajes al central core cerebral izquierdo. ATH: abordaje transcalloso homolateral, para acceso a la superficie dorsal y medial intraventricular del tálamo y núcleo caudado. ATC: abordaje transcalloso contralateral, brinda acceso a lesiones laterales del tálamo y caudado. ATFC: abordaje trans-fisura coroidea, para lesiones talámicas en el III ventrículo. ATE: abordaje trans-esplenial, permite el acceso a la superficie cisternal del pulvinar del tálamo. ATP: acceso trans-parietal, ingresando al surco intraparietal se ingresa en el atrio ventricular con visión directa del pulvinar del tálamo intraventricular y cola del n. caudado. ATS: abordaje trans-silviano, accediendo al CCC lateral.
Como se encuentra resumido en la Tabla 2, se provee allí la división en regiones quirúrgicas del CCC y la estrategia en su abordaje para cada caso. Los abordajes frontotemporales (Pterional, Pretemporal, etc.) permiten el acceso a la fisura silviana y tras su disección en sus segmentos esfenoidal y lateral, se expone la superficie lateral del central core. Como se observa en las disecciones de la fig. 4 y se grafica en el dibujo de fig. 7A, la trayectoria de los ramos M2 de la arteria cerebral media deben ser conservados, utilizando el espacio entre ellas para la disección y el acceso a estructuras subcorticales del CCC lateral. Esto último es especialmente importante detrás del plano lentículo insular posterior (distancias en tabla 1) ya que estos ramos arteriales brindan perforantes que atraviesan la corteza insular llegando hasta el brazo posterior de la cápsula interna.


Figura 8: A) Representación artística de abordaje pretemporal con apertura del valle silviano para el acceso a la ínsula en sus sectores anterior, medio y posterior. Es a través de este tipo de abordaje que se puede acceder a operar patologías localizadas en la corteza de la ínsula, claustro, capsulas externa y extrema, fascículo unciforme y frontooccipital. B) Dibujo del abordaje interhemisférico transcalloso para alcanzar al central core relacionado con el ventrículo lateral, tercer ventrículo o cisterna cuadrigeminal a través del acceso transesplenial. Sus variantes son transcalloso homolateral, contralateral, transesplenial y trans fisura coroidea.
En la fig. 8B a través de una representación artística digital se demuestra un abordaje interhemisférico izquierdo, el mismo puede atravesar el cuerpo calloso del lado homolateral o contralateral1,7,9,10, permitiendo acceder al central core medial en relación al ventrículo lateral, tercer ventrículo o cisterna cuadrigeminal en caso del acceso transcalloso posterior a través del esplenio.
Los accesos hacia el pulvinar del tálamo en su sector intraventricular y la cola del núcleo caudado, son aquellos empleados para patología del atrio ventricular. El surco intraparietal se localiza en dirección anteroposterior separando al lóbulo parietal superior del inferior (giro supramarginal y angular) y generalmente transcurre paralelo a la línea media a 2 o 3 centímetros de la fisura interhemisférica. Una vez realizado el acceso se debe retraer suavemente y en algunos casos puede emplearse la asistencia endoscópica para el trabajo microquirúrgico intraventricular sobre el tálamo o cola del núcleo caudado.

Figura 9: Ilustración artística que representa un abordaje parietal a través del surco intraparietal derecho para el acceso al atrio ventricular y a través del mismo a la superficie ependimaria del pulvinar del tálamo. Si bien es una elección transcortical, con este corredor se evita lesionar las fibras geniculocalcarinas y, por otro lado, queda respetada hacia medial las fibras del fascículo del cíngulo. El surco intraparietal se encuentra localizado separando al lóbulo parietal interior del superior y generalmente transcurre paralelo a la línea media a 2 o 3 centímetros del borde medial del hemisferio cerebral. Una vez realizado el acceso se debe retraer suavemente y en algunos casos puede emplearse la asistencia endoscópica para el trabajo microquirúrgico intraventricular sobre el tálamo o cola del núcleo caudado.
Hemos empleado este abordaje para cavernomas pulvinares y subependimomas de la cola del núcleo caudado, ya que el acceso es directo a estos componentes el CCC, como se representa en el dibujo de la figura 9 y en el caso H de la figura 6.
DISCUSIÓN
La subdivisión de los hemisferios cerebrales en lóbulos se realizó en base a los huesos del cráneo con los que se relacionan23, aunque en el año 1809 en su descripción original por Reil se reconoce a la ínsula como un lóbulo distinto4,23. Si comenzamos analizando que la ínsula se comporta como un escudo externo del bloque central5 y que este último se encuentra por encima del tronco encefálico, comprendemos que los abordajes a este sector topográfico son un verdadero desafío. Por otro lado, el CCC incluye numerosas estructuras corticales y subcorticales elocuentes, por este motivo se deben analizar los estudios preoperatorios del paciente, comprendiendo las lesiones según la ubicación y de ese modo seleccionar el abordaje más preciso y seguro.
Para aquellas lesiones con expresión ependimaria en el ventrículo lateral, localizadas lateralmente, el acceso transcalloso contralateral brinda un ángulo de visión mayor1,12 sin necesidad de retracción del giro y fascículo del cíngulo. Si bien algunos autores recomiendan accesos transcorticales al cuerno frontal o cuerpo del ventrículo lateral, nosotros preferimos utilizar el corredor natural que ofrece la fisura interhemisférica y la cisterna pericallosa. Evitando los accesos transcorticales, se disminuyen las probabilidades de crisis comiciales postoperatorias, además de lesionar igualmente fibras del cuerpo calloso, que discurren indefectiblemente por debajo de la corticotomía. El pequeño sector del central core en relación con la superficie dorsal del tercer ventrículo, representado por la superficie medial del tálamo, puede exponerse a la visión del cirujano por un corredor transcalloso o transcortical endoscópico. El acceso transcalloso homolateral, luego de ingresar al cuerpo del ventrículo lateral se debe identificar el plexo coroideo, desplazándolo hacia medial para proceder con la abertura de la fisura coroidea y por debajo de la misma alcanzar la superficie talámica del tercer ventrículo; teniendo como límite el surco hipotalámico. En los casos de pacientes con hidrocefalia, otra opción válida es la realización de una tercer ventriculoscopia accediendo vía trans foramen de Monro al III ventrículo.
El acceso transurcal por el surco intraparietal de la cara lateral del hemisferio nos direcciona hacia el atrio ventricular, sin lesionar fascículos importantes como las radiaciones ópticas, fascículo longitudinal superior y fórceps occipital del cuerpo calloso. Si existiera dificultad en la localización del surco intraparietal, con guía ecográfica se puede determinar la trayectoria al ver por ultrasonido el LCR del atrio ventricular.
CONCLUSIONES
Se provee a través de este trabajo una descripción detallada sobre los límites y anatomía cortical y subcortical del central core, empleando secciones cerebrales, disecciones de fibras y el análisis paso a paso en material cadavérico inyectado con silicona y preparado con técnica de klingler. Se analizan las medidas útiles para el neurocirujano como la proyección del foramen de monro sobre la superficie insular y a partir de este, el plano ínsulo-lenticular anterior y posterior. Con el avance en las técnicas de ultrasonido transcortical, creemos en un futuro poder localizar el foramen de monro a través de ecografía transcortical insular y de este modo poder emplear las medidas obtenidas en nuestro trabajo en pacientes con tumores del central core lateral, disminuyendo la morbilidad postoperatoria.
Creemos útil la división propuesta por propuesta por Carvalhal Ribas et al.4 sobre la división del central core lateral en 4 cuadrantes4, sumándole la delimitación de los bordes anterior y posterior del núcleo lenticular, ya que actúa como un escudo de sustancia gris protegiendo a la cápsula interna. Esta división en 4 cuadrantes a partir de la proyección insular del foramen de Monro, permite orientarnos para los abordajes transilvianos hacia patologías localizadas en el central core cerebral laterales a la capsula interna.
Proponemos una división del central core medial a partir del abordaje neuroquirúrgico a emplear para los accesos a esta región anatómica. Entre ellos se incluyen: Abordaje interhemisférico transcalloso homolateral y contralateral1, transforámen de Monro, transcoroideo, transesplenial y transurcal intraparietal.
El acceso a patologías en esta área implica rutas transcorticales por giros o surcos cerebrales, disecciones cisternales o el acceso primario hacia algún sector de los ventrículos laterales o tercer ventrículo, hasta poder visualizar el CCC. Por ello es importante un correcto posicionamiento del paciente, utilización de técnica microquirúrgica y endoscópica, empleo de neuronavegación o guía estereotáxica con aguja o láser; además del uso de estimulación cortical y subcortical intraoperatoria.
BIBLIOGRAFÍA
- Baldoncini M., González López P. & Col. “Abordaje Interhemisferico Contralateral Transfalcino, Subfalcino y Transcalloso” Rev. Argentina de Neurocirugía vol. 32, N°1: 1-15 2018.
- Brodal A. Neurological anatomy in relation to clinical medicine. 3 Ed. New York: Oxford University Press, 1981.
- Campero A., Ajler P., Emmerich J. “Abordajes neuroquirúrgicos al cerebro y la base del cráneo” Cap. 1 Abordaje interhemisferico transcoroideo. Ed. JOURNAL 2013.
- Eduardo Carvalhal Ribas, MD, PhD, Kaan Yağmurlu, MD, Evandro de Oliveira, MD, PhD, Guilherme Carvalhal Ribas, MD, PhD, and Albert Rhoton Jr., MD, PhD. Microsurgical anatomy of the central core of the brain. J Neurosurg December 22, 2017.
- Guilherme Carvalhal Ribas, Evandro de Oliveira. A insula e o conceito de bloco cerebral central”. Arq Neuropsiquiatr 2007;65(1):92-100.
- Duvernoy, H. (1999). The Human Brain. Vienna: Springer Vienna.
- Ehni G: Comments on Shucart WA, Stein BM: Transcallosal approach to the anterior ventricular system. Neuro- surgery 3:343, 1978
- Federative Committee on Anatomical Terminology: Terminología Anatómica: International Anatomical Terminol- ogy. Stuttgart: Thieme, 1998.
- García Navarro V.- Castillo Velázquez G. “Estrategias y abordajes en neurocirugía craneal” Cap. 14 Apertura del valle silviano, Cap. 23 Abordajes Interhemisfericos. Ed. AMOLCA 2015.
- Kasowski M, Piepmeier JM. “Transcallosal approach for tumors of the lateral and third ventricles”. Neurosurgical focus. June 2001 /vol. 10/ No. 6.
- Christos Koutsarnakis, Faidon Liakos, Evangelia Liouta, Konstantinos Themistoklis, Damianos Sakas, and George Stranjalis. “The cerebral isthmus: fibertract anatomy, functional significance, and surgical considerations” J. Neurosurg September 11, 2015.
- Lawton MT, Golfinos JG, Spetzler RF. “The contralateral transcallosal approach experience with 32 patients”. Neurosurgery 39(4): 729-735, 1996.
- Ludwig E, Klingler J: Atlas cerebri humani. Boston: Little, Brown & Co, 1956.
- Nader Sanai, M.d., Mei-Yin Polley, Ph.d. & Mitchel S. Berger, M.d. “Insular glioma resection: assessment of patient morbidity, survival, and tumor progression” J Neurosurg 112:1–9, 2010.
- Thomas P. Naidich, Eugene Kang, Girish M. Fatterpekar, Bradley N. Delman, S. Humayun Gultekin, David Wolfe, Orlando Ortiz, Indra Yousry, Martin Weismann, and Tarek A.Yousry. “The Insula: Anatomic Study and MR Imaging Display at 1.5 T” AJNR Am J Neuroradiol 25:222–232, February 2004.
- Daniel G. Nehls, Robert F. Spetzler & Col. “Transcallosal Approach to the contralateral Ventricle” Barrow Neurological Institute, Phoenix. J. Neurosurg 62:304-306, 1985.
- Nieuwenhuys R, Voogd J, van Huijzen C: The Human Central Nervous System, ed 4. New York: Springer, 2008.
- R. Nieuenhuys - J. Voogd – C. Van Huijzen The Human Central Nervous Sistem. Ed. Springer Fourth Edition.
- Potts MB, Chang EF, Young WL, Lawton MT: Transsylvian- transinsular approaches to the insula and basal ganglia: operative techniques and results with vascular lesions. Neurosurgery 70:824–834, 2012.
- Rangel Castilla L. Md, and Spetzler R. Md “The 6 thalamic regions: surgical approaches to thalamic cavernous malformations, operative results, and clinical outcomes”. J neurosurg May 29, 2015.
- Refojos, Manuel - Morley, Gabriela - Trindade de Veglia, H. M. Preparación anatómica de encéfalo bovino con fines didácticos. Universidad Nacional del Nordeste. Comunicaciones Científicas y Tecnológicas 2003.
- Ribas GC, de Oliveira E: [The insula and the central core concept.] Arq Neuropsiquiatr 65:92–100, 2007.
- Ribas G.C. “Neuroanatomical basis of behavior: history and recent contributions”. Rev. Bras. Psiquiatr. 29:63–71, 2007.
- Ribas, G. (2010). “The cerebral sulci and gyri”. Neurosurgical Focus, 28(2), p.E2.
- Rhoton AL. The Cerebrum. Neurosurg. 2002;51(1):375-410.
- Rubino, Pablo; Baldoncini, Matías & Conesa, Horacio A. Disección de Sustancia Blanca Cerebral. Importancia para el Entrenamiento Neuroquirúrgico – pág. 130 Revista Argentina de Anatomía Online 2012 (Octubre – Noviembre – Diciembre), Vol. 3, No 4, pp. 97 – 136 ISSN impresa 1853-256x / ISSN online 1852-9348.
- Stein BM: Transcallosal approach to third ventricular tumors, in Schmidek HH, Sweet WH (eds): Current Tech- niques in Operative Neurosurgery. New York: Grune & Stratton, 1977, pp 247-255.
- Tanriover N, Rhoton AL Jr, Kawashima M, Ulm AJ, Yasuda A: “Microsurgical anatomy of the ínsula and the sylvian fissure”. J Neurosurg 100:891–922, 2004.
- Terminología Anatómica internacional, FCAT Comité Federal sobre Terminología Anatómica, Ed. Médica PANAMERICANA, Madrid, España, 2001.
- Testut, L., Latarjet, A. and Latarjet, M. (1988). Tratado de anatomía humana. Barcelona: Salvat.
- Trove. (2017). Atlas of the cerebral sulci / Michio Ono, Stefan Kubik, and Chad D. Abernathey; foreword by M.G. Yasargil.
- Türe U, Yaşargil DC, Al-Mefty O, Yaşargil MG: Topographic anatomy of the insular region. J Neurosurg 90:720–733, 1999.
- Türe U, Yaşargil MG, Allan H. Friedman, M.D., Ossama Al-Mefty, M.D. “Fiber Dissection Technique: Lateral Aspect of the Brain” Neurosurgery, Vol. 47, No. 2, August 2000.
- Türe U, Yaşargil MG, Al-Mefty O, Yaşargil DC: Arteries of the insula. J Neurosurg 92:676–687, 2000.
- Wen HT, Rhoton AL Jr, de Oliveira E: Transchoroidal ap- proach to the third ventricle: an anatomic study of the choroidal ssure and its clinical application. Neurosurgery 42:1205–1219, 1998.
- Yaşargil MG, Krisht AF, Türe U, Al-Mefty O, Yaşargil DCH: Microsurgery of insular gliomas: Part I: surgical anatomy of the Sylvian cistern. Contemp Neurosurg 24:1–8, 2002.
- Yaşargil MG: “Microneurosurgery” Vol IV B, Microneurosurgery of CNS Tumors, Pages: 54-57 Stuttgart: Georg Thieme Verlag, 1996.
- Yaşargil G., M.D., Türe U., M.D. &, Yaşargil D. R.N. “Surgical anatomy of supratentorial midline lesions” Neurosurg Focus 18 (6b):E1, 2005.