Título
Autor
Fecha
Lugar de Realización
Correspondencia
Texto
REV ARGENT NEUROC | VOL. 31, N° 4: 278-286 | 2017
TRABAJO PREMIADO
Cirugía endoscópica de la base del cráneo.
¿Qué reparos han de guiar el procedimiento?
Premio Beca Asociación Argentina de Neurocirugía,
XIV Jornadas Argentinas de Neurocirugía 2017
Román P. Arévalo, Daniel A. Seclen Voscoboinik, Maximiliano A. Nuñez, Eduardo Salas López, Pablo A. Rubino, Miguel Mural
Servicio de Neurocirugía. Hospital Alta Complejidad en Red El Cruce S.A.M.I.C. Buenos Aires, Argentina
RESUMEN
Introducción: El abordaje endonasal endoscópico a la base del cráneo puede alcanzar lesiones ubicadas desde la apófisis crista galli en la fosa cerebral anterior hasta el foramen magnum y la unión atlantoaxoidea, tanto en la línea media como en la región paramediana. Un conocimiento anatómico exhaustivo es mandatorio si se quiere dominar esta técnica en constante desarrollo.
Objetivo: Realizar un análisis anatómico exhaustivo de la anatomía endoscópica de la base del cráneo, desde la fosa craneal anterior hacia la posterior, dejando en claro qué Reparos guían los diferentes abordajes según la fosa craneal a abordar.
Material y método: Reporte técnico, anatómico, de todas aquellas estructuras óseas de la base del cráneo que sean identificables a través de un abordaje endonasal endoscópico. Se trata de un análisis anatómico que combina preparados cadavéricos y secos, junto con imágenes intraoperatorias de pacientes tratados en nuestra institución.
Resultados: Se logró el análisis óseo y sus relaciones con los elementos neurovasculares profundos, tanto en los abordajes endoscópicos en el plano sagital así como coronal, para las tres fosas craneales.
Conclusión: Un buen conocimiento de la anatomía ósea de cada sector de la base del cráneo permite tener un control más certero sobre elementos como la arteria carótida interna o los pares craneales. Se demostró que es posible realizar una correlación anatómica entre los diferentes Reparos observados en cada fosa craneal, con los aspectos neurovasculares más relevantes, dentro del gran conjunto de abordajes que aún dan en llamar “abordaje endoscópico a la base del cráneo”.
Palabras clave: Reparos; Abordaje Endonasal Endoscópico; Plano Coronal; Transpterigoideo
ABSTRACT
Introduction: The endonasal endoscopic approach to the skull base enables surgeons to access lesions from the crista galli to the foramen magnum, and even those in the paramedian skull base. However, extensive anatomical knowledge is indeed required to achieve full familiarity and competence with this endoscopic microsurgical technique.
Purpose: To perform anatomical analysis of endoscopic anatomy, from the anterior to the posterior cranial fossae, particularly identifying the anatomic landmarks that will best guide the procedure, depending on which fossa the surgeon aims to reach.
Materials and Methods: An anatomical and technical review was conducted to identify all anatomic landmarks that could be identified using an endonasal endoscopic approach. This anatomic analysis combined cadaveric dissections and intraoperative photos of patients who underwent surgery within our department.
Results: Full understanding of the osseous landmarks and underlying neurovascular structures was achieved for the three cranial fossae in the sagittal plane and in paramedian locations.
Conclusion: Familiarity with the osseous anatomy of each sector of the skull base allows for more accurate control over structures like the carotid artery and cranial nerves. We found that it is possible to perform anatomical correlations between the different landmarks observed in each cranial fossa, and the most relevant neurovascular features, under the extensive umbrella of techniques covered under the name "endoscopic endonasal approaches to the skull base".
Key words: Landmarks; Endoscopic Endonasal Approach; Coronal Plane; Transpterigoyd
Román P. Arévalo
dr.roman.arevalo@gmail.com
INTRODUCCIÓN
La cirugía endoscópica de la base del cráneo es, quizás, uno de los mayores avances y aportes de las últimas décadas en nuestra especialidad. Entre sus principales aspectos a destacar, se encuentran la posibilidad de visualizar en primer plano las estructuras anatómicas y la patología en cuestión que hemos de tratar. Si a esto adicionamos la posibilidad de utilizar lentes endoscópicas anguladas (30°, 45°, 70°, entre otras), podremos observar de manera panorámica las regiones laterales para lograr una mejor inspección y una eventual resección de un remanente tumoral.
Merece especial atención la gran superficie de la base del cráneo que este abordaje permite alcanzar. Inicialmente, el acceso transesfenoidal fue instituido y “restringido” para la cirugía de las lesiones hipofisarias, pero conforme el avance tecnológico y un conocimiento anatómico más pulido entraron en escena, los abordajes endonasales lograron imponerse para alcanzar regiones sumamente distantes de la base del cráneo; y no solamente en la línea media, sino también regiones alejadas de la misma, extendiéndose notablemente hacia otras estructuras distribuidas por el plano coronal. Para nombrarlo de un modo algo más simple, el abordaje endonasal endoscópico a la base del cráneo puede alcanzar lesiones ubicadas desde la apófisis crista galli en la fosa cerebral anterior hasta el foramen magnum y la unión atlantoaxoidea1,2. A su vez, puede alcanzar regiones distantes a la línea media, como ser el ápex petroso o la fosa infratemporal.
Sin lugar a dudas, la anatomía quirúrgica endoscópica de las fosas nasales y sus comunicaciones y accesos a la base del cráneo, es la mejor aliada para poner todas las citadas ventajas en práctica. Pero el camino desde la narina hacia el adenoma hipofisario o el cordoma de clivus está superpoblado de numerosos “reparos” o reparos anatómicos que nos han de guiar a lo largo del recorrido quirúrgico, diciéndonos qué paso ha de seguir o qué element anatómico noble deberemos hallar en profundidad. Proponemos un estudio completo y sitematizado de esos reparos a lo largo de toda la base del cráneo.
OBJETIVOS
En este reporte, nuestro equipo, integrado en su totalidad por neurocirujanos, se propone realizar un análisis anatómico exhaustivo de la anatomía endoscópica de la base del cráneo, desde la fosa craneal anterior hacia la posterior; teniendo en cuenta no sólo las estructuras de la línea media sino también aquellas ubicadas a sus lados. Se propone “homogeneizar” todo el conocimiento anatómico disponible, el cual es más que inabarcable, en una guía práctica, aplicable y reproducible.
MATERIAL Y MÉTODO
Se llevó a cabo un reporte técnico, anatómico, de todas aquellas estructuras óseas de la base del cráneo que sean identificables a través de un abordaje endonasal endoscópico. En función de ello, se estudian las relaciones fundamentales de cada una de ellas con respecto a los elementos neurovasculares que han de ser preservados a lo largo del procedimiento quirúrgico, y asisten al neurocirujano a la hora de realizar la intervención en cuestión, guiando el recorrido quirúrgico.
Este análisis anatómico se complementa con imágenes intraoperatorias de los procedimientos realizados en nuestra institución. El equipamiento quirúrgico de endoscopía que utilizamos consta de:
- Dos ópticas de la firma Karl Storz Endoscopy® (Tuttlingen, Alemania), de 0 y 45 grados.
- Torre de endoscopía con cámara y grabadora HD de la firma Stryker® (Michigan, Estados Unidos de América).
- Drill de alta velocidad, modelo “Midas Rex Legend” de la firma Medtronic® (Minnesota, Estados Unidos de América).
RESULTADOS
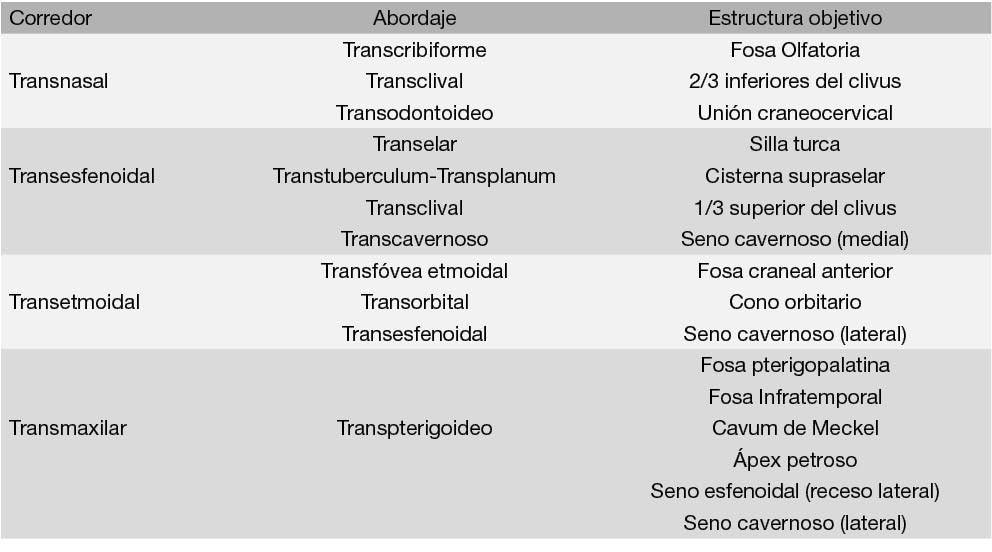
Las fosas nasales constituyen nuestra vía de entrada natural a la hora de tratar endoscópicamente patologías que involucren a la base del cráneo, o bien aquellas que para ser accedidas precisen una osteotomía en la base del cráneo. Dichos accesos son por demás variados y requieren un conocimiento exhaustivo de la anatomía rinal normal. En función del abordaje endoscópico considerado, existen diferentes corredores (o “canales de trabajo”) que han de ser empleados, con diferentes estructuras o regiones “objetivo” en donde se ha de encontrar la patología que hemos de resolver. La Tabla 1 resume las características de los diferentes abordajes endonasales endoscópicos a la base del cráneo3,4,5.
La precedente tabla ilustra, al menos en parte, cuán complejo es el concepto de “abordaje endoscópico a la base del cráneo”. Ello es así debido a que en la base del cráneo existen numerosas estructuras óseas que permiten identificar elementos neurovasculares importantes a ser tenidos en cuenta a la hora de efectuar un procedimiento endonasal endoscópico. Desde este punto de vista endoscópico, se las puede entender como un conjunto de prominencias y recesos que delimitan forámenes, conductos y superficies en toda la base del cráneo. Lo más importante, y quizás la verdadera razón del porqué de este artículo, es que estas prominencias y recesos son la expresión de estructuras del endocráneo en el exocráneo, y generalmente son “antagónicas”, por lo que una prominencia en el endocráneo determina un receso en el exocráneo, y viceversa. La importancia de estas estructuras anatómicas óseas radica en la utilidad de las mismas durante el procedimiento neuroquirúrgico, ya que habitualmente la anatomía normal a la que nos referimos puede estar alterada, o eventualmente podría llegar a ser difícil de reconocer. Según su ubicación estas estructuras pueden ser únicas y de la línea media, o pares y laterales.
Tabla 1: Abordajes endoscópicos a la base del cráneo3-5
Las estructuras óseas a identificar representan accidentes relativamente constantes y que nos orientarán a reconocer a las estructuras neurovasculares subyacentes. Por lo tanto, estos representan verdaderos reparos que nos van a permitir discernir entre los diferentes elementos de la región de la base del cráneo que estamos abordando. Por otro lado, hoy en día resulta casi imposible ignorar la ayuda de la neuronavegación, la cual nos va a asistir a la hora de identificar los mencionados elementos neurovasculares haciendo uso de los diferentes reparos previamente analizados en los estudios preoperatorios, fundamentalmente la TC ventana ósea y la RMN.
Los reparos a los que nos estamos refiriendo son prácticamente incontables, e irán haciéndose evidentes en las diferentes etapas del procedimiento. Los mencionados reparos han de ser estudiados según la fase del procedimiento y su ubicación espacial, a saber:
a. Cavidades Nasales (Etapa Nasal)
b. Corredor Transnasal:
1. Fosa Craneal anterior.
2. Fosa Craneal Posterior.
c. Corredor Transesfenoidal (Etapa Esfenoidal):
1. Fosa craneal Media:
- Línea Media.
- Plano Coronal.
2. Fosa craneal Posterior:
- Línea Media.
- Plano Coronal.
La citada lista es una forma “acotada” de organizar los diferentes reparos en los accesos endoscópicos a la base del cráneo. Sin embargo, y con fines académicos, el orden que llevará el relato será algo diferente, con el objetivo de llevar a cabo una descripción detallada y un orden que sea comprensible para la lectura. Se comenzará con una descripción exhaustiva de la anatomía de las fosas nasales, luego siguiendo con el acceso endonasal a la fosa anterior. Una vez completado ello, se continuará con el corredor transesfenoidal como acceso a la fosa media y posterior (en el plano sagital) para finalmente cerrar el análisis con los reparos o reparos que caracterizan a los diferentes accesos paramedianos (en el plano coronal) de una forma integral.
Etapa nasal
Las cavidades nasales se han convertido en los últimos años en uno de los actores principales en términos de cirugía reconstructiva. Esto se debe a que la mucosa nasal alberga a una intrincada red de suministro vascular pocas veces hallada en otro sector del organismo. Tal es así que son cada vez más los reportes en la literatura sobre colgajos nasoseptales, de la pared lateral o de cornete medio a la hora de reconstruir la base del cráneo6-9. Dicha mucosa, por demás útil hacia el cierre de nuestra intervención, nos “oculta” numerosos accidentes óseos que son de importancia capital a la hora de guiar nuestro procedimiento endoscópico.
La fosa nasal, y sus comunicaciones con las cavidades neumáticas paranasales, con una vía de acceso natural a la base del cráneo (fig. 1). Mediante ellas es posible alcanzar desde la apófisis crista galli hasta el foramen magno y la unión cráneo cervical1,2, e inclusive a numerosas estructuras paramedianas como la fosa infratemporal o el ápex petroso. La fosa nasal (fig. 2) es un órgano osteocartilaginoso, comprendida entre el septum nasal (conformado por el vómer y la lámina perpendicular del etmoides en su porción ósea, y por una porción cartilaginosa anterior) y una compleja pared lateral, integrada por la apófisis ascendente del hueso maxilar, el unguis, la masa lateral del etmoides, y la lámina perpendicular del hueso palatino. Su pared inferior o piso está conformada por lo que se conoce como paladar duro, integrado en sus ¾ anteriores por el hueso maxilar y en ¼ posterior por la lámina horizontal del palatino. Como abertura posterior, se destacan las coanas, las cuales se encuentran limitadas hacia medial por el septum nasal posterior (vómer), hacia lateral por la lámina vertical del hueso palatino, hacia superior por el rostrum del cuerpo esfenoidal, e inferiormente hallaremos la lámina horizontal del palatino (paladar duro).
La etapa nasal (fig. 3) del procedimiento comienza con la elección de la fosa nasal a comenzar. Generalmente se comienza por la derecha, y una vez culminada la fase nasal se diseca la mucosa septal izquierda para conformar el conocido abordaje binostril impuesto por Aldo Stamm10,11. Es fundamental la generación de un corredor nasosinusal amplio (fig. 4) para garantizar el correcto desplazamiento del instrumental, para poder llevar a cabo una disección microquirúrgica delicada hacia el tiempo intradural de nuestro procedimiento.
Es por ello que será de capital importancia reconocer y movilizar una serie de estructuras anatómicas que siempre estarán presentes. Las estructuras anatómicas que deberán ser reconocidas en la etapa nasal se enlistan en la Tabla 2. Pero a su vez, y como ya se comentó, ciertas de estas estructuras se convierten en verdaderos reparos o “reparos” que nos han de “decir” que a través de ellas discurre algún vaso de capital importancia, o bien que a través de ellas obtendremos acceso a determinadas regiones de la base del cráneo, siendo éstas el verdadero objetivo del procedimiento quirúrgico. Los principales reparos que deben ser evaluados y reconocidos en esta etapa son los que se nombran y detallan a continuación.
Cabeza del Cornete Medio y su Inserción
El cornete medio (fig. 5a) es quizás uno de los primeros relieves endonasales que uno identifica al ingresar con la óptica. Es una estructura importante que protruye hacia la cavidad nasal obstruyendo de alguna forma el pasaje de la cámara y el instrumental a través del corredor nasosinusal hacia las estructuras más posteriores. La lateralización del cornete medio (mediante el uso de un disector protegido con algodones embebidos en adrenalina diluida al 1/100000 u oximetazolina)11, permite ampliar este corredor, muchas veces siendo esta maniobra suficiente para abordar algunas lesiones de la base de cráneo, principalmente microadenomas hipofisarios en los que no se requiere una exposición mucho mayor.
El cornete medio es una protrusión del propio etmoides hacia la luz de la cavidad nasal, a diferencia del inferior que es un hueso individualizado en sí mismo. La turbina o cornete medio tiene inserciones tanto en la base craneal anterior a través de la lamela que lo ancla a la masa lateral del etmoides y al aspecto más externo de la lámina cribosa, así como también a la órbita. Estas son relaciones muy importantes a la hora de efectuar un acceso transcriboso (véase más adelante) ya que la porción más superior de la inserción del cornete medio es una suerte de “guía” hacia el techo de las fosas nasales y la pared posterior del seno frontal (lo que se denomina receso frontal). Estas inserciones deben ser bien identificadas, ya que en casos de requerir un corredor nasosinusal aún más amplio, se deberá realizar una turbinectomía media (fig. 5). Es crucial conocer esta relación de la inserción conchal en la base de cráneo, ya que si se desgarrara o desinsertara de manera accidental o intempestiva, esta maniobra puede devenir en una fístula de líquido cefaloraquídeo por disrupción de la lámina cribosa.
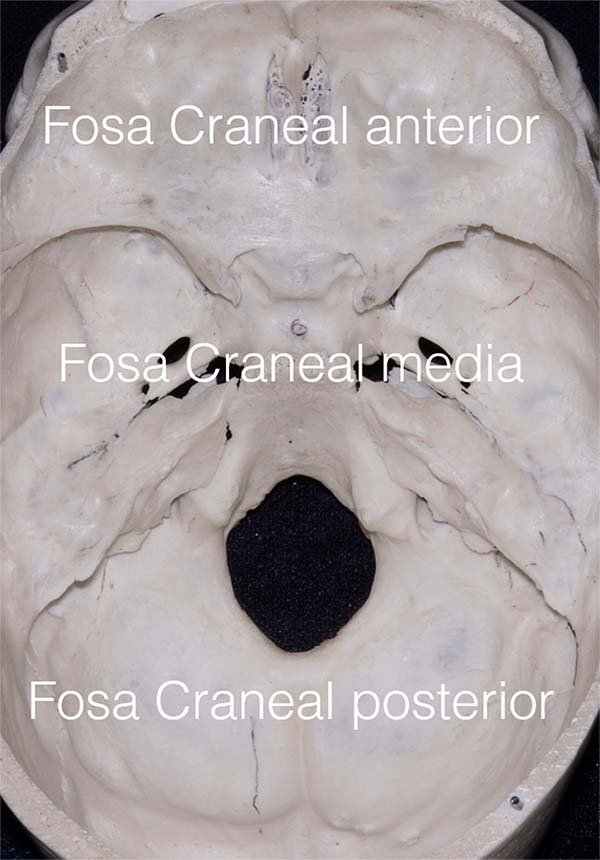
Figura 1: La base del cráneo.
Tabla 2: Reparos en la fase nasal

La manera indicada de realizar la turbinectomía media comienza con la cauterización de la lamela de inserción de la cabeza del cornete, para luego seccionarla lo más próximo posible a la pared nasal lateral. El cirujano debe palpar la dureza ósea con la tijera al seccionar la lamela, ya que una vez que se ha seccionado por completo, sólo se experimentará una delicada sección de mucosa debido a que no hay inserción ósea en el cuerpo y cola del cornete medio. Tal es así que tras seccionar la lamela se debe cortar y traccionar el conjunto del cornete hacia inferior hasta que se desprenda de la pared por completo. Puede ser necesaria la cauterización de algunos vasos nutricios posteriores a lo largo de este procedimiento.

Figura 2: Límites óseos de las fosas nasales. A) Huesos propios de la nariz, maxilares superiores y hueso frontal. B) El tabique óseo se compone del hueso vómer posteroinferiormente, y la lámina perpendicular del etmoides anterosuperiormente. En el ángulo abierto hacia anterior que éstos dos forman se inserta el cartílago septal que formará el tabique cartilaginoso, que corresponde a los dos tercios anteriores del septum nasal. C) Las coanas se encuentran limitadas inferior y lateralmente por el hueso palatino (sus láminas horizontal y vertical, respectivamente), hacia superior por el cuerpo esfenoidal, y medialmente por el septum nasal óseo (vómer).
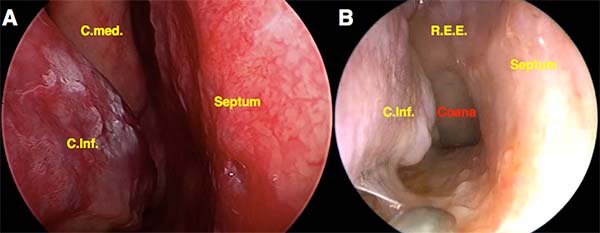
Figura 3: Fase nasal: Fosa nasal derecha A. Vista inicial del abordaje. se aprecian los cornetes inferior y medio y la mucosa septal. B. Obsérvese cómo la cola del cornete inferior nos apunta en dirección a la coana. Inmediatamente superior a ella, encontramos el receso esfenoetmoidal (REE), cubierto por la mucosa que en su profundidad alberga a la arteria esfenopalatina que ha de irrigar el futuro flap nasoseptal, por lo que dicho tejido debe ser preservado a lo largo de todo el procedimiento quirúrgico.
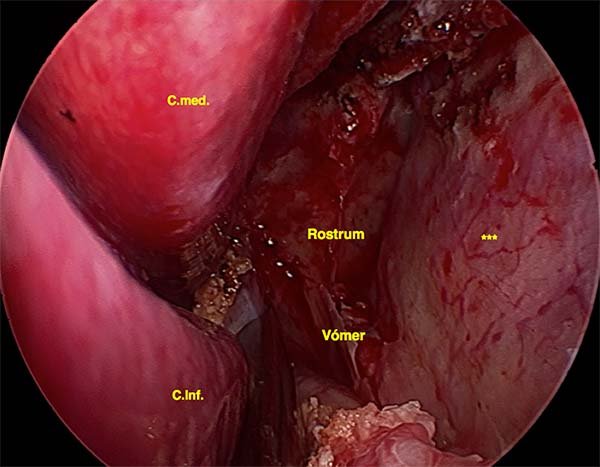
Figura 4: Corredor nasosinusal tras abordaje binostril. Se ha expuesto el rostrum esfenoidal tras haber realizado la septectomía posterior, dejando completamente denudada e intacta a la mucosa septal contralateral (***).

Figura 5: Turbinectomía media. A) Tras la coagulación de la lamela de inserción del cornete medio, se secciona la misma mediante tijera. recordar que siempre debe seccionarse esa inserción y no causar una lesión por arrancamiento, debido a que ello podrá predisponer a una fístula de LCR por disrupción de la lámina cribosa. En el hueso etmoides (visto por su cara derecha) se grafica mediante una línea de puntos la inserción del cornete medio inmediatamente a nivel de la lámina cribosa. B) Una vez retirado el cornete medio, se expondrán el relieve del conducto lacrimonasal (lac.), así como también los reparos que representan al “etmoides anterior”: la apófisis uniforme (unc.) y la bulla etmoidal (Be). Entre ellos se encuentra el hiato semilunar, sitio donde se encuentra el ostium del seno maxilar. al retirar estos elementos generaremos o bien mayor espacio en el corredor nasosinusal, o a su vez una vía de entrada al seno maxilar como parte del abordaje transmaxilar y transpterigoideo.
Foramen Esfenopalatino
Como concepto general, en la base del cráneo existen dos tipos de orificios o forámenes: aquellos que son “verdaderos” agujeros, vale decir, labrados en el espesor del hueso en cuestión, y aquellos que se forman por “espacios” que quedan delimitados por articulaciones entre dos huesos cuyas superficies de contacto se separan y dejan una luz delimitada por dos márgenes. Ejemplos de estos últimos son el foramen lacerum, el foramen yugular, y una lista numerosa en la cual se incluye también el forman esfenopalatino.
El foramen esfenopalatino (fig. 6) da paso a la arteria y nervio homónimos, comunicando la fosa pterigopalatina con la cavidad nasal. Este orificio óseo está formado por el espacio que queda delimitado entre los procesos orbitario y esfenoidal del hueso palatino, al articularse con el hueso esfenoides. Ambos procesos se encuentran en la porción más distal de la lámina vertical del citado hueso. En la porción vertical del palatino además de los dos procesos previamente citados, se encuentran dos crestas: la cresta conchal, donde se inserta el cornete inferior (recordando que es un hueso en sí mismo que se articula con el etmoides), y la cresta etmoidal, que está en relación con la cola del cornete medio (fig. 7). Esta cresta etmoidal, en su dirección anteroposterior nos conduce al foramen esfenopalatino, y a través de éste a la fosa pterigopalatina, la cual ha de ser expuesta en el abordaje transpterigoideo en sus diversas variantes y alcances. Por lo tanto, si se diseca la mucosa que cubre esta estructura ósea, o bien con el uso del neuronavegador, se puede identificar a la arteria esfenopalatina que como ya fue enunciado, da irrigación al Colgajo Nasoseptal de Hadad-Bassagasteguy6 (fig. 8).

Figura 6: Hueso palatino y Formen esfenopalatino. A) El hueso palatino se compone de una porción horizontal (que conforma el tercio posterior del paladar duro u óseo) y una lámina vertical, que constituye el límite lateral de la coana. La porción distal de la lámina vertical posee dos apófisis, una ordinaria (Orb.) y otra esfenoidal (Esf.). cuando se articula con el cuerpo del esfenoides se forma el forámen esfenopalatino, el que comunicará la fosa pterigopalatina con la cavidad nasal. B) La arteria esfenopalatina (la rama terminal de la maxilar interna) penetra el foramen esfenopalatino para dar irrigación a gran parte de la mucosa septal y el tercio posterior de la pared nasal lateral.
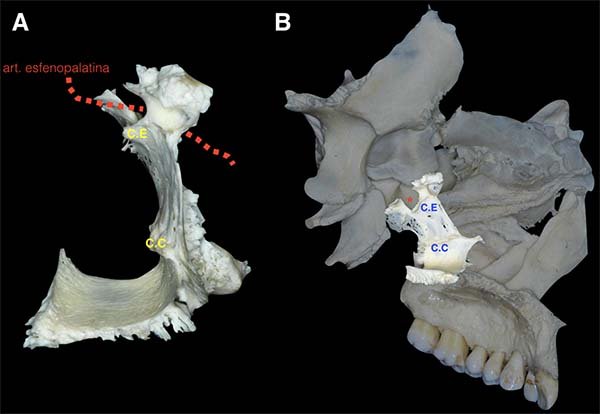
Figura 7: Hueso palatino. A) En su porción vertical, además de los dos procesos previamente citados, se encuentran dos crestas: la cresta conchal (C.C), donde se inserta el cornete inferior (recordando que es un hueso en sí mismo que se articula con el etmoides), y la cresta etmoidal (C.E), que está en relación con la cola del cornete medio. B) Nótese cómo la cresta etmoidal apunta en dirección del canal esfenopalatino (*).
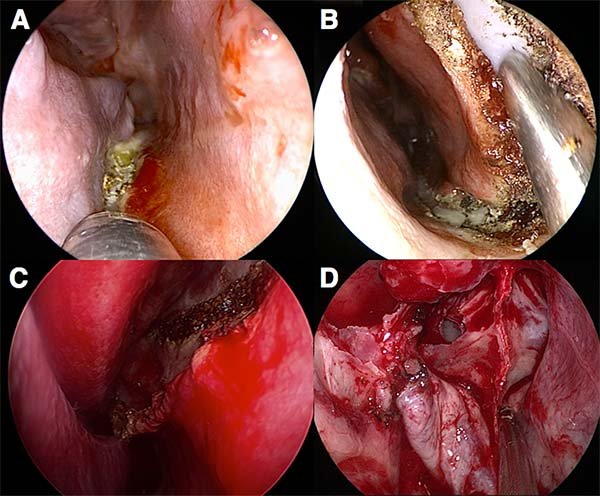
Figura 8: Colgajo nasoseptal de Haddad-Bassagasteguy. A) Incisión inferior. B) Incisión anterior. C) Incisión superior. D) Colgajo completado y reservado en la coana (flecha).
Canal Palatoesfenoidal
Comúnmente conocido como canal Palatovaginal, este canal se encuentra delimitado por el proceso esfenoidal del palatino y el cuerpo del esferoide, particularmente por su proceso vaginal (fig. 9). Este túnel o canal contiene a la arteria faringea y a las ramas del ganglio esfenopalatino. Según lo descripto por Pinheiro-Neto y cols.12, este canal está en verdad formado por el proceso esfenoidal del palatino y la pared anteroinferior del cuerpo esfenoidal, siendo que el proceso vaginal en sí mismo no formaría parte del canal. Por lo tanto, el canal palatovaginal debe ser llamado en su lugar Canal Palato Esfenoidal. Por otro lado, este canal puede ser claramente identificado en los estudios preoperatorios, particularmente en la tomografía computada, pudiendo ser utilizado como verdadero reparo en la cirugía endoscópica endonasal tal cual ocurre con todos los precedentes.
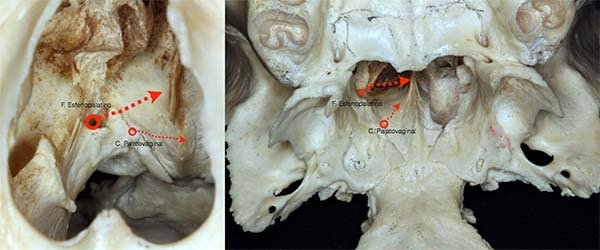
Figura 9: Canal Palatovagina y esfenopalatino.
Ostium del Seno Esfenoidal
El seno esfenoidal representa una excelente vía de acceso natural a las regiones selar, paraselar y clival, así como también al cavum de Meckel y la fosa media1,2,13. Como todo seno paranasal, el seno esfenoidal se comunica con las fosas nasales a través de un orificio conocido como ostium esfenoidal (fig. 10). El mismo es el “blanco” que se ha de mantener a lo largo de la fase nasal, debido a que es a través de él que hemos de identificar el rostrum esfenoidal. Además, el ostium esfenoidal marca el inicio de la incisión superior del flap nasoseptal de Haddad-Bassagasteguy6. Como se ve, el ostium esfenoidal es sumamente importante por diversas razones, principalmente porque es el reparo que marca el fin de la etapa nasal y el comienzo de la etapa esfenoidal, la que ha de comenzar con la osteotomía del rostrum esfenoidal. La misma puede ser realizada con drill de alta velocidad, o en su defecto con escoplos y gubias de Kerrison.

Figura 10: Exposición de ambos ostiums esfenoidales. Ellos se encuentran separados entre sí por aproximadamente 1 cm. en promedio. Aunque a veces se encuentran imperforados, es decir, cubiertos por mucosa, pueden ser hallados a 1,5-2 cm. por encima del techo de la coana.
En términos prácticos y quirúrgicos, el ostium esfenoidal no siempre es visible ya que muchas veces se encuentra obliterado por la misma mucosa. Como regla y guía para ubicarlo, el mismo se encuentra en la gran mayoría de los casos a unos 2 cm. superiores a la coana11,13. Esto significa que entre el ostium esfenoidal y el techo de la coana se extiende un “puente” de mucosa. Esta mucosa se encuentra cubriendo lo que se conoce como receso frontoetmoidal11,13, y es un sitio de capital importancia debido a que por la profundidad de esta mucosa (fig. 3) discurre la arteria nasoseptal, la cual es rama de la arteria esfenopalatina. La arteria nasoseptal debe ser preservada en toda cirugía endonasal debido a que ella es la que brinda el aporte sanguíneo a la mayor parte de la mucosa septal, es decir, al futuro colgajo nasoseptal de Haddad-Bassagasteguy (fig. 8).
El corredor transnasal como acceso a la fosa craneal anterior. Reparos en el abordaje transcriboso a la fosa anterior
La fosa craneal anterior (fig. 11 A-B) se encuentra formada en sus 2/3 anteriores por el hueso frontal y el etmoides, mientras que el tercio posterior lo compone el planum esfenoidal. Esto significa que la fosa anterior puede ser accedida a través de un corredor transnasal (sin necesidad de osteotomía alguna del seno esfenoidal), o bien a través de un abordaje transplanum-transtuberculum, en este caso por el corredor transesfenoidal.
El hueso etmoides se compone de una porción horizontal, multiperforada en su sector mediano, conocida como lámina cribosa, y un sector paramediano conocido como fóvea etmoidal que no es más que el techo de las celdillas etmoidales anteriores y posteriores. Cuenta a su vez con una lámina vertical que se extiende por arriba y por debajo de la lámina cribosa, constituyendo la apófisis crista galli y la porción anterior del septum nasal óseo, respectivamente. Y finalmente, hacia ambos lados e inferiormente a la lámina cribosa se extienden dos masas laterales que se encuentran neumatizadas y que contribuirán a conformar las celdillas etmoidales anteriores y posteriores, separando así las cavidades orbitarias de la nasal (fig. 11 C-D). Se la denomina también lámina papirácea.
Desde una vista endonasal (fig. 12), una vez que el techo etmoidal ha sido completamente expuesto, la visión nos ofrecerá apreciación desde el receso frontal hasta la unión del techo esfenoidal con el planum. Es en este punto donde debemos hallar y coagular las arterias etmoidales anterior y posterior14,15 (fig. 12). Ellas deben ser coaguladas lo más distal posible de su salida orbitaria, debido a que, si se seccionan y se retraen hacia el interior orbitario sin una hemostasia completa, se podría ocasionar un hematoma retro-orbitario que comprometa completamente la visión del paciente.
La arteria etmoidal anterior se encuentra inmediatamente posterior al receso frontal y a las celdillas etmoidales anteriores. La arteria etmoidal posterior se encuentra en la unión del etmoides con el planum esfenoidal, estando en la mayoría de los casos recubierta por hueso, con una dirección prácticamente horizontal, al contrario de su contrapartida anterior que describe una dirección oblicua de anterior a posterior y de lateral a medial.
La lámina cribosa por su parte, se encuentra multiperforada por los ramilletes nerviosos del nervio olfatorio. Esto es importante no solo por su función sensorial, sino también porque a través de esos pequeños orificios se producen invaginaciones de la duramadre que hacen de este sector un sitio muy proclive a desarrollar fístulas iatrogénicas de LCR, o bien encefaloaracnoidoceles, que son motivo de consulta habitual dentro de la patología de la fosa anterior.
Las figuras 13 y 14 grafican dos casos de patología de la fosa craneal anterior abordables por un acceso transnasal-transcriboso: un osteoma osteoide de la lámina cribosa, y un osteoma con diferenciación quística.

Figura 11: La fosa craneal anterior. A) Vista endocraneana. La fosa craneal anterior se encuentra formada en sus 2/3 anteriores por el hueso frontal y el etmoides, mientras que el tercio posterior lo compone el planum esfenoidal (ausente). B) Vista inferior del hueso frontal y etmoides. C) Vista lateral derecha del etmoides. D) Vista supero lateral del hueso etmoides
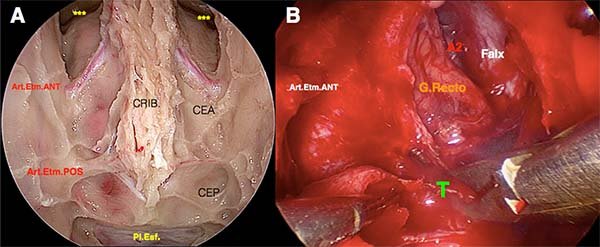
Figura 12: Abordaje transnasal transcriboso. A) Se aprecia desde el receso frontal (***) hasta la unión del techo esfenoidal con el planum (Pl.Esf). Nótense las arterias etmoidales anterior y posterior, y cómo esta última se encuentra recubierta por un tejido óseo más abundante que la anterior. Se han abierto y comunicado las celdillas etmoidales anteriores (CEA) y posteriores (CEP) B) Vista intraoperatoria tras la resección de un osteoma etmoidal (T). Se aprecian los componentes intradurales de la fosa anterior: el Giro recto, la hoz cerebral insertándose en la apófisis cresta galli. La arteria etmoidal anterior ha sido coagulada y seccionada.

Figura 13: Abordaje Transcriboso. A-B) Muestran las imágenes de TC preoperatorias en las que se evidencia una lesión de densidad prácticamente idéntica al tejido óseo (osteoma etmoidal), asociada a una gran cavidad neumoencefálica. C-D) Imágenes en TC postoperatorias que objetivan la resección tumoral junto con la vertiente derecha de la lámina cribosa del etmoides. E) Imágenes intraoperatorias en la que se observa la formación tumoral (T) que impide la visualización completa de la fóvea etmoidal, la que se extiende desde el cono orbitario (Orb.) hasta la lámina cribosa (crib.). F) En la imagen inferior de observa la exéresis completa de la lesión con el defecto (flecha) consiguiente que nos conduce al interior de la cavidad neumoencefálica objetivada en los estudios preoperatorios. Se aprecian la arteria etmoidal anterior coagulada (AEA) y el receso frontal (**).

Figura 14: Abordaje Transcriboso. A) Imágenes de TC preoperatorias en las que se evidencia una lesión quística calcificada.(osteoma quístico). B) Vista intramural tras la resección completa de la lesión. C) Reconstrucción 3D en TC que muestra el defecto tras el abordaje. D) TC control que evidencia exéresis completa de la lesión y el techo etmoidal, con apertura parcial del seno frontal. E) Reconstrucción satisfactoria con HBF.
Los abordajes a la fosa media: la etapa esfenoidal
Como ya se sabe y se ha expresado, el seno esfenoidal representa la principal ruta de acceso a las regiones selar, paraselar y clival, el cavum de Meckel y la fosa media1,2,11. La valoración de las características óseas del seno esfenoidal es mandatoria a la hora de planear un procedimiento endonasal endoscópico. Clásicamente, se ha estudiado la neumatización del seno esfenoidal clasificándola en conchal, preselar y selar16. En el primer tipo, la neumatización es mínima. En el segundo tipo, la neumatización es parcial, pero con ausencia del receso clival, mientras que en el tipo selar la neumatización es completa.
El seno esfenoidal, en los casos de neumatización parcial o total, está completamente tapizado por mucosa de igual manera que las fosas nasales tal como ya describiéramos. Una vez que se retira dicha mucosa, se dejarán al descubierto uno a varios tabiques intrasinusales, los cuales están sujetos a notable variación; y una vez retirados éstos, se dejarán al descubierto una serie de protrusiones y depresiones que, prácticamente, constituyen “un mapa” del contenido neurovascular en contacto con la base del cráneo.
Si el cirujano instilara solución salina fisiológica en el interior del seno esfenoidal (estando el paciente en posición quirúrgica) observaría que en ciertos lugares la solución se acumularía y en otros, no. A aquellas depresiones en las que se acumularía la solución las llamamos recesos mientras que llamamos prominencias a aquellos sitios que se encuentran sobreelevados con respecto al techo del seno esfenoidal.
Analizaremos cada uno de los reparos que se aprecian en el seno esfenoidal y su utilidad al ser puestos en práctica en el quirófano.
Neumatización del seno esfenoidal
Cómo ya se ha dicho, la clasificación clásica en cuanto a la neumatización del seno esfenoidal es aquella que lo cataloga como preselar, selar o conchal16. Sin embargo, esta clasificación no es del todo adecuada a la hora de hablar del corredor transesfenoidal como ruta de acceso al cavum de Meckel y a la fosa media. Esto se debe a que, para acceder a dichos sectores, la neumatización que debemos analizar es si existe o no un receso lateral neumatizado en el seno esfenoidal. Este receso lateral se encuentra ubicado en la base de inserción del proceso pterigoideo del esfenoides, y se encuentra limitado superiormente por el agujero redondo e inferiormente por el agujero vidiano. En caso de que este espacio o receso lateral no se encuentre neumatizado, deberemos drilar el hueso ubicado entre estos dos elementos. Para una mejor ubicación intraoperatoria sería de gran ayuda la guía de neuronavegación con objeto de ubicar los forámenes redondo y vidiano y evitar lesionar ambos nervios.
Es así que existe otra clasificación (fig. 15) en función de la neumatización del receso lateral impuesta por Fernández-Miranda y cols.17, siendo:
- Tipo I o previdiano: neumatización que no excede el borde medial del canal vidiano.
- Tipo II o prerredondo: neumatización que alcanza el borde medial del agujero redondo.
- Tipo III posredondo: la neumatización alcanza o excede el borde lateral del agujero redondo.
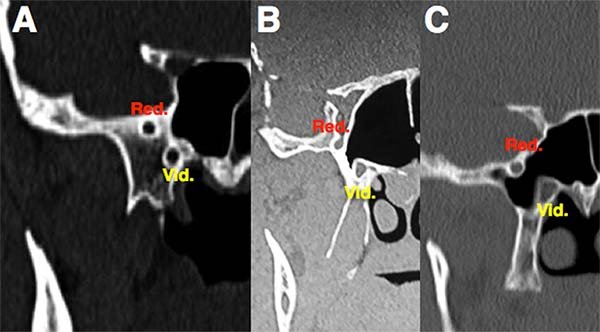
Figura 15: Neumatización del seno esfenoidal. A) Previdiano o Tipo 1. B) Prerredondo o tipo 2. C) Posredondo o tipo 3.
Los Tabiques en el seno esfenoidal
La cirugía endoscópica de la base del cráneo requiere una esfenoidotomía amplia. Sin embargo, lo que puede sonar simple, en verdad no lo es. La luz del seno esfenoidal se encuentra ocupada por numerosos tabiques óseos (fig. 16), de configuraciones y direcciones variadas. Ello hace del planeamiento prequirúrgico un aspecto fundamental a la hora de llevar a cabo un procedimiento endoscópico.
Si bien las configuraciones son más que variadas, existe una neta relación entre la prominencia carotídea y los tabiques esfenoidales. Según Fernández-Miranda et.al16, casi la mitad de los casos presentan un único tabique, un 30% dos, y tres o más tabiques sólo en una minoría de los casos (13%). En esa serie publicada de 27 casos, los hallazgos anatómicos fueron más que interesantes, sobre todo desde un punto de vista quirúrgico: en el 87% de los casos evaluados, por lo menos un tabique se implantó en la prominencia carotídea paraselar o paraclival, y hasta en un 44% de los casos, esa implantación carotídea era de dos tabiques. Solamente en 3 casos (13%) se halló el clásico tabique solitario de localización mediana.
De esto se desprende la necesidad de ser extremadamente cuidadoso la hora de remover estos tabiques, ya que una maniobra inadecuada podría lacerar la carótida y causar un sangrado difícil de controlar. Para remover los tabiques, nuestro servicio utiliza un drill de alta velocidad con fresas diamantadas de 4 mm. realizando movimientos suaves en sentido paralelo a la prominencia carotídea. Creemos que esta es una maniobra adecuada y segura para remover estos tabiques y así exponer finalmente todos aquellos reparos fundamentales del seno esfenoidal que han de guiar la parte final del abordaje.
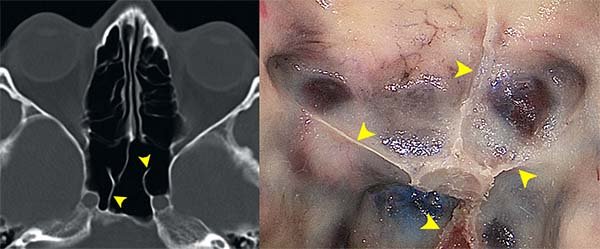
Figura 16: Los tabiques en el seno esfenoidal. Según se describe, en el 87% de los casos, por lo menos un tabique se implanta en la prominencia carotídea paraselar o paraclival, y hasta en un 44% de los casos, esa implantación carotídea puede ser de dos tabiques. Solamente en un13% de los casos puede hallarse el clásico tabique solitario de localización mediana. A) Nótese en esta TC axial cómo los tabiques se implantan en las prominencias carotídeas, sobre todo la izquierda, la cual, a su vez, presenta una dehiscencia ósea completa en su cara anterior. B) Correlación anatómica que evidencia cuatro tabiques, tres izquierdos sobre la carótida intracavernosa y paraclival, y uno derecho sobre la arteria carótida interna (ACI) paraselar.
Reparos en el seno esfenoidal: una vía de acceso a la fosa media y posterior
A la hora de realizar las diferentes variantes de craneotomías esfenoidales (en función de la patología a tratar) es capital reconocer absolutamente todas las impresiones que dejan los elementos neurovasculares intracraneales en las diferentes porciones del seno esfenoidal. Para evaluarlas, creemos que la manera más ilustrativa es aquella basada en la publicación de Alfieri et.al11,19,20, la que reconoce 5 regiones en la vista endoscópica del seno esfenoidal. Dichas regiones son el compartimiento medial, el compartimiento paramediano, y por último el compartimiento lateral (fig. 17). Numerosas estructuras dejan su impresión en estos compartimientos, organizándose de la siguiente manera:
Compartimiento medial: podríamos definirlo como aquel que pautará a que fosa craneal acceder según la patología que nos ocupe. Se disponen de superior a inferior las impresiones de los diferentes accidentes correspondientes a las tres fosas del endocráneo. El planum esfenoidale (como elemento ubicado entre las fosas anterior y media, perteneciendo a la fosa anterior), la silla turca (perteneciente a la fosa craneal media), y la depresión o receso clival (nuestra puerta de acceso endoscópico a la fosa posterior).
Compartimiento paramediano: en este caso, esta región incluye los elementos neurovasculares que rodean al seno esfenoidal. Existen dos impresiones y una depresión. La prominencia óptica es la más superior de esta región, mientras que la prominencia carotídea es el relieve más inferior. Además, encontramos al receso óptico-carotídeo lateral, el receso ópticocarotídeo medial y el receso tubercular lateral.
Compartimiento lateral: para lograr examinar completamente este compartimiento puede ser necesaria la utilización de una óptica angulada (de 30 o 70°). En él, hallamos dos protrusiones, prominencia maxilar y aquella correspondiente al ápex cavernoso.
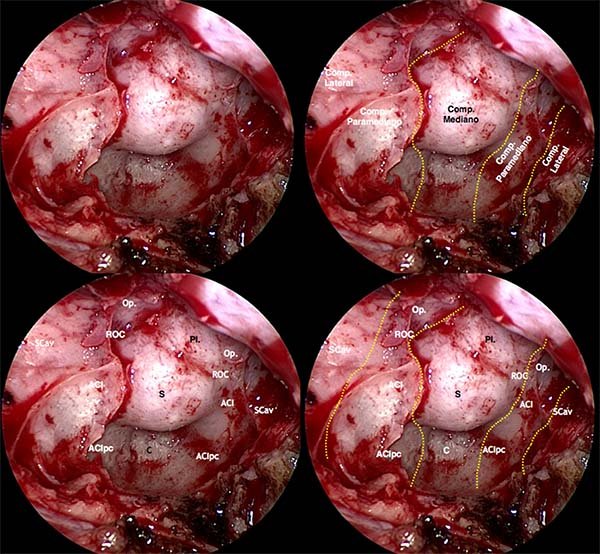
Figura 17: Vista endoscópica del techo del seno esfenoidal. A) Nótese cómo los tabiques sinusales se implantan a los lados de la prominencia selar, hacia la prominencia carotídea. B) La pared superior del seno esfenoidal se divide en cinco regiones: una región mediana, dos regiones paramedianas y otras dos regiones laterales. C-D) En el compartimiento mediano encontramos tres estructuras encolumnadas: el planum esfenoidal (Pl.), la prominencia selar (S) y el receso clival (C). En el compartimiento paramediano se aprecian la prominencia del nervio óptico (Op.), la prominencia carotídea (ACI), ambas separadas por el receso óptico-carotídeo lateral (ROC); a los lados de la invaginación clival se insinúa la prominencia de la carótida paraclival (ACIpc). En el compartimiento lateral se encuentra la prominencia del ápex del seno cavernoso (SCav). La prominencia del nervio maxilar se insinúa por debajo de la anterior.
Anatomía ósea de la región selar
La fosa pituitaria se ubica entre el planum esfenoidal anteriormente, y el dorso selar por detrás (fig. 18). El tubercullum sellae (tubérculo selar) es una prominencia ósea que se extiende transversalmente separando la silla turca del canal quiasmático, aquella pequeña depresión ubicada entre ambos forámenes ópticos.
El pilar óptico (fig. 18) constituye la raíz posterior de anclaje del ala menor del esfenoides. Se lo define como aquel puente óseo que se extiende desde la cara inferior del proceso clinoideo anterior, hasta la cara lateral del cuerpo del esfenoides, inmediatamente por delante del surco carotídeo. El pilar óptico tiene tres superficies:
superior, la que constituye la cara inferior del conducto óptico;
inferior, la que limita superiormente a la fisura orbitaria superior; y posterior, la que se une al cuerpo esfenoidal y constituye parte de lo que será el canal carotídeo.
Otro accidente de suma importancia es lo que se conoce como cresta tubercular lateral (fig. 18)21. La misma es una protrusión ósea localizada en el aspecto más lateral del tuberculum, en el sector más medial del canal carotídeo. El segmento óseo que la une al pilar óptico lo denominaremos puente óptico-tubercular.
La apófisis clinoides media (fig. 18) es una leve prominencia ósea inconstante, que se aprecia generalmente en un 44% de los casos22. Dicho proceso se ubica en la cara medial del canal carotídeo, en el tercio anterior del cuerpo esfenoidal a los lados de la fosa pituitaria. En algunas ocasiones, la apoófisis clinoides media puede ser lo suficientemente protruyente hasta casi alcanzar la punta de la apófisis clinoides anterior, o incluso fusionarse, constituyendo un verdadero anillo alrededor de la arteria carótida interna. Cuando se produce esta variante, se lo denomina conducto carótido-clinoideo19,20.
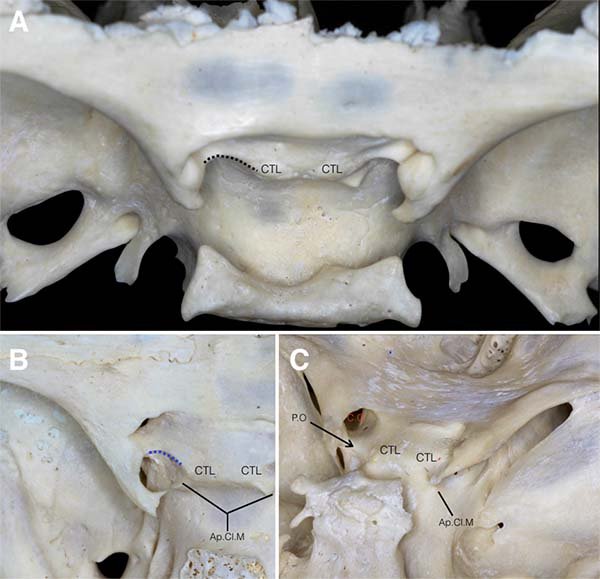
Figura 18: La región selar. A) La fosa pituitaria se ubica entre el planum esfenoidal anteriormente, y el dorso selar por detrás. El tubercullum sellae (tubérculo selar) es una prominencia ósea que se extiende transversalmente separando la silla turca del canal quiasmático, aquella pequeña depresión ubicada entre ambos forámenes ópticos. La cresta tubercular lateral (CTL) es una protrusión ósea localizada en el aspecto más lateral del tuberculum, en el sector más medial del canal carotídeo. B-C) La CTL se une al pilar óptico (PO) por un segmento óseo que denominaremos puente óptico-tubercular (línea de puntos azul). La apófisis clinoides media (Ap.Cl.M) se ubica en la cara medial del canal carotídeo, en el tercio anterior del cuerpo esfenoidal a los lados de la fosa pituitaria. En algunas ocasiones, puede ser lo suficientemente protruyente hasta casi alcanzar la punta de la apófisis clinoides anterior, o incluso fusionarse, constituyendo un verdadero anillo alrededor de la arteria carótida interna, que será denominado conducto carótido-clinoideo.
La apófisis clinoides anterior, el pilar óptico y el receso ópticocarotídeo lateral
La apófisis clinoides limita anterolateralemente la fosa pituitaria. Ella presta inserción a numerosos repliegues durales, como ser el diafragma selar, el ligamento petroclinoideo anterior y el interclinoideo16. Presenta tres puntos de anclaje a la base del cráneo anterior: uno medial, al planum esfenoidal; otro lateral hacia el ala menor del esfenoides, y uno inferior que se corresponde con el pilar óptico que, tal como ya fuera descripto, constituye el límite inferior del conducto óptico.
La apófisis clinoides anterior guarda especial relación con la arteria carótida interna (ACI), ya que ella contribuye a formar lo que se denomina el segmento clinoides de la misma16. Dicho segmento se encuentra limitado entre los anillos durales proximal y distal, los cuales no son más que prolongaciones durales que se desprenden de la duramadre que recubre a la apófisis clinoides. Si bien se lo entiende como un segmento aparte, por la laxitud de la unión del anillo dural proximal a la pared de la ACI, se produce la penetración de canales venosos desde el seno cavernoso, por lo que, desde el punto de vista quirúrgico, el segmento clinoideo es entendido en verdad como “parte” del segmento cavernoso.
Si bien el proceso clinoideo anterior no tiene una contrapartida endoscópica, el pilar óptico se corresponde con el receso ópticocarotídeo lateral11,19-22 (fig 19). Éste es una depresión de profundidad variable entre los diferentes casos, que separa la prominencia carotídea de la prominencia óptica. Esta depresión es un reparo fundamental para determinar la ubicación de estos elementos neurovasculares, evaluando la relación entre ellos y la osteotomía que hemos de realizar. Este receso se encuentra limitado superiormente por la cara inferior del canal óptico, inferiormente por la cara superior de la fisura orbitaria superior (hendidura esfenoidal), y medialmente por el fino recubrimiento óseo de la prominencia carotídea, que en muchos casos puede estar ausente23 significando entonces un importante dato a tener en cuenta para no lacerar este vaso durante el procedimiento.

Figura 19: El pilar óptico se corresponde con el receso ópticocarotídeo lateral (ROCL). Este es una depresión de profundidad variable que separa la prominencia carotídea (ACI) de la prominencia óptica (Pr.Op). Este receso se encuentra limitado superiormente por la cara inferior del canal óptico, inferiormente por la cara superior de la fisura orbitaria superior (Prominencia que desde esta vista se corresponde con la protrusión de V1, delimitada con líneas de puntos), y medialmente por el fino recubrimiento óseo de la prominencia carotídea, que en muchos casos puede estar ausente. A su vez se observa la prominencia maxilar (V2), delimitada con línea de puntos. Entre ambas protrusiones trigeminales se aprecia un área de hueso levemente deprimida, lo que se conoce como pilar maxilar o maxilar struct (PM).
El receso tubercular y el receso ópticocarotídeo medial
Continuando con la visión endoscópica, en el aspecto más lateral de la prominencia del tubérculo selar, existe una depresión que se conoce como receso tubercular lateral21 (fig. 20). Éste se encuentra rodeado lateralmente por la prominencia carotídea. Este receso tubercular lateral se encuentra “unido” al receso ópticocarotídeo lateral por una suerte de puente óseo. Ese puente óseo representa un verdadero arco en el sector más superior de la prominencia carotídea (la carótida paraselar), por lo que se denomina arco óseo distal21,23 (DOA, por sus siglas en inglés). Inmediatamente por debajo de este arco se tiende el repliegue dural del anillo dural distal, por lo que el DOA no es otra cosa que el relieve óseo que representa el “final” de la ACI intracavernosa para convertirse en supraclinoidea.
Como se logra apreciar, son varios los reparos que nos hablan acerca de las relaciones entre la ACI con el nervio óptico, y el receso ópticocarotídeo medial (ROCM)21,23 es otro más de los reparos que integran este importantísimo grupo. Este mismo puede ser interpretado como un verdadero “key-hole” endoscópico21, ya que su reconocimiento puede representar el acceso a un numeroso conjunto de estructuras y regiones; o bien que debería ser tenido en cuenta para no lesionar o retraer determinadas estructuras que se encuentran relacionadas a él.
El ROCM. (fig. 20) es una depresión ósea en forma de “lágrima”, la cual se encuentra conformada en la unión medial del canal carotídeo (su segmento paraclinoideo, es decir, entre ambos anillos durales) y el canal óptico (a medida que el nervio discurre oblicuamente en una dirección antero posterior, alejándose del cono orbitario). El vértice lateral de esta lágrima se centra en el aspecto más medial del ROCL, o sea en el punto de intersección de la ACI con el nervio óptico. El límite inferior de este receso en forma de “lágrima” se encuentra en la unión del DOA con el aspecto más inferior del receso tubercular lateral y el aspecto superolateral de la silla. Lo que ocurre en realidad en este punto, es que la parte más medial de la ACI paraclinoidea encuentra la cara superolateral de la silla. El vértice mediosuperior de la “lágrima” está representada por la cara inferomedial del canal óptico. A diferencia del anillo dural proximal descripto anteriormente, el anillo dural distal es completo y está firmemente adherido a la adventicia de la arteria carótida. El aspecto anterior de este anillo está formado lateralmente por la duramadre de la superficie superior del pilar óptico, y medialmente por la duramadre que reviste profundamente al DOA del surco carotídeo y su extensión medial hacia el receso tubercular lateral, por lo que se puede aceptar que el DOA no es otra cosa que el “representante” endoscópico del anillo dural distal21. Como se logra apreciar, el MOCR se convierte en un reparo más que importante, para localizar y tener control sobre la ACI, algo parecido a lo que ocurre con la apófisis clinoides anterior en una craneotomía pterional16,21.
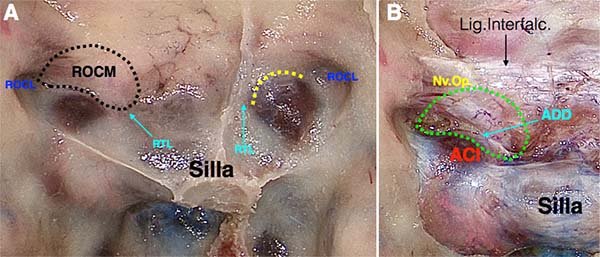
Figura 20: A) El receso tubercular lateral (RTL) se encuentra rodeado lateralmente por la prominencia carotídea. Este receso tubercular lateral se encuentra “unido” al receso ópticocarotídeo lateral por una suerte de puente óseo, el cual representa un verdadero arco en el sector más superior de la prominencia carotídea (la carótida paraselar), por lo que se denomina arco óseo distal (línea de puntos amarillos). El receso ópticocarotídeo medial (ROCM, línea de puntos negros) es una depresión ósea en forma de “lágrima”, que se encuentra conformado en la unión medial del canal carotídeo y el canal óptico. El vértice lateral de esta lágrima se centra en el aspecto más medial del ROCL, siendo el límite inferior de esta “lágrima”, la unión del arco óseo distal con el aspecto más inferior del RTL y el aspecto superolateral de la silla. Superiormente el ROCm. se encuentra limitado por la cara inferior del conducto óptico. B) Una vez retirado el recubrimiento óseo, se expone la duramadre que recubre cada uno de los elementos y recesos enumerados. Como puede apreciarse, el anillo dural distal (ADD) coincide plenamente con el arco óseo distal, es decir, con el aspecto más inferior del ROCM. (línea de puntos verdes). Se aprecia también el ligamento interfalciforme, que se extiende entre ambos nervios ópticos, siendo éste el límite superior de una futura osteotomía transplanum.
Los abordajes endoscópicos a la fosa media y posterior por el corredor transesfenoidal
Como se ha visto en la primera parte de este trabajo, el corredor transesfenoidal es la vía inicial común para numerosos abordajes a la fosa media asi como también a la fosa posterior. Entre los primeros se incluyen el abordaje transplanum-transtuberculum y el abordaje transelar, mientras que el abordaje transclival es la vía de acceso a la fosa posterior, mejor dicho, a la región del clivus superior.
- Abordaje Transplanum-Transtuberculum: (fig. 21) para realizarlo, es conveniente realizar, además de la septectomía posterior, una etmoidectomía posterior, mediante la apertura, comunicación y remoción de las celdillas etmoidales posteriores. Este abordaje está definido por la remoción del planum esfenoidal y el tuberculo sellar11. La remoción ósea se extiende hacia los canales ópticos, y se encuentra limitada hacia anterior por las arterias etmoidales posteriores, hacia posterior por la identación ósea que separa el tubérculo de la silla, es decir, por el aspecto más inferior del receso tubercular lateral, y hacia los laterales por los ROCM, con el objetivo de no dañar la ACI. Así, la remoción ósea adopta la forma de un trapecio, siguiendo los límites anteriormente citados.
Mediante el abordaje transplanum-transtuberculum alcanzamos al contenido de la cisterna supraselar: los nervios ópticos y el quiasma, las ACI, y las arterias cerebrales anteriores en su porción infracallosa (A1) La indicación más acertada para este abordaje, quizás, se centra en los meningiomas del planum o adenomas hipofisarios con extensión supraselar, así como también para la cirugía de los craneofaringiomas, donde este abordaje es casi una regla a la hora de tratarlos por vía endoscópica. - Abordaje transelar: (fig. 22) como ya ha sido enunciado, éste es la variante más utilizada dentro del amplio conjunto de abordajes endonasales a la base del cráneo. Mediante él se logran tratar los adenomas hipofisarios, craneofaringiomas intraselares y quistes de Rathke, entre otros. Existe un aspecto a mencionar acerca de la exposición en esta variante de abordaje, que es lo que se conoce como los cuatro azules (Kassam y cols.)24: mediante esta denominación nos referimos a las estructuras venosas que rodean a la silla turca: ambos senos cavernosos hacia los laterales, y los senos intercavernosos anterior y posterior, conformando una verdadera “corona venosa” alrededor de nuestro objetivo quirúrgico. La craniectomía selar se encuentra limitada en 360 grados por dichas estructuras venosas, además de las prominencias carotídea y óptica. El abordaje transelar puede combinarse con un abordaje transplanum o eventualmente con un abordaje transclival para acceder a patologías extensas tales como un cráneofaringioma o un cordoma del tercio superior del clivus.
- Abordaje transclival: (fig. 23) en este abordaje, la craniectomía se lleva a cabo inmediatamente caudal al relieve selar, es decir, en la invaginación clival, limitada hacia los laterales por las prominencias carotídeas paraclivales, y hacia superior por el dorso selar y las apófisis clinoides posteriores. La remoción ósea puede ser parcial (para exponer el tercio superior y/o medio del clivus) o total (panclivectomía). Es así que nos provee un acceso amplio, sea a las estructuras ubicadas en el tercio más alto del clivus, relacionado al dorso selar, por ende, a la cisterna interpeduncular, el III par y el tope de la arteria basilar; pero, y siendo lo más representativo del abordaje, lo más crítico desde el punto de vista anatómico, es la exposición de las estructuras neurovasculares del tronco encefálico: los pares craneales III al XII (aunque los pares bajos logran ser expuestos de mejor manera utilizando una óptica angulada efectuando un abordaje al foramen magno, como se verá más adelante) y la totalidad de la circulación posterior: el sistema vértebrobasilar y sus ramas colaterales y terminales: las arterias cerebrales posteriores. Mediante esta variante, podemos tratar numerosas patologías, siendo las más frecuentes los cordomas del clivus o los meningiomas petroclivales.
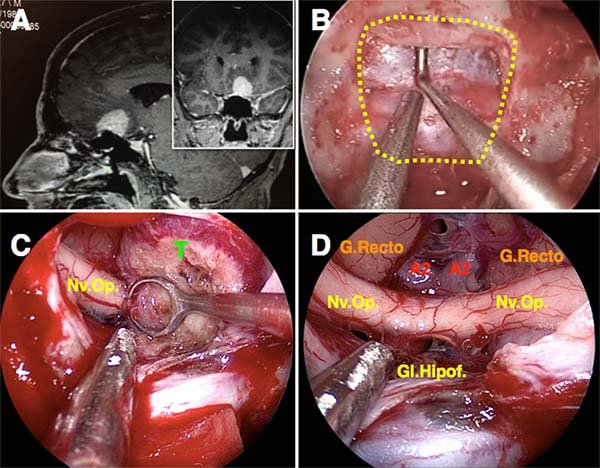
Figura 21: Abordaje transplanum-transtuberculum. A) RMN preoperatoria en la que se aprecia una lesión compatible con meningioma del planum esferoidal B) Abordaje endoscópico transplanum-transtuberculum. la craniectomía se repasa con línea de puntos, mientras se observa cómo el disector separa la porción ósea del plenum propiamente dicha. C) Disección de la lesión tumoral (T) del nervio óptico (Nv.Op.) derecho. D) Vista final luego de la exéresis completa de la lesión. Se aprecian el quiasma óptico, el tallo y la glándula hipófisis (Gl.Hipof) y ambas A2 en la fisura interhemisférica.
El abordaje endoscópico a la fosa posterior: aportes del corredor transnasal
Como ya se ha visto, la fosa posterior, desde un abordaje endoscópico, puede ser accedida a través de un corredor transesfenoidal en lo que se conoce como abordaje transclival11. Sin embargo, dicho acceso provee un alcance sólo al clivus superior, esto es, a la región comprendida entre la fosa interpeduncular y el surco pontomescencefálico. Este abordaje es excelente para tratar lesiones localizadas en dicha región, como ser por ejemplo un cordoma de clivus que comprometa el dorso selar y la porción más superior del mismo. Pero no es suficiente para aquellas lesiones cuyo compromiso se extiende más caudalmente que los ya citados límites.
Para esos casos es posible realizar un abordaje a través de los dos tercios inferiores del clivus25,26, diferenciándose del anteriormente descripto en que el abordaje al clivus bajo no se ha de realizar por el corredor transesfenoidal clásico. A continuación, se desarrollarán los diferentes reparos implicados en un abordaje endonasal al clivus bajo.
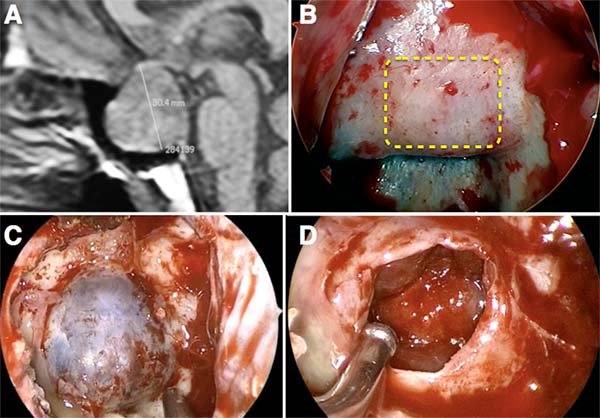
Figura 22: A) RMN preoperatoria que evidencia macroadenoma de hipófisis de 30 mm. de diámetro mayor B y C) Abordaje endoscópico transitar clásico. la craniectomía se repasa con línea de puntos, D) Vista final luego de la exéresis completa de la lesión. Se aprecia el diafragma aracnoidal selar sin signos de fístula de LCR.

Figura 23: Abordaje transclival. A) RMN T1 con gadolinio preoperatoria que evidencian un cordoma del tercio superior del clivus. B-C) Imágenes intraoperatorias en las que se observa la arteria basilar (AB),las arterias cerebrales posteriores (ACP); se aprecia la emergencia de la arteria comunicante posterior (ACoP) y la salida de la art. Cerebelosa superior (ACS). Entre la ACP y la ACS se objetiva la emergencia del nervio motor ocular común (III). Nótese las perforantes naciendo del tope de la basilar e ingresando al espacio perforando posterior.
Reparos óseos del clivus y la fosa posterior
El clivus, que se corresponde con la lámina cuadrilátera del hueso occipital, se articula anterosuperiormente con el cuerpo esfenoidal, y lateralmente con la porción petrosa del hueso temporal. Esta articulación deja una brecha ocupada por tejido conectivo de relativa densidad, conformando un espacio que se conoce como fisura petroclival. Esta fisura, en sus extremos, tiene dos ensanchamientos, los cuales no son otra cosa que los agujeros rasgados anterior (o foramen lacerum) y posterior (foramen yugular).
En una vista endocraneana del clivus14 (fig. 24), lo apreciamos como una lámina ósea gruesa, bastante lisa sin grandes rugosidades. Hacia su margen inferolateral, se encuentra una prominencia ósea redondeada que se denomina tubérculo yugular. El mismo se encuentra limitado inferiormente por el canal del hipogloso y lateralmente por el foramen yugular en sí mismo. El cóndilo occipital (porción condilar del occipital) se encuentra inmediatamente inferior al canal del hipogloso, y forma el margen anterolateral del foramen magno.
Ahora bien, si miramos al clivus desde su cara anterior (fig. 25), o sea, la cara que se ha de exponer en un abordaje endoscópico endonasal, veríamos una superficie rugosa, a diferencia de la cara dorsal como ya se ha enunciado. Eso ocurre porque la cara anteroinferior del clivus presta inserción a numerosos músculos. Es así que la cara ventral del clivus está atravesada por dos líneas “horizontales”, las líneas clivales superior e inferior (también llamada cresta supracondilar)25,26. La primera marca la inserción del músculo largo de la cabeza (longus capitis) mientras que la segunda presta inserción al recto anterior de la cabeza (rectus capitis anterior). A nivel de la línea clival superior, en la línea media, se encuentra una prominencia más pequeña que se conoce como tubérculo faríngeo. Éste presta inserción a la fascia faríngobasilar y al constrictor superior de la farínge. Una vez desinsertados y retirados, se podrán evaluar las líneas clivales y músculos subyacentes que en ellas se insertan, todo logrado a través de un abordaje transclival bajo, el cual tiene como principal objetivo patologías que involucren el 1/3 inferior del clivus y el forámen magno (fig. 26).
Otro dato importante a notar, es que la línea clival inferior coincide con el orificio externo del canal del hipogloso y, de hecho, éste se encuentra en el aspecto más lateral de esa línea. De hecho, es quizás el reparo más importante de esta región debido a que será de utilidad para localizar a los pares bajos y al nervio hipogloso, con el objetivo de evitar lesionarlos (fig. 26).
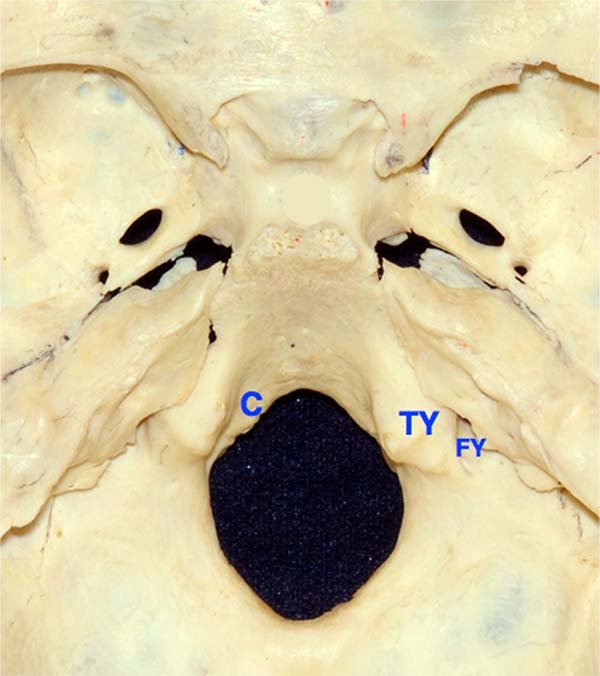
Figura 24: Vista endcraneana del clivus. FY: foramen yugular. TY: tubérculo yugular. C: cóndilo occipital.

Figura 25: Vista ventral del clivus. A) Vista exocraneana del clivus, evidenciando las líneas clávales superior e inferior (LCSup y LCInf.). En posición mediana se aprecia el tubérculo faríngeo. B) Disección cadavérica. Se ha retirado la fascia faringobasilar, evidenciándose los músculos largos de la cabeza y recto anterior de la cabeza, insertándose en sus respectivas líneas clivales.
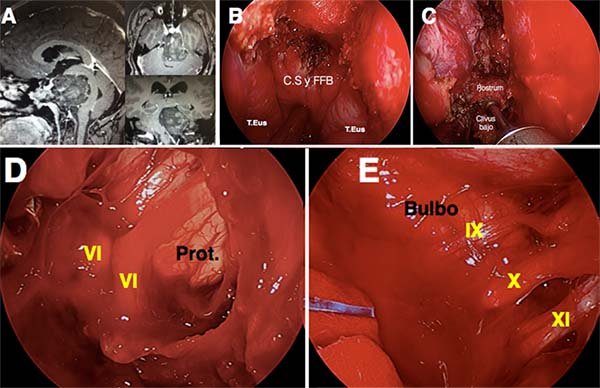
Figura 26: Abordaje endonasal al clivus bajo, por el corredor transnasal. A) RMN que evidencia cordomaa de los tres tercios clivales. B) Se comienza con la desinserción del constrictor superior y la fascia faringobasilar (C.S y FFB). C) Se procede a drilar los dos tercios inferiores del clivus. D-E) Imágenes intraoperatorias que evidencian la cara anterior pontina y bulbar, con ambos VI pares en la línea media, y tras utilizar una óptica anulada observamos los pares bajos.
Reparos que guían los abordajes extendidos en el plano coronal: el abordaje transpterigoideo
Los abordajes transpterigoideos implican un conjunto de diferentes accesos con diferentes “targets” quirúrgicos pero que guardan un factor en común: se realizan a través de los procesos pterigoideos del hueso esfenoides. El proceso pterigoideo (o apófisis pterigoides) del esfenoides consta de una base de la cual se desprenden dos ramas, una medial y una lateral, dejando un espacio entre ambas que se denomina fosa pterigoidea. Desde un punto de vista funcional, los procesos pterigoideos prestan inserción a los músculos pterigoideos medial y lateral, los cuales tienen función masticatoria.
La región del proceso pterigoideo consta de tres importantes forámenes (figs. 8 y 27 A): el foramen redondo (que da paso a la rama V2 o nervio maxilar), el forámen vidiano27,28,30 (que da paso al nervio homónimo) y el canal palatovaginal, ya descripto (fig. 11). El proceso pterigoideo limita con numerosas regiones de interés neuroquirúrgico, como ser la fosa infratemporal hacia lateral, la fosa media superiormente, y la trompa de Eustaquio y la fosa de Rossenmueller posteriormente. Es por eso que comprender la anatomía del proceso pterigoideo es una verdadera “llave” para acceder a las regiones paramedianas de las fosas infratemporal, media y posterior.
Los abordajes transpterigoideos pueden acceder a diferentes zonas de la fosa media y posterior. Todos ellos requieren la utilización del espacio aéreo del seno maxilar, y desplazan los tejidos blandos de la fosa pterigopalatina28, para finalmente remover parcial o totalmente el proceso pterigoideo, de manera de tener control de la región quirúrgica de interés. Durante el planeamiento operatorio puede ser dificultoso estimar la extensión necesaria de este corredor quirúrgico, por lo que se propone dividir al proceso pterigoideo a través de líneas imaginarias verticales y horizontales que “atraviesan” los forámenes vidiano y redondo (fig. 27 B). Así quedan divididas las siguientes zonas de interés para abordar las diferentes patologías que se extienden en el plano coronal: la fosa infratemporal, la fosa media, el receso lateral del seno esfenoidal (fig. 15) y la mismísima fosa pterigopalatina (localizada entre las dos líneas verticales). Nótese cómo la carótida petrosa se ubica entre las dos líneas horizontales, vale decir, que el reconocimiento de los forámenes redondo y vidiano como dos verdaderos reparos quirúrgicos para tomar reparo de la localización en profundidad del segmento petroso de la ACI.
Es importante remarcar que el abordaje transpterigoideo, dependiendo de la zona objetivo (fig. 27 B), requerirá una mayor o menor exposición en el corredor nasosinusal. Tal es así que aquellos abordajes a zonas que se extienden superiormente al agujero vidiano (y no por debajo de él) requerirán un corredor nasosinusal “ampliado”28 (fig. 27 C). ¿Qué significa esto? Se trata de corredor nasosinusal con mayor extensión anteroposterior, desde el conducto lacrimonasal hasta la pared posterior del seno maxilar (sin necesidad de removerla), y desde la pared orbitaria inferior (o sea, el techo del seno maxilar) hasta el borde más caudal del cornete inferior. Vale decir, se realiza la exéresis de la apófisis uncinada y la bulla etmoidal (etmoidectomía anterior, fig. 5), y se continúa con la etmoidectomía posterior para ganar extensión suficiente. Mediante este corredor “ampliado”28 se podrán tratar patologías mediante los abordajes al receso lateral del seno esfenoidal, al cavum de Meckel y al ápex petroso.
Por el contrario, para tratar patologías que se encuentran por debajo del nivel del agujero vidiano, la exposición que brinda el canal nasosinusal “ampliado” no ha de ser suficiente. Para ampliar la exposición aún más, se realiza una resección completa de la pared posterior del seno maxilar (generándose así un corredor “nasomaxilar”) que brindará acceso a la fosa infratemporal (fig. 28), el espacio parafaríngeo e incluso a la fosa media si nos dirigimos más superiormente. Asimismo está descripto combinar esta maxilectomía parcial con una extensión hacia anterior mediante la remoción del proceso ascendente del hueso maxilar, lo que también se conoce como abordaje de Denker.
En este punto, es posible inferir que si combináramos un abordaje transclival bajo (fig. 25) a través de un corredor nasomaxilar amplio con la remoción del proceso pterigoideo, podríamos alcanzar patologías que invaden el plano coronal de la fosa posterior. Eso es correcto y se conoce como abordaje transcondilar o eventualmente trans-tubérculo yugular, englobados en la literatura como abordajes tipo “far medial”25,26.
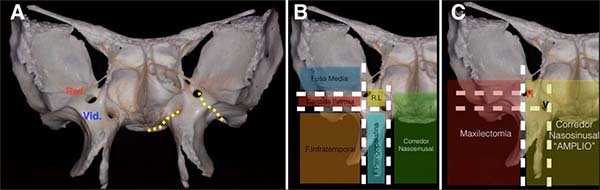
Figura 27: Los abordajes transpterigoideos. A) Anatomía del proceso pterigoideo, y de los forámenes Redondo (Red.) y vidino (vid.), graficandose el nervio V2 y vidiano. B) Dos líneas verticales y horizontales que atraviesan los forámenes Redondo y vidiano dividen la región en los objetivos de cada Abordaje transpterigoideo: al receso lateral del seno esfenoidal (R.L), fosa pterigopalatina, fosa infratemporal y fosa media. C) Corredor quirúrgico necesario para efectuar cada tipo de Abordaje transpterigoideo.
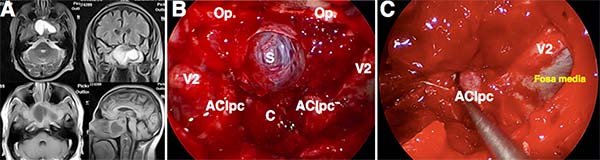
Figura 28: Abordaje Transpterigoideo BILATERAL. A) Imágenes intraoperatorias en la que se observan cortes axiales, sagital y coronal en RMN de un adenoma de hipófisis no funcionante invasor. Nótese la relación con el piso de ambas fosas medias, ambos conos orbitarios, ubicándose posteriormente a ambos senos maxilares. B-C) Imagen intraoperatoria tras un abordaje transpterigoideo bilateral, exponiéndose la duramadre de ambas fosas craneales medias. Se aprecia la aracnoides selar (S) en el centro de la imagen. Inmediatamente superior destacamos al planum esfenoidal y ambos nervios ópticos (Óp) recubiertos por una capa delgada de duramadre, y la invaginación clival (C) por debajo de la prominencia selar. Hacia los laterales observamos a la arteria carótida interna paraselar y para clival (ACIpc). Y en el compartimiento lateral, lo más destacado de la imagen: el nervio maxilar (V2) e inmediatamente lateral a él la duramadre de la fosa media.
DISCUSIÓN
La anatomía microquirúrgica es el mejor aliado del neurocirujano a la hora de emprender el procedimiento quirúrgico. La endoscopía de base de cráneo no viene sino a complementar la técnica microquirúrgica impuesta por Gazi Yasargil a principios de la década de 1970. Si bien a principios de la década de 1960 el uso del endoscopio fue introducido por Guiot como una simple asistencia al microscopio, fue un aporte invalorable al igual que el de Jho y Carrau en los años subsiguientes; sin mencionar los enormes aportes de nuestros contemporáneos Cappabianca, Fernández-Miranda, Prevedello y Kassam.
La patología de la base del cráneo es por demás variada, desde el aspecto histopatológico, así como de ubicación anatómica. Hasta mediados de la década de 1990, la endoscopía de base de cráneo se reservaba prácticamente para la cirugía del adenoma de hipófisis, compartiendo dicha indicación con el abordaje microscópico clásico. Hacia comienzos de los años 2000, la indicación de la cirugía hipofisaria prácticamente había virado casi en su totalidad al abordaje endoscópico endonasal, así como también habiéndose ampliado los alcances de la endoscopía, tal como lo resume Amin Kassam. Hoy en día, no sólo la endoscopía de la base del cráneo logra alcanzar la patología mediana “desde la crista galli hasta el foramen magno”, sino que también ha logrado “exceder” la barrera impuesta por la ACI y extenderse lateralmente en el plano coronal para alcanzar patología orbitaria, de la fosa infratemporal, o del glomus yugular.
La patología de la fosa anterior que inicialmente fue abordada endonasalmente fue la fístula de LCR14,15. Para tratarlas, es necesario lograr una exposición amplia y adecuada para reconocer y sellar el defecto, sin descuidar el epitelio olfatorio que en su profundidad alberga los filetes que penetran desde la lámina cribosa. Es así que muchos cirujanos comenzaron a intentar tratar patología tumoral de la fosa anterior por este mismo abordaje. Siempre es de buena práctica reconocer y tomar control de la arteria etmoidal anterior (quizás el reparo más importante en la cirugía endoscópica de la fosa anterior, figs. 13 y 14), ya que su ubicación nos dirá que hacia anterior encontraremos el receso frontal y la apófisis crista galli, e inmediatamente posterior y medial a ella tomaremos reparo de la lámina cribosa. Tomando reparo de estos elementos, nos guiarán directamente y sin estructuras nobles intermedias a patología que nace de la fosa anterior, como meningiomas del surco olfatorio o estesioneuroblastomas. Estas lesiones, habitualmente de gran tamaño, ocasionarían quizás más daño secundario al ser abordadas transcranealmente que endonasalmente, debido a que en esta última vía no se retraerían los lóbulos frontales ni se traccionarían los nervios ópticos. Es importante tomar reparo de la arteria etmoidal posterior, ya que ésta nos marcará el límite posterior de la osteotomía a realizar, debido a que, en profundidad a la misma, encontraremos un repliegue dural que se conoce como ligamento interfalciforme que marca el inicio (hacia posterior) del seno intercavernoso anterior21. Esto significa que cuando se insinúa la arteria etmoidal posterior, inmediatamente por detrás de ella se encontrará el planum esfenoidal con el inicio de “los cuatro azules”24. En nuestro servicio hemos tratado satisfactoriamente por esta vía fístulas de LCR (tanto traumáticas como adquiridas), encefaloaracnoidoceles, osteomas cribosos, estesioneuroblastomas y meningiomas del surco olfatorio.
Otro dato a tener en cuenta es la utilización de la TC preoperatoria a la hora de planear el recorrido quirúrgico que ha de emprenderse. Y la TC es fundamentalmente útil para evaluar la anatomía ósea del seno esfenoidal y los forámenes relacionados al esfenoides. Como ya se sabe, el grado de neumatización del seno esfenoidal es un importante condicionante a la hora de realizar la osteotomía en el techo del seno esfenoidal. Conforme avanza la edad del paciente, el hueso se adelgaza progresivamente, pudiendo en muchos casos, como hemos observado en nuestra experiencia, existir solo una fina o inexistente capa de hueso recubriendo a la ACI23 o al nervio óptico, obteniendo una clara visualización de un ROCL sumamente neumatizado. Además, la TC en ventana ósea es una herramienta muy útil a la hora de evaluar la existencia y configuración de los tabiques intrasinusales, que, como ya ha sido enunciado, presentan una interesante variabilidad anatómica. Pero independientemente de eso, y como ya ha sido reportado en la literatura, más de un 80% de los tabiques esfenoidales tienen como base de implantación en la ACI paraselar o paraclival, por lo que su conocimiento orientará al cirujano a reconocer las prominencias carotídeas en un seno poblado de tabiques y con una neumatización incompleta18.
Exactamente lo mismo ocurre con un receso lateral lo suficientemente neumatizado (fig. 15), debido a que éste es la puerta de entrada a la fosa media e infratemporal28 en los abordajes transpterigoideos (fig. 28). Y para tener buen reparo y conocimiento de ellos, la anatomía de los forámenes vidiano27,28,30,31 y redondo debe ser siempre tenida en cuenta por el cirujano en todo momento. Recordemos que el orificio vidiano, es decir, el final del canal vidiano que alberga al nervio homónimo (que nace de la anastomosis del nervio petroso profundo mayor y petroso superficial mayor) se encuentra inmediatamente por detrás de la apófisis esfenoidal del hueso palatino (fig. 8). Ambos, el foramen esfenopalatino y el orificio vidiano, se encuentran recubiertos por la mucosa nasal, pero son abordables en el aspecto posterolateral de la fosa nasal, a la hora de realizar un abordaje transpterigoideo, con o sin maxilectomía. Recordemos que un reparo importante para inferirlo es la cola del cornete medio, la cual apunta en dirección al foramen esfenopalatino; recordando también que la cresta etmoidal del palatino (fig. 9), la cual se relaciona íntimamente con el cornete medio, también apunta en dirección al foramen. De aquí se desprende la importancia de reconocer la dirección de la cola del cornete medio, que apuntará a los forámenes esfenopalatino y vidiano, los que se encuentran a aproximadamente unos 12 mm. superolateralmente a la coana. El foramen redondo (fig. 8), por su parte, es otro reparo fundamental debido a que de él emerge la rama trigeminal V2, que se continuará como nervio infraorbitario, recorriendo el techo del seno maxilar desde su pared posterior hasta el foramen infraorbitario por el que se distribuirá en su territorio sensitivo. Vale decir que a la hora de realizar una apertura del seno maxilar en la pared nasal lateral (previa etmoidectomía anterior), localizar al nervio nos servirá de guía hacia la pared posterior del seno maxilar, y una vez removida ésta, hacia la fosa pterigopalatina y la base del proceso pterigoideo27,28,30,31.
Una vez dentro del seno esfenoidal, habiendo drilado todos los tabiques óseos, y ya realizada “la inspección anatómica” de todos los recesos y prominencias que allí se observan, debemos tomar reparo de los elementos subyacentes para realizar el abordaje deseado sin ninguna lesión a ellos. En este punto, es adecuado afirmar que, para nuestro equipo de trabajo, el reparo más importante a este nivel (y por una cuestión de frecuencia en la patología que tratamos día a día, quizás el más importante de este artículo) es el receso ópticocarotídeo medial (fig. 20). El ROCM21 reviste tal importancia por numerosas razones: es un punto de convergencia de la carótida paraselar, el nervio óptico, el seno cavernoso, la silla y la fosa craneal anterior. Por eso, representa un verdadero “key-hole” o “entry point” para acceder a cualquiera de esas estructuras, o bien como una guía o “barrera” para limitar la expansión de la osteotomía a realizar. Antiguamente se creía que el ROCM se correspondía con la apófisis clinoides media22, pero estudios anatómicos ulteriores demostraron que dicha prominencia no puede corresponderse con el ROCM debido a que éste último es una estructura lateral al tubérculo selar, mientras que la apófisis clinoides media es una estructura lateral a la silla turca21. Tal es la importancia que reviste que, por ejemplo, ante un caso de una lesión que involucre al quiasma óptico (como un meningioma del planum esfenoidal, fig. 21), la apertura dural en el ROCm. permitirá tener un control adecuado de las arterias perforantes subquiasmáticas para así disecarlas y evitar causar daño isquémico a ambos nervios ópticos y al tallo hipofisario.
Para ir finalizando esta sección del relato, creemos que es adecuado en este punto hacer referencia a un elemento noble que siempre debe ser tenido en cuenta, independientemente de que sea visible o no en determinado procedimiento. Se trata de la arteria carótida interna. La misma se comporta como un límite lateral para los abordajes en el plano sagital, pero como ya se ha nombrado incontables veces, los abordajes en plano coronal están en pleno perfeccionamiento, por lo que un conocimiento detallado de la anatomía endoscópica de la ACI es mandatoria. Clásicamente, se ha entendido a la ACI según el análisis propuesto por el profesor Albert Rhoton16, basada en cuatro segmentos según su localización: cervical o C1, petrosa o C2, cavernosa o C3 y supraclinoidea o C4; siendo este último segmento a su vez dividido en otros tres: oftálmico, comunicante y coroideo. Esta clasificación es extremadamente útil ya que tiene en cuenta las relaciones endocraneanas de la arteria, pero desde un punto de vista endoscópico no es quizás la más adecuada, fundamentalmente por las relaciones óseas de la ACI que no se aprecian desde un abordaje transcraneano clásico. Según nuestra perspectiva, nos parece más adecuada la división impuesta por Labib y Kassam23, debido a que representa de una manera más fidedigna las relaciones de la ACI con las diferentes estructuras de la base del cráneo. Según ellos, se reconocen 6 segmentos carotídeos:
- Parafaríngeo,
- Petroso,
- Paraclinoideo,
- Paraselar,
- Paraclinoidea, e
- Intradural.
La ACI parafaríngea es importante (desde un punto de vista endoscópico) sólo en el segmento superior al paladar blando. Este se encuentra limitado lateralmente por la rama medial del proceso pterigoideo y medialmente por la fascia faringobasilar (fig. 25). De aquí se desprende que el mejor reparo para entender dónde se encuentra la ACI parafaríngea sea la trompa de Eustaquio (figs. 25 y 28), en el aspecto más posterolateral y profundo de la fosa de Rossenmüller29.
La ACI petrosa, es decir, su segmento horizontal ubicado entre el orificio de entrada al canal carotídeo y el forámen lacerum, está insinuada como ya se vio en el espacio comprendido entre las dos líneas horizontales imaginarias que atraviesan los forámenes redondo y vidiano (fig. 27). El agujero vidiano es sin dudas el reparo más importante para inferir la posición de este segmento de la ACI debido a que, como se sabe, su orificio posterior se abre hacia el foramen lacerum (rasgado anterior), marcando el nervio vidiano un buen reparo del nivel en el que la ACI pasa de su segmento petroso al paraclival. El segmento paraclival se extiende desde su salida del foramen lacerum hasta el nivel del ápex petroso. Este segmento tiene una porción extracavernosa y otra intracavernosa, separadas por el ligamento petrolingual. En senos esfenoidales bien neumatizados, podemos inferir la localización de la ACI a los lados del receso clival (figs. 19 y 28).
A continuación, el segmento paraselar es quizás el más conocido y familiar, se extiende a los lados de la silla turca, siendo la prominencia selar y la mismísima prominencia carotídea los dos reparos a ser tenidos en cuenta para encontrar este segmento carotídeo. El mismo se extiende desde la entrada al segmento cavernoso hasta el anillo dural proximal, momento a partir del cual comienza el segmento paraclinoideo, que, como ya se sabe, es aquel comprendido entre ambos anillos durales proximal y distal. Sin lugar a dudas, el ROCM (fig. 20) es el gran reparo para localizar este segmento, pues recordemos que en su conformación interviene el arco óseo distal (DOA, fig. 20) que no es más que el reparo óseo que recubre al anillo dural distal. Una vez atravesado este anillo, comenzará en segmento intradural, por demás conocido por sus reparos intracraneales.
CONCLUSIÓN
La anatomía ósea y neurovascular de la base del cráneo es por demás rica, y aún en nuestros días continúa ampliándose su estudio y conocimiento. Los reparos óseos son incontables, y su relación en profundidad con los elementos neurovasculares es en verdad sorprendente y apasionante. Un buen conocimiento de la anatomía ósea de cada sector de la base del cráneo (tanto en la línea media como en la región paramediana) nos permitirá tener un control más certero sobre elementos como la ACI o los pares craneales. Si bien homogeneizar todo el conocimiento anatómico es una tarea titánica, creemos que es posible realizar una correlación anatómica entre los diferentes reparos observados en cada fosa craneal, con los aspectos más relevantes del conjunto de abordajes que aún dan en llamarse “abordaje endoscópico a la base del cráneo”.
BIBLIOGRAFÍA
- Amin Kassam, Carl H. Snyderman, Arlan Mintz, Paul Gardner, And Ricardo L. Carrau. Expanded endonasal approach: the rostrocaudal axis. Part I. Crista galli to the sella turcica. Neurosurg Focus 19 (1): E3, 2005
- Amin Kassam, Carl H. Snyderman, Arlan Mintz, Paul Gardner, And Ricardo L. Carrau. Expanded endonasal approach: the rostrocaudal axis. Part II. Posterior Clinoids to the foramen magnum. Neurosurg Focus 19 (1): E4, 2005
- Schwartz TH, Fraser JF, Brown S, Tabaee A, Kacker A, Anand VK. Endoscopic cranial base surgery: classification of operative approaches. Neurosurgery. May;62(5):991-1002. 2008
- Ainsworth T, Tessema B, Brown SM. Overview of endonasal corridors to intracranial targets. Op Tech Otolaryngol.;22(3):194–9. 2011
- Hosemann W., Schroeder H.W.S. Comprehensive review on rhino-neurosurgery. GMS Current Topics in Otorhinolaryngology - Head and Neck Surgery, Vol. 14 ISSN 1865-1011. 2015
- Gustavo Hadad, MD; Luis Bassagaisteguy, MD; Ricardo L. Carrau, MD; Juan C. Mataza, MD; Amin Kassam, MD; Carl H. Snyderman, MD; Arlan Mintz, MSc, MD. A Novel Reconstructive Technique After Endoscopic Expanded Endonasal Approaches: Vascular Pedicle Nasoseptal Flap. Laryngoscope, 116:1882–1886, 2006
- Emiro Caicedo-Granados, MD; Ricardo Carrau, MD; Carl H. Snyderman, MD; Daniel Prevedello, MD;Juan Fernandez-Miranda, MD; Paul Gardner, MD; Amin Kassam, MD. Reverse Rotation Flap for Reconstruction of Donor Site After Vascular Pedicled Nasoseptal Flap in Skull Base Surgery. Laryngoscope, 120:1550–1552, 2010
- Gustavo Hadad, MD; Carlos M. Rivera-Serrano, MD; Luis H. Bassagaisteguy, MD; Ricardo L Carrau, MD, FACS; Juan Fernandez-Miranda, MD; Daniel M. Prevedello, MD; Amin B. Kassam, MD. Anterior Pedicle Lateral Nasal Wall Flap: A Novel Technique for theReconstruction of Anterior Skull Base Defects. Laryngoscope, 121:1606–1610, 2011
- Carlos M. Rivera-Serrano, MD; Carl H. Snyderman, MD; Paul Gardner, MD; Daniel Prevedello, MD; Stephen Wheless, BS; Amin B. Kassam, MD; Ricardo L. Carrau, MD; Anand Germanwala, MD; Adam Zanation, MD. Nasoseptal ‘‘Rescue’’ Flap: A Novel Modification of the Nasoseptal Flap Technique for Pituitary Surgery. Laryngoscope, 121:990–993, 2011
- Aldo Cassol Stamm, MD, Shirley Pignatari, MD, PhD,Eduardo Vellutini, MD, Richard John Harvey, MBBS, and João Flávio Nogueira Jr, MD. A novel approach allowing binostril work to the sphenoid sinus. Otolaryngology–Head and Neck Surgery 138, 531-532. 2008
- Arévalo Román Pablo, Seclen Voscoboinik Daniel Alejandro, Herrera Juan Martín, Rojas Mauricio Gabriel, Vallejos Taccone Walter Emanuel, Mural Miguel. Abordaje endonasal endoscópico a la base del cráneo. Un estudio anatómico de sus alcances. Nuestra experiencia. REV ARGENT NEUROC VOL. 29, N° 3: 132-152. 2015.
- Carlos D. Pinheiro-Neto, MD; Juan C. Fernandez-Miranda, MD; Carlos M. Rivera-Serrano, MD; Alessandro Paluzzi, MD; Carl H. Snyderman, MD, MBA; Paul A. Gardner, MD; Luiz U. Sennes, MD. Endoscopic Anatomy of the Palatovaginal Canal (Palatosphenoidal Canal): A Landmark for Dissection of the Vidian Nerve During Endonasal Transpterygoid Approaches. Laryngoscope 122: January. 2012
- Aldo Cassol Stamm "Transnasal endoscopic skull base and brain surgery". Thieme, 2011.
- Ming Songa,b, Xuyi Zongc, Xinsheng Wangc, Ao Peid, Peng Zhaoc, Songbai Guic,Yaohua Yane, Yazhuo Zhang. Anatomic study of the anterior skull base via an endoscopic transnasal approach. Clinical Neurology and Neurosurgery 113 (2011) 281–284
- Vincent Patron, Julie Berkaoui1, Roger Jankowski Emmanuelle Lechapt-Zalcman Sylvain Moreau Martin Hitier. The forgotten foramina: a study of the anterior cribriform plate. Surg Radiol Anat. DOI 10.1007/s00276-015-1471-2. 2015
- Albert Rhoton Jr. M.D "Cranial anatomy and surgical approaches". Neurosurgery, 2000.
- Juan C. Fernández-Miranda, Alec Vaezi, Eugenio Ca rdenas, Carlos Pinheiro-Neto, Alessandro Paluzzi, Barton F. Branstetter, Paul A. Gardner, Carl H. Snyderman. Classification of Sphenoid Sinus Pneumatization: Relevance for Endoscopic Skull Base Surgery. Laryngoscope, 00:000–000, 2014.
- Juan C. Fernandez-Miranda, MD; Daniel M. Prevedello, MD; Ricky Madhok, MD; Victor Morera, MD;Juan Barges-Coll, MD; Katharine Reineman, MS; Carl H. Snyderman, MD; Paul Gardner, MD;Ricardo Carrau, MD; Amin B. Kassam, MD. Sphenoid Septations and Their Relationship With Internal Carotid Arteries: Anatomical and Radiological Study. Laryngoscope, 119:1893–1896, 2009.
- Alessandra Alfieri, M.D., Hae-Dong Jho, M.D., Ph.D. Endoscopic Endonasal Approaches to the Cavernous Sinus: Surgical Approaches. Neurosurgery 49:354–362, 2001.
- Alessandra Alfieri, M.D., Hae-Dong Jho, M.D., Ph.D. Endoscopic Endonasal Cavernous Sinus Surgery: An Anatomic Study. Neurosurgery 48:827–837, 2001.
- Mohamed Ahmed Labib, Daniel M. Prevedello, Juan C. Fernandez-Miranda, Sanan Sivakanthan, Arnau Benet, Victor Morera, Ricardo Carrau, Amin Kassam. The Medial Opticocarotid Recess: An Anatomic Study of an Endoscopic “Key Landmark” for the Ventral Cranial Base. Neurosurgery 72[ONS Suppl 1]:ons66–ons76, 2013.
- Juan C. Fernandez-Miranda, Matthew Tormenti, Fernando Latorre, Paul Gardner, Carl Snyderman. Endoscopic Endonasal Middle Clinoidectomy: Anatomic, Radiological, and Technical Note. Neurosurgery 71[ONS Suppl 2]:ons233–ons239, 2012.
- Mohamed A. Labib, Daniel M. Prevedello, Ricardo Carrau, Edward E. Kerr, Cristian Naudy, Hussam Abou Al-Shaar, Martin Corsten, Amin Kassam. A Road Map to the Internal Carotid Artery in Expanded Endoscopic Endonasal Approaches to the Ventral Cranial Base. Operative Neurosurgery 10:448–471, 2014.
- Amin B. Kassam, M.D., Daniel M. Prevedello, M.D., Ricardo L. Carrau, M.D.,Carl H. Snyderman, M.D., Ajith Thomas, M.D., Paul Gardner, M.D., Ada m Zanation, M.D., Bulent Duz, M.D., S. Tonya Stefko, M.D.,Karin Byers, M.D., and Micha el B. Horowitz, M.D. Endoscopic endonasal skull base surgery: analysis ofcomplications in the authors’ initial 800 patients. J Neurosurg, 114:1544–1568. 2011.
- Victor A. Morera, Juan C. Fernandez-Miranda, Daniel M. Prevedello, Ricky Madhok, Juan Barges-Coll, Paul Gardner, Ricardo Carrau, Carl H. Snydermann, Amin Kassam. “Far-Medial” Expanded Endonasal Approach to the Inferior Third of the Clivus: The Transcondylar and Transjugular Tubercle Approaches. Neurosurgery 66[ONS Suppl 2]:ons211-ons220, 2010.
- Arnau Benet, Daniel M. Prevedello, Ricardo L. Carrau, Jordina Rincon-Torroella, Juan C. Fernandez-Miranda, Alberto Prats-Galino, Amin B. Kassam. Comparative Analysis of the Transcranial “Far Lateral” and Endoscopic Endonasal “Far Medial” Approaches: Surgical Anatomy and Clinical Illustration. j.wneu.2013.01.091. 2013.
- Amin B. Kassam, Allan D. Vescan,Ricardo L. Carrau, Daniel M. Prevedello, Paul Gardner, Arlan H. Mintz,Ncarl H. Snyderman, M.D.,1,2 And Albert L. Rhoton Jr., M.D. Expanded endonasal approach: vidian canal as a landmark to the petrous internal carotid artery. J Neurosurg 108:177–183, 2008
- Pornthep Kasemsiri, MD; C. Arturo Solares, MD; Ricardo L. Carrau, MD; J. Drew Prosser, MD;Daniel M. Prevedello, MD; Bradley A. Otto, MD; Matthew Old, MD; Amin B. Kassam, MD. Endoscopic Endonasal Transpterygoid Approaches: Anatomical Landmarks for Planning the Surgical Corridor. Laryngoscope, 123:811–815, 2013
- Jianfeng Liu, MD, PhD; Carlos D. Pinheiro-Neto, MD, PhD; Juan C. Fernandez-Miranda, MD; Carl H. Snyderman, MD, MBA; Paul A. Gardner, MD; Barry E. Hirsch, MD; Eric Wang, MD. Eustachian Tube and Internal Carotid Artery in Skull Base Surgery: An Anatomical Study. Laryngoscope, 124:2655–2664, 2014
- Shigeyuki Osawa, M.D., Albert L. Rhoton, Jr., M.D. Askin Seker, M.D. Satoru Shimizu, M.D. Kiyotaka Fujii, M.D. Amin B. Kassam, M.D. Microsurgical And Endoscopic Anatomy Of The Vidian Canal. Neurosurgery 64[ONS Suppl 2]:ons385–ons412, 2009
- Ali M. Elhadi, MD, PhD, Hasan A. Zaidi, MD, Kaan Yagmurlu, MD,Shah Ahmed, BS, Albert L. Rhoton Jr., MD, Peter Nakaji, MD, Mark C. Preul, MD, Andrew S. Little, MD. Infraorbital nerve: a surgically relevant landmark for the pterygopalatine fossa, cavernous sinus, and anterolateral skull base in endoscopic transmaxillary approaches. J Neurosurg March 4, doi/abs/10.3171/2015.9.JNS151099. 2016.
